乙二醇又名甘醇, 是非常重要的一种化工基础原料.它不仅是用来制备聚酯纤维、聚酯树脂和醇酸树脂的主要单体, 同时还是防冻液、胶黏剂、增塑剂、表面活性剂等许多化工产品的原材料[1].目前, 乙二醇生产工艺大概分为两种:石油路线和非石油路线.石油路线主要以乙烯水合法合成乙二醇为主[2], 但该工艺存在工艺复杂、反应流程长、能耗高及乙二醇收率低等不足之处.而非石油路线即通过碳一路线制备乙二醇, 该方法反应条件温和、能耗低, 且符合对反应有利的热力学条件[3], 其合成路线主要分为两步:首先由合成气氧化偶联制得草酸二甲酯(DMO);然后DMO催化加氢制得乙二醇(EG)[4].众所周知, 我国化石能源整体呈现“贫油、少气、富煤”的现状, 因此开发合成气制乙二醇工艺, 对解决我国乙二醇的需求量大和节约石油资源具有深远的战略意义.但该工艺的关键在于高效催化剂的开发.
近年来, DMO催化加氢制乙二醇催化剂的研究一直是该领域的研究热点.其中, Cu基催化剂由于成本低及羰基加氢活性较高, 而广泛地用于酯加氢反应[5-8]. Chen等[6]采用蒸氨法合成Cu/SiO2催化剂, 并将其用于DMO加氢制乙二醇反应, DMO的转化率高达99.9%, 但EG的选择性仅为95.0%.上述Cu基催化剂虽在DMO加氢反应中具有较高的催化活性, 但均存在活性组分易团聚、催化剂易失活、制备流程繁琐等问题, 这一直制约着Cu基催化剂的工业化应用[9-11].
提高催化剂稳定性常用的方法是对催化剂活性组分或载体进行改性. Wen等[12]研究发现, Cu-SiO2催化剂失活的原因之一是载体发生了变化.在DMO甲醇溶液中, SiO2反应生成正硅酸甲酯, 导致催化剂的比表面积减小, 继而催化剂活性降低.我们采用水热合成法制备的Cu-HMS催化剂能显著提高DMO的催化加氢性能.对Cu/SiO2催化剂, 不同Cu负载量对其催化性能有较大的影响[13].因此, 我们研究了不同铜负载量对DMO催化加氢性能的影响, 并通过XRD, BET, FI-IR, H2-TPR, TEM等手段对该催化剂的结构特性进行了详细表征.
1 实验部分 1.1 试剂本实验所需试剂如下, 草酸二甲酯: EP, 上海中秦化学化学试剂有限公司;甲醇: AR, 天津市光复科技发展有限公司;十六胺: AR, 上海中秦化学化学试剂有限公司;硝酸铜: AR, 天津市大茂化学试剂厂;正硅酸乙酯、乙醇酸甲酯: AR, 上海中秦化学化学试剂有限公司;无水乙醇: AR, 天津市富宇精细化工有限公司;异丙醇: AR, 天津市鼎盛鑫化工有限公司;乙二醇: AR, 国药集团化学试剂有限公司.
1.2 催化剂的制备催化剂采用水热合成法制备.具体步骤如下:先将适量的十六胺(模板剂)溶于63.00 g去离子水和32.20 g乙醇组成的溶液中, 在50 ℃下搅拌形成A溶液;再将一定量的Cu(NO3)2·3H2O溶于异丙醇和正硅酸乙酯(TEOs)组成的混合溶液中, 搅拌溶解, 形成B溶液.将溶液B快速倒入溶液A中, 在50 ℃下搅拌18 h, 所得产物离心分离, 并置于110 ℃下干燥24 h, 后经450 ℃焙烧4 h即可.分别制得铜负载量(理论铜负载量)在10%、15%、20%以及30%的Cu-HMS催化剂, 催化剂记为x-Cu-HMS, 其中x代表不同的铜负载量.制得的催化剂研磨后采用粉末压片机压片过筛, 然后筛分出粒径0.450~0.280 mm的催化剂留用.
1.3 催化剂表征采用日本Rigaku Ultima Ⅳ型X射线衍射仪对催化剂试样进行XRD衍射分析, 用Cu(Kα)射线(波长λ = 0. 154 056 nm)照射催化剂, 管电压40 kV, 管电流40 mA, 扫描速度4 °/min, 扫描步长0.02°, 2 θ=5°~80°.样品的比表面积(BET)测定在美国康塔公司生产的NOVA4000e型物理吸脱附仪上完成.试样在300 ℃下真空预处理3 h, 以N2为吸附质, 在液氮温度(-196 ℃)下进行吸附, 比表面积采用BET方程计算得到. FT-IR表征是在德国Bruker公司生产的带有DTGS检测器的IFS120HR型红外光谱仪上进行. H2-TPR实验在TP5090全自动多用吸附仪装置上进行, 催化剂用量20 mg, 催化剂先经300 ℃、Ar气预处理60 min后降至室温, 再以5% H2-95% Ar为还原气, 流速20 mL/min, 升温速率为10 K/min, 热导检测耗氢量.采用美国FEI公司生产的TECNAI G2 TF20型场发射透射电子显微镜观察催化剂的微观形貌.
1.4 活性评价该催化剂在带有不锈钢管(内径0.9 cm, 恒温区长度为35 cm)的固定床反应装置上进行活性评价.实验中, 将1.20 g的催化剂(粒径0.450~0.280 mm)装入反应管中部.常压下, 以100 mL/min的流量通入H2, 升温至350 ℃后还原4 h.待温度降至205 ℃时, 将压力升至2.0 MPa, 氢酯比保持在80 mol/mol、DMO液时空速为0.4 h-1的条件下, 在此条件下用双柱塞微量进样泵将质量分数为10%的DMO甲醇溶液注入到反应管中, 反应开始计时, 冷凝后取样分析.产物采用岛津GC2014c气相色谱仪分析结果, 检测器为氢火焰检测器(FID).进样器温度250 ℃, 检测器温度260 ℃, 柱温采用程序升温, 45 ℃保留1.5 min, 然后以30 ℃/min的升温速率升至85 ℃, 保留5 min, 再以30 ℃/min的升温速率升至200 ℃, 保留2 min.采用面积归一法定量.
催化反应转化率和选择性计算方法如下(以下公式皆是摩尔比).
DMO的转化率:
| $ {\rm{X}} = \frac{{{\rm{The}}\;{\rm{amount}}\;{\rm{of}}\;{\rm{DMO}}\;{\rm{converted}}}}{{{\rm{The}}\;{\rm{amount}}\;{\rm{of}}\;{\rm{DMO}}\;{\rm{material}}\;{\rm{entering}}\;{\rm{the}}\;{\rm{reactor}}}} \times 100\% $ |
EG的选择性:
| $ {\rm{S}} = \frac{{{\rm{The}}\;{\rm{amount}}\;{\rm{of}}\;{\rm{EG}}\;{\rm{generated}}}}{{{\rm{The}}\;{\rm{amount}}\;{\rm{of}}\;{\rm{DMO}}\;{\rm{converted}}}} \times 100\% $ |
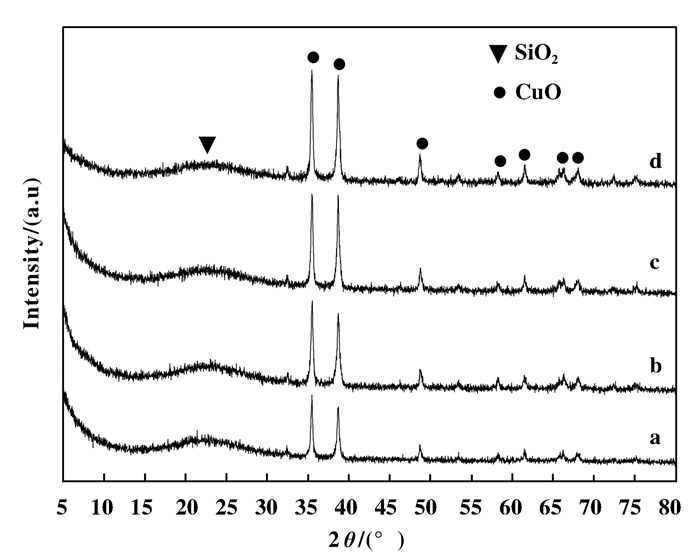
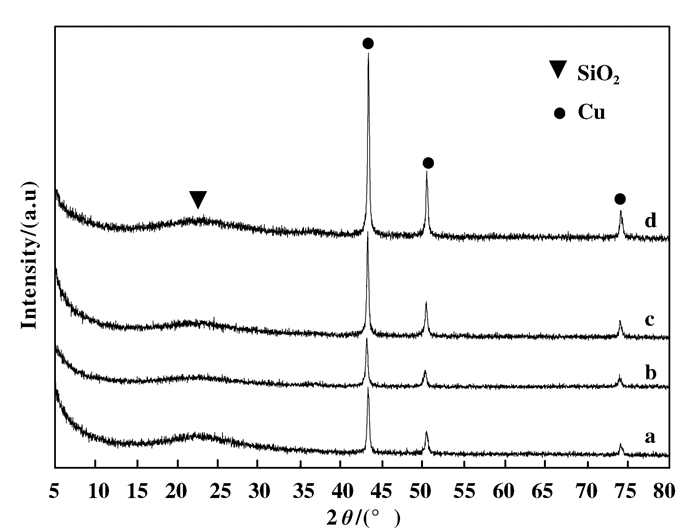
图 1、2分别为不同铜含量的Cu-HMS催化剂还原前后的XRD图谱.由图可知, 还原前后都具有SiO2(2θ=23°附近)的特征衍射峰, 而还原前铜物种以CuO物相(2 θ=35.5°、38°和48°等处)的形式存在, 还原后在2θ=43°、51°及74°附近出现金属Cu物相的特征衍射峰, 且随着铜负载量的增加, CuO和Cu的晶相峰均有一个缓慢变大的趋势, 表明Cu负载量过大会导致活性组分在催化剂表面出现团聚现象.同时, 在还原后的XRD图中未观察到Cu+的特征峰, 说明影响DMO催化加氢制EG反应活性的是催化剂表面的零价Cu.另外, 由Debye-Scherrer公式计算得到还原后Cu粒径大小在表 1中可以看到, 随着铜负载量的增加, 铜颗粒的平均粒径先变小后增大, 但总体上变化不明显, 说明在一定程度上尺寸效应对该催化反应有一定的影响.
|
图 1 不同铜负载量的Cu-HMS催化剂还原前的XRD图谱 Figure 1 XRD patterns of Cu-HMS catalysts of different copper loadings before reduction a. 10-Cu-HMS; b. 15-Cu-HMS; c. 20-Cu-HMS; d. 30-Cu-HMS |
|
图 2 不同铜负载量的Cu-HMS催化剂还原后的XRD图谱 Figure 2 XRD patterns of Cu-HMS catalysts of different copper loadings after reduction a. 10-Cu-HMS; b. 15-Cu-HMS; c. 20-Cu-HMS; d. 30-Cu-HMS |
表 1显示了载体及不同铜负载量催化剂的理化参数.从表 1可以看出, 载体HMS的比表面积、孔体积及平均孔径都比催化剂的高.随着铜负载量的增加, 催化剂的比表面积先增加后减小, 同时介孔体积及平均孔径总体呈现下降的趋势.这可能是由于铜负载量较高使金属Cu发生了某种积聚作用, 或者是SiO2骨架发生了崩解及重组;也可能是在制备过程中, 产生了含有大量小孔的特殊结构页硅酸铜[14].当Cu负载量在30%时, 催化剂比表面积明显降低仅有569.7 m2·g-1, 远低于20-Cu-HMS催化剂的比表面积(785.1 m2·g-1), 这是因为Cu负载量较高导致Cu粒子堵塞了载体孔道.
| 表 1 载体及不同铜负载量Cu-HMS催化剂的理化参数 Table 1 Physicochemical parameters of the carrier and Cu-HMS of different copper loading Catalyst |
图 3是不同铜负载量的Cu-HMS样品及载体HMS的FT-IR谱图.其中462、805和1 078 cm-1附近的特征峰分别是载体中Si—O—Si键的不同振动模式.在3 430 cm-1附近出现宽吸收峰是由于吸附水和硅烷醇-OH振动峰的重叠导致的, 该峰变宽与邻近-OH的氢键度有关[15].而1 635 cm-1处的特征峰与吸附水的-OH弯曲振动峰相对应[16].此外, 在1 050 cm-1附近出现一个Cu—O—Si的特征峰, 且随着铜负载量的增加, 该特征峰逐渐增强而1 078 cm-1处的Si—O—Si特征峰逐渐减弱并消失, 同时这两个特征峰发生重叠. 1 078 cm-1附近的特征峰迁移到1 050 cm-1处, 是由于大量的Cu与SiO2相结合, 从而导致它们之间的相互作用变强[17].当持续增加铜负载量时, 1 078 cm-1处的Si—O—Si特征峰消失, 这可能是过量的Cu覆盖了载体HMS, 且导致催化剂比表面积及孔体积大幅度降低, 这与表 1中30-Cu-HMS的数据相吻合.

|
图 3 载体和不同铜负载量Cu-HMS催化剂的FT-IR图谱 Figure 3 FT-IR spectra of Cu-HMS catalyst with different copper loadings and carrier a. HMS; b. 10-Cu-HMS; c. 15-Cu-HMS; d. 20-Cu-HMS; e. 30-Cu-HMS |
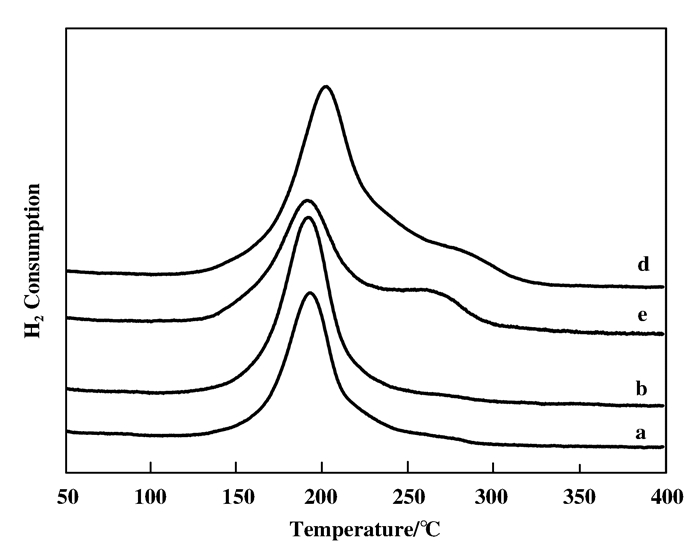
图 4是不同铜负载量的Cu-HMS催化剂的H2-TPR图谱.从图 4中可以发现不同的Cu-HMS催化剂均在200 ℃附近出现了一个还原峰, 这与该催化剂上高分散CuO的还原峰相对应.随着铜负载量的增加, 催化剂中CuO的还原峰温度由190逐渐升高到205 ℃, 且还原峰的对称性越来越差, 说明该催化剂的分散状态逐渐变差, 且活性组分分散良好有利于催化剂的还原[18].由图 4观察到20-Cu-HMS、30-Cu-HMS这两个催化剂都出现了两个还原峰, 说明该催化剂还存在另外一种形式的铜物种, 可能是在还原过程中生成了页硅酸铜, 这与从BET中得出的结论相符合.查阅文献可知[19], 出现低温还原峰是铜物种分散较好的原因, 且铜物种与SiO2间的相互作用力较弱;高温还原峰的出现是由于铜负载量过大而引起铜物种团聚, 导致铜物种与SiO2间的相互作用力变大.这表明铜负载量对Cu与SiO2间的相互作用有很大的影响.
|
图 4 不同铜负载量的Cu-HMS催化剂的H2-TPR图谱 Figure 4 H2-TPR spectra of Cu-HMS catalysts with different copper loadings a. 10-Cu-HMS; b. 15-Cu-HMS; c. 20-Cu-HMS; d. 30-Cu-HMS |
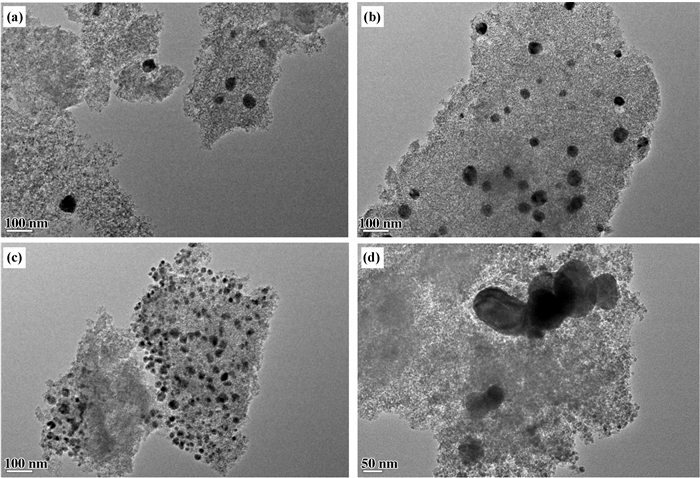
图 5展示了不同铜负载量的Cu-HMS样品在还原后的代表性TEM图像.由图a-d可以明显看到铜粒子的分散情况, 并通过观察Cu颗粒的大小及数量可得知铜负载量逐渐增加.同时, 出现了典型地虫孔结构, 这可能是由于在制备过程中TEOS的自组装效应导致的. 图 5c是还原后的20-Cu-HMS样品的TEM图, 可以看到浅灰色SiO2颗粒与黑色的Cu颗粒, 且铜粒子大小均一、分散良好.还原后30-Cu-HMS样品的TEM图(图 5d), 表明随着铜负载量的不断增加, HMS骨架中铜粒子明显聚集且介孔结构恶化, 从而导致催化剂比表面积降低, 这与相应的XRD、BET数据相符.
|
图 5 还原后不同铜负载量的Cu-HMS催化剂TEM图像 Figure 5 TEM images of Cu-HMS catalysts with different copper loadings after reduction a. 10-Cu-HMS; b. 15-Cu-HMS; c. 20-Cu-HMS; d. 30-Cu-HMS |
表 2列出了在2.0 MPa、205 ℃、氢酯比为80 mol/mol、DMO的液时空速为0.4 h-1的反应条件下, 不同Cu负载量的催化剂对应的DMO转化率和产物选择性数据.从表 2中可以看到, DMO催化加氢反应的产物主要有乙二醇(EG)、乙醇(EtOH)、乙醇酸甲酯(MG)及其它副产物如1, 2-丙二醇(1, 2-BDO)等.从而得出DMO催化加氢制EG是多重连续反应:首先DMO与H2反应生成中间产物MG, MG继续与H2反应得到目标产物EG, 但EG进一步反应会生成副产物EtOH、1, 2-BDO等[20].由表 2可知, 在一定的反应条件下, 随着铜负载量的增加, DMO的转化率和EG的选择性都表现出先增大后减小的趋势, 当Cu负载量在20%时, Cu-HMS催化剂的催化性能最优, DMO的转化率接近100%, 而EG的选择性高达98.11%;此外, MG的选择性先降低再升高, 表明催化剂的催化加氢性能先增强后变弱.
| 表 2 不同铜负载量对DMO加氢性能的影响 Table 2 Effect of different copper loading for DMO hydrogenation performance |
实验结果表明, 采用水热合成法制备的20-Cu-HMS催化剂, 具有较高的比表面积、加氢能力较强、铜颗粒分散良好、粒径均一且反应条件较温和的优势.该催化剂在催化DMO加氢制乙二醇的反应中表现出优异的催化性能, 在压力为2.0 MPa、温度为205 ℃、氢酯比为80 mol/mol、DMO的液时空速为0.4 h-1的反应条件下, 反应4 h后EG的收率高达98.11%.通过一系列表征手段, 发现铜负载量对该催化剂中铜颗粒的分散和Cu与SiO2间的相互作用有较大的影响.
| [1] | Zhang Hai-song(张海松). Technical advance on the indirect method to synthesis ethylene glycol by syngas(合成气间接制乙二醇技术的进展)[J]. Chem Engineer Des Commun(化工设计通讯), 2009, 35(4): 37–40. |
| [2] | Li Y C, Yan S R, Yue B, et al. Selective catalytic hydration of ethylene oxide over niobium oxide supported on α-alumina[J]. Appl Catal A:Gener, 2004, 272(1/2): 305–310. |
| [3] | Yin An-yuan(尹安远), Dai Wei-lin(戴维林), Fan Kang-nian(范康年). Thermodynamics of Ethylene Glycol Synthesis via Hydrogenation of Dimethyl Oxalate(草酸二甲酯催化加氢合成乙二醇过程的热力学计算与分析)[J]. Petrochem Technol(石油化工), 2008, 37: 62–66. |
| [4] | Yin A Y, Guo X Y, Dai W L, et al. Highly active and selective copper-containing HMS catalyst in the hydrogenation of dimethy loxalate to ethylene glycol[J]. Appl Catal A:Gener, 2008, 349(1/2): 91–99. |
| [5] | Zhao S, Yue H, Zhao Y, et al. Chemoselective synthesis of ethanol via hydrogenation of dimethyl oxalate on Cu/SiO2:Enhanced stability with boron dopant[J]. J Catal, 2013, 297(1): 142–150. |
| [6] | Chen L F, Guo P J, Qiao M H, et al. Cu/SiO2 catalysts prepared by the ammonia-evaporation method:Texture, structure, and catalytic performance in hydrogenation of dimethyl oxalate to ethylene glycol[J]. J Catal, 2008, 257: 172–180. DOI:10.1016/j.jcat.2008.04.021 |
| [7] | Zhu Y M, Li S. Zn promoted Cu-Al catalyst for hydrogenation of ethyl acetate to alcohol[J]. J Ind Eng Chem, 2014, 20(4): 2341–2347. DOI:10.1016/j.jiec.2013.10.010 |
| [8] | Zhu Y M, Wang X, Shi L. Hydrogenation of ethyl acetate to ethanol over bimetallic Cu-Zn/SiO2 catalysts prepared by means of coprecipitation[J]. Bull Korean Chem Soc, 2014, 35(1): 141–146. |
| [9] |
a. Lin J D, Zhao X Q, Cui Y H, et al. Effect of feedstock solvent on the stability of Cu/SiO2 catalyst for vapor-phase hydrogenation of dimethyl oxalate to ethylene glycol[J]. Chem Commun, 2012, 48(8):1177-1179. b. Wang Xiao-xiao(王潇潇),Liu Zhen-min(刘振民),Guo Shao-qing(郭少青), et al. Study on methylation of naphthalene with methanol over SAPO-11 zeolites modified by Cu (Cu改性SAPO-11分子筛催化萘和甲醇甲基化反应的研究)[J]. J Mol Catal(China)(分子催化), 2016, 30(5):435-443. c. Sun Pei-yong(孙培永),Luo Xue-qing(罗学清),Zhang Sheng-hong(张胜红), et al. Deactivation and regeneration of Cu/B/Ca/Al2O3 catalysts for the hydrogenation of sec-butyl acetate(醋酸仲丁酯加氢反应中Cu/B/Ca/Al2O3催化剂的失活及再生)[J]. J Mol Catal(China)(分子催化), 2016, 30(3):226-233. d. Di Yan-bing(狄艳冰),Xiao Zi-hui(肖子辉),Di Xin(邸鑫), et al. Hydrogenolysis of glucose to value-added C2-C4 compounds over bimetallic NiCu/MgO catalysts(双金属NiCu/MgO催化剂上葡萄糖氢解制备高附加值C2-C4化学品)[J]. J Mol Catal(China)(分子催化), 2016, 30(4):324-337. e. Lu Peng(吕鹏), Xu Ding(徐钉), Shen Dong-ming(申东明), et al. Preparation of Cu-based catalyst by solid-phase grinding method with citric acid assisting and performance research in methanol synthesis reaction from CO2 hydrogenation(柠檬酸辅助固相研磨法制备铜基催化剂及在CO2加氢合成甲醇反应中的性能研究)[J]. J Mol Catal(China)(分子催化), 2017, 31(2):141-151. |
| [10] | Wen C, Li F, Cui Y, et al. Investigation of the structural evolution and catalytic performance of the CuZnAl catalysts in the hydrogenation of dimethyl oxalate to ethylene glycol[J]. Catal Today, 2014, 233: 117–126. DOI:10.1016/j.cattod.2013.10.075 |
| [11] | Huang H, Cao G, Fan C, et al. Effect of water on Cu/Zn catalyst for hydrogenation of fatty methyl ester to fatty alcohol[J]. Korean J Chem Engineer, 2009, 26(6): 1574–1579. DOI:10.1007/s11814-009-0267-7 |
| [12] | Wen C, Cui Y Y, Dai W L, et al. Solvent feedstock effect:the insights into the deactivation mechanism of Cu/SiO2 catalysts for hydrogenation of dimethyl oxalate to ethylene glycol[J]. Chem Commun, 2013, 49(45): 5195–5197. DOI:10.1039/c3cc40570b |
| [13] | Ma Jun-guo(马俊国), Ge Qing-jie(葛庆杰), Xu Heng-yong(徐恒泳). Effect of copper content on the performance of Cu/SiO2 catalyst for dimethyl oxalate hydrogenation to ethylene glycol(铜含量对草酸二甲酯加氢制乙二醇Cu/SiO2催化剂性能的影响)[J]. Nat Gas Chem Ind(天然气化工), 2016, 41(06): 10–14. |
| [14] | Grift C J G V D, Elberse P A, Mulder A, et al. Preparation of silica-supported copper catalysts by means of de-position-precipitation[J]. Appl Catal, 1990, 59: 275–289. DOI:10.1016/S0166-9834(00)82204-6 |
| [15] | Chaminand J, Djakovitch L A, Gallezot P, et al. Glyce-rol hydrogenolysis on heterogeneous catalysts[J]. Green Chem, 2004, 6(8): 359–361. DOI:10.1039/b407378a |
| [16] | Henrist C, Traina K, Hubert C, et al. Study of the morphology of copper hydroxynitrate nanoplatelets obtained by controlled double jet precipitation and urea hydrolysis[J]. J Crys Grow, 2003, 254(1): 176–187. |
| [17] | Zhang B, Hui S G, Zhang S H, et al. Effect of copper loading on texture, structure and catalytic performance of Cu/SiO2 catalyst for hydrogenation of dimethyl oxalate to ethylene glycol[J]. J Nat Gas Chem, 2012, 21: 563–570. DOI:10.1016/S1003-9953(11)60405-2 |
| [18] | Cong Yu(丛昱), Bao Xin-he(包信和), Zhang Tao(张涛), et al. Characterization of ultrafine Cu-ZnO-ZrO2 catalysts for methanol synthesis via CO2 hydrogenation(CO2加氢合成甲醇的超细CuZnO-ZrO2催化剂的表征)[J]. Chin J Catal(催化学报), 2000, 21(4): 314–318. |
| [19] | Robinson W R A M, Mol J C. Support effects in methanol synthesis over copper-containing catalysts[J]. Appl Catal, 1991, 76(1): 117–129. DOI:10.1016/0166-9834(91)80008-K |
| [20] | Gong J L, Yue H R, Zhao Y J, et al. Synthesis of ethanol via syngas on Cu/SiO2 catalysts with balanced Cu0-Cu + sites[J]. J Am Chem Soc, 2012, 134: 13922–13925. DOI:10.1021/ja3034153 |
 2018, Vol. 32
2018, Vol. 32

