卤代芳香族化合物作为有机化学中一类对人们生活具有重要作用的化学品, 在食品、药物等方面有着不可替代的地位.但是伴随着卤代物的广泛使用, 一系列的环境问题也逐渐暴露出来[1-4].由于卤代物尤其是氯代物等具有很高的稳定性, 如何在温和条件下脱卤素以降低污染物的毒性一直困扰着人们.因此卤代物污染的治理和资源化利用就成为制约着相应企业发展的一个因素[5-8].工业上往往是利用多相催化剂和廉价的还原剂在高温条件下进行脱卤素反应, 或者是利用均相催化剂和强还原剂进行脱卤素反应.前者一般会因为苛刻的反应条件产生积碳从而使得催化剂的活性降低得很快[9-11], 后者往往会因为在均相体系中产物难以分离且催化剂难以循环利用使得反应成本升高[12-14], 同时反应后对体系的处理容易造成对环境的二次污染[15].为了能够在温和条件下使卤代物快速高效脱卤素, 科研工作者制备并尝试了各种新型催化剂.
近些年来纳米粒子的出现为人们提供了一种新的研究思路, 尤其是过渡族贵金属类纳米粒子以其较高的催化活性引起了研究者的关注.但是单一的金属催化剂往往具有易失活、选择性差等缺点.为了解决上述问题, 人们研究了多元催化剂(例如AgAu、PdAg、FePt等二元催化剂).针对卤代芳香类化合物的脱卤反应, 有文献报道了PdCl2-M双金属催化剂, 此类催化剂的催化活性以及重复催化性能明显高于单金属Pd催化剂[16-18].负载型的多相纳米催化剂以其易分离的优势得到了人们的青睐[19-20], 但是多相催化剂往往需要苛刻的反应条件, 催化活性也相对较低.纳米粒子的尺寸对催化剂活性具有很大的影响, 当催化剂粒子尺寸小于10 nm时, 催化剂具有极高的催化活性[21].由于金属粒子需要负载于固体载体上, 因此如何设计载体也成为制约着催化剂催化效率的一个因素, 例如PtPd负载于活性炭上的催化剂脱氯需要250 ℃的苛刻条件[22], 而负载于TiO2载体上的PtPd纳米粒子的脱卤素转化率只有56%[23], 负载碳酸钙上的Pd纳米粒子的催化转化率也只有18%[24].但是Nguyen等[25]报道了负载于三联吡啶上的Pd纳米粒子均相催化剂, 对于卤代物的脱卤素在较长时间的情况下转化率可以达到90%左右.虽然均相催化剂具有很高的催化活性, 但是其很难从体系中分离出来, 造成了极大的浪费和环境污染.综合均相催化剂和多相催化剂的优点, 我们设计了一种新型准均相催化剂.它不仅具有均相催化剂的高活性, 同时也具有多相催化剂易分离的特点.催化剂制备过程中所用的聚酰胺酸是合成聚酰亚胺的前驱体, 其合成工艺简单并且十分成熟.实验中以三乙醇胺为成盐剂, 聚酰胺酸为稳定剂, NaBH4为还原剂, 将Pt和Pd还原得到聚酰胺酸稳定的纳米粒子.作为一种水相的新型准均相催化剂, 具有单金属催化剂所不具有的超高活性, 可以在温和的条件下对卤代物通过催化加氢实现快速脱卤素.
1 实验部分 1.1 实验原料HT3, 3’, 4, 4’-二氨基二苯醚(ODA), 上海嘉辰化工有限公司, 分析纯; 4, 4’-二苯酮四酸二酐(BTDA), 北京马尔蒂科技有限公司, 分析纯; 氯化钯(PdCl2), 氯铂酸(H2PtCl6), 3-氯苯酚, 3-溴苯酚, 4-碘苯酚, 2-氯苯胺, 4-氯苯胺, 4-溴苯胺, 2-氯苯甲醚, 2-氨基-4-氯苯酚, 2-溴-4-氯苯酚, 2, 4-二氯苯酚, 3, 4-二氯苯酚, 2, 4-二氯苯甲腈, 2, 4, 6-三氯苯酚, 2, 4, 5-三氯苯甲腈, 2, 6-二氯-4-溴苯酚等, 百灵威科技有限公司; N, N-二甲基甲酰胺(DMF), 三乙醇胺(TEA), 硼氢化钠(NaBH4), 乙酸乙酯, 国药集团化学试剂有限公司, 分析纯.
1.2 催化剂的表征铂钯合金纳米粒子的晶体结构和结晶状态通过X射线衍射仪(D/max 2500/PC)进行分析, 通过调节PtPd/PAAS溶液的pH约为2, 得到黑色沉淀, 用丙酮和去离子水反复洗涤, 将沉淀物室温真空干燥后覆于XRD载玻片, 压平即可.铂钯合金纳米粒子的形貌和尺寸使用透射电子显微镜(TITAN G2 60-300)进行观察, 通过将PtPd/PAAS溶液滴加于碳膜铜网上并室温晾干即可得到样品.
1.3 催化剂的制备首先, 根据文献方法由ODA和BTDA在DMF中通过缩聚反应制得聚酰胺酸(PAA)粉末[26].将摩尔比为1: 1的PAA粉末和三乙醇胺混合, 并加入适量的水制得100 mmol/L的聚酰胺酸盐(PAAS)溶液并冷藏待用.取适量PdCl2与两倍摩尔量的NaCl混合加入去离子水制得50 mmol/L的Na2PdCl4溶液.取Na2PdCl4(50 mmol/L)溶液200 μL, H2PtCl6(50 mmol/L)溶液200 μL, 充分混合后加入200 μL PAAS溶液并加适量的去离子水调节溶液体积至9 mL并置于冰水浴中快速搅拌30 min使得金属离子与PAAS充分混合, 然后快速加入新配制得NaBH4溶液(1 mL, 100 mmol /L)在冰水浴中快速搅拌2 h得到10 mL浓度为1 mmol/L聚酰胺酸负载的铂钯纳米粒子催化剂.将得到的催化剂置于冰箱中在4 ℃的条件下冷藏保存.
1.4 卤代芳香族物的氢化脱卤反应以3-氯苯酚的氢化脱卤反应为例, 取PtPd/PAAS溶液(1 mmol/L, 2 mL)置于反应瓶中, 加入3-氯苯酚(0.2 mmol)和Na2CO3(0.2 mmol), 在一个大气压的氢气中, 室温下剧烈搅拌反应.反应进程使用气相色谱仪(GC-2014C)进行监测.反应结束后, 将反应溶液的pH调至6左右, 分离出产物, 然后将剩余水相的pH调至2, 催化剂发生沉淀, 通过离心的方法可将催化剂回收.
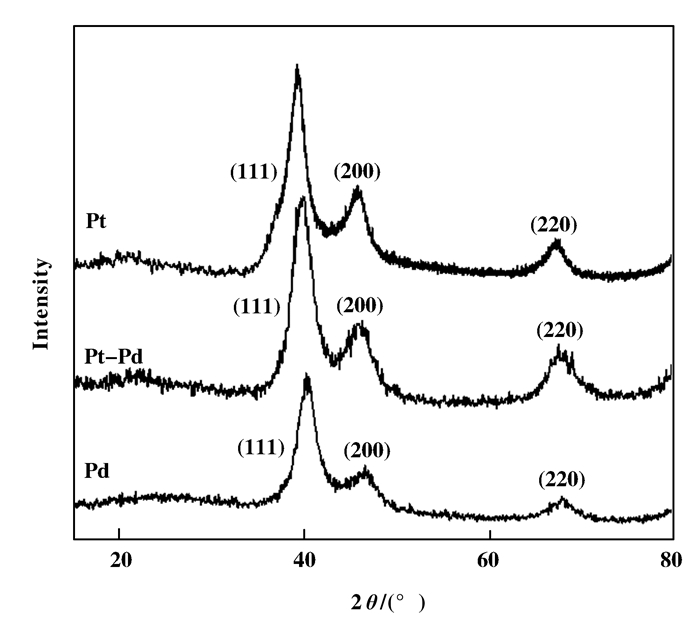
2 结果与讨论 2.1 PtPd/PAAS合金纳米催化剂的结构与形貌由图 1中PtPd/PAAS的XRD图像中2θ = 39.51°, 2θ=39.85°, 2θ =40.12°时的衍射峰分别为铂, 铂钯合金, 钯的(111)晶面的衍射峰, 结果表明了其中的铂离子和钯离子都被还原, 铂钯纳米粒子(111)晶面衍射峰所处的角度介于铂纳米粒子和钯纳米粒子之间, 说明铂钯确实以合金的形式存在, 并且宽化的衍射峰说明了合金纳米粒子的尺寸较小, 通过谢乐公式计算得到纳米粒子的粒径约为4 nm.
|
图 1 Pt/PAAS, Pd/PAAS和PtPd/PAAS的XRD图 Figure 1 X-ray patterns of Pt/PAAS, Pd/PAAS and PtPd/PAAS |
图 2是PtPd/PAAS的透射电子显微镜照片, PtPd-NPs的粒径分布图以及HRTEM.在图(a)中可以清晰地观察到PtPd纳米粒子分布均匀并且在自然状态下大都为球形或类球形, 通过粒径分布图可以得知PtPd纳米粒子粒径分布主要集中于3到5 nm的范围内, 平均尺寸约为4±1 nm.由图(b)PtPd/PAAS的高分辨率透射电子显微镜得到的纳米粒子(100)面的图像, 可以看出铂钯合金纳米粒子呈面心立方(FCC)的嵌套结构, 这与铂钯合金具有FCC结构相吻合[27].这就说明了1: 1的PtPd纳米粒子具有稳定的晶体结构, 这一特点保证了催化剂在反应过程中不会因为晶体结构不稳定而导致失活.

|
图 2 PtPd/PAAS的TEM照片和金属的粒径分布(a)以及HRTEM(b) Figure 2 TEM image, size distribution of PAAS-stabilized PtPd-NPs(a) and HRTEM of PtPd/PAAS(b) |
以3-氯苯酚的氢化脱氯反应作为模型反应进行反应条件的探究, 因为反应生成的氯化氢会导致溶液呈酸性, 所以加入了等摩尔量的碳酸钠去中和.如表 1所示, 在常温下反应1 h后, 不同铂钯摩尔比的催化剂对3-氯苯酚催化加氢的影响.在只加入PAAS和Na2CO3(编号1)的情况下底物并没有发生转化, 这说明了载体没有催化活性.经过对比(编号7和编号2, 3)实验, 可以发现铂钯合金的催化活性明显高于单金属铂或钯, 这是由于铂钯合金具有协同效应.另外通过对比发现铂钯合金纳米粒子的催化活性也受到金属摩尔比的影响, 当铂钯摩尔比为1: 1时, 其催化活性最高, 可以使卤代物脱卤素的转化率达到99%.然而以其他配比制备得到的铂钯纳米粒子催化活性较低, 这是因为铂和钯的单金属都是面心立方结构, 以1: 1的比例形成的新合金能够稳定存在, 在催化过程中纳米粒子也能够稳定存在, 而其他比例的催化剂表面稳定性稍差, 在催化脱氯反应时表面原子会发生重排, 进而较大程度上降低了催化活性.通过编号6、11可以发现Na2CO3和NaOH的加入都能促进底物的转化, 而且强碱性的NaOH能在更短的时间内使转化率达到99%, 并且溶液中金属粒子始终处于均匀分布的状态.加氢脱卤时生成的HCl会降低溶液的pH, 使得聚酰胺酸分子链蜷曲, 催化剂从溶液中析出, 因此用来助催化的碱性物质在中和盐酸维持体系pH上显得至关重要.
| 表 1 铂钯纳米粒子催化3-氯苯酚的氢化脱氯反应 Table 1 The PAAS-stabilized PtPd nanoparticles catalyze dechlorination of 3-chlorophenol |
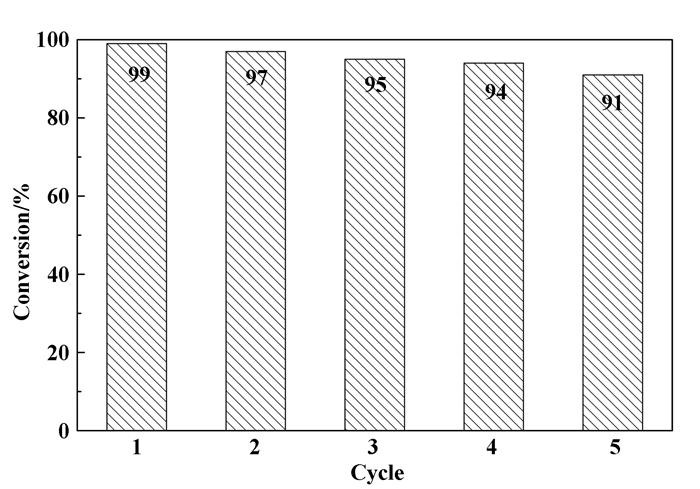
催化剂的稳定性是评估其优劣的另一项标准, 所以在最优条件下, 我们对3-氯苯酚的氢化脱氯模型反应进行了5次重复试验.每次反应结束后, 用HCl将溶液调至酸性(pH=2), 经离心洗涤后将所得黑色沉淀物重新分散至碱性水溶液中(pH=9), 回收得到的深黑色溶液用于下一次的催化反应.纳米粒子的回收效率可以借助ICP-AES分析, 结果显示离心得到的上清液中残留的铂、钯金属浓度分别约为10-2 mmol/L, 而重分散的金属纳米粒子溶液中的铂、钯金属浓度分别约为0.99 mmol/L, 这表明催化剂几乎可以完全回收利用. 图 3是催化剂对3-氯苯酚脱氯的重复性实验的结果, 可以看出在5次重复实验中催化剂的催化活性虽有略微降低, 但底物的转化率始终在90%以上, 这说明催化剂在多次循环催化过程中仍然稳定, 而且始终保持着高催化活性.
|
图 3 PtPd-PAAS对3-氯苯酚的重复催化 Figure 3 Recycling of PtPd-PAAS in the dechlorination of 3-chlorophenol |
图 4是进行5次循环催化后PtPd-PAAS的TEM照片, 从图中可以看出5次循环催化以后催化剂粒子仍然保持原有形貌并且保持着良好的分散性, 表明催化剂在多次催化以后依然可以稳定存在, 但从图中发现有少量的团聚现象发生这也很好地解释了图 3中重复催化转化率有略微降低是因为催化剂在多次循环以后出现了微量的团聚现象.

|
图 4 循环催化后PtPd-PAAS的TEM照片 Figure 4 TEM image of PtPd-PAAS after recycling catalysis |
随后我们在最优的实验条件下进行了底物的拓展, 以此来探究催化剂对反应物的适应性, 结果如表 2所示.通过对比可以发现一卤代物, 二卤代物, 三卤代物的脱卤是由易到难的.大部分二卤代物可以通过延长反应时间令转化率达到90%以上, 然而三卤代物不止需要更长的时间, 反应温度也要求更高.因为随着卤代物中卤素原子的增加, 底物的稳定性升高, 导致催化脱卤素的难度上升.此外, 相对于溴原子, 氯的电负性更强, C-Cl键能也比C-Br更大, 分析(编号1和2; 4和5; 7和8)可知氯代物更难被活化, 反应所需要的时间相对较长.芳环上官能团的种类以及位置也是影响反应的重要因素.通过一卤代酚(编号1、2)和其他一卤代物(编号3、4、5)的对比可以发现, 一卤代酚可以在常温下很短时间内进行脱卤素, 这是由于一卤代酚相对于其他卤代物更易溶于水.此外通过对比(编号3和4)可以发现邻位脱卤素要比对位更容易, 这是由于空间位阻效应以及分子间氢键的影响.综上可知, 通过该催化反应, 几乎大部分的卤代物都可以实现在水相中加氢脱卤, 并得到相应产物.
| 表 2 PdPt/PAAS催化的卤代芳香族化合物氢化脱卤反应 Table 2 Dehalogenation of halogenated aromatic compounds catalyzed by PdPt/PAAS |
表 3是不同催化剂催化3-氯苯酚脱氯的效果对比, 不同载体负载的Pd或者Pt-Pd纳米粒子对3-氯苯酚的催化脱氯效果差异很大, Pd-TiO2催化剂在1 h的时间内底物转化率仅有20%, Pd-C催化脱氯效果较好但与PAAS负载的Pt-Pd纳米粒子相比仍有17%的差距, PAAS负载的Pt-Pd纳米粒子可以在30 min内促使底物几乎完全转化, 这是得益于金属纳米粒子的高度均匀分散性以及微小的尺寸.
| 表 3 各类催化剂对3-氯苯酚的脱氯反应的活性对比 Table 3 Comparison of catalytic activity of the PtPd/PAAS catalyst in the dechlorination of 3-chlorophenol with previously reported systems |
利用一锅法制备了准均相铂钯合金纳米粒子并用于催化脱卤反应, 由于铂钯金属的协同效应, 使得该催化剂在水相中催化卤代物脱卤的转化率高达99%, 与单金属Pt或者Pd纳米催化剂相比其反应条件更为温和, 催化活性更高.此外纳米粒子分散均匀并且其粒子直径约为4 nm, 通过调节溶液的pH可以实现催化剂的有效分离和重复利用, 这些都显著体现了铂钯二元准均相催化剂的优势.
| [1] | Zhu Qing-shi(朱清时). Green chemistry(绿色化学)[J]. Prog Chem(化学进展), 2000, 12(4): 410–414. |
| [2] | Fabini D. Quantifying the potential for lead pollution from halide perovskite photovoltaics[J]. J Phys Chem Lett, 2015, 6(18): 3546–3548. DOI:10.1021/acs.jpclett.5b01747 |
| [3] | Farkas A, Acs A, Vehovszky A, et al. Interspecies comparison of selected pollution biomarkers in dreissenid spp. inhabiting pristine and moderately polluted sites[J]. Sci Total Environ, 2017, 599: 760–770. |
| [4] | Cash D J, Serfozo P., Zinn K. Use of 82Br-radiotracer to study transmembrane halide flux:The effect of a tranquilizing drug, chlordiazepoxide on channel opening of a GABAA receptor[J]. J Memb Biol, 1995, 145(3): 257–266. |
| [5] | Hildebrand H, Mackenzie K, Kopinke F D. Pd/Fe3O4 nano-catalysts for selective dehalogenation in wastewater treatment processes-influence of water constituents[J]. Appl Catal B, 2009, 91(1/2): 389–396. |
| [6] | Huang Q, Liu W, Peng P A, et al. Reductive dechlorination of tetrachlorobisphenol A by Pd/Fe bimetallic catalysts[J]. J Hazard Mater, 2013, 262: 634–641. DOI:10.1016/j.jhazmat.2013.09.015 |
| [7] | Guasp E, Wei R. Dehalogenation of trihalomethanes in drinking water on Pd-Fe bimetallic surface[J]. J Chem Technol Biotechnol, 2003, 78(6): 654–658. DOI:10.1002/jctb.v78:6 |
| [8] | Goswami A, Rathi A K, Aparicio C, et al. In situ gene-ration of Pd-Pt core-shell nanoparticles on reduced graphene oxide (Pd@Pt/rGO) using microwaves:Applications in dehalogenation reactions and reduction of olefins[J]. ACS Appl Mater Interf, 2017, 9(3): 2815–2824. DOI:10.1021/acsami.6b13138 |
| [9] | Caixia , Matsunaga A, Tezuka M. Electroreductive dechlorination of chlorophenols with Pd catalyst supported on solid electrode[J]. J Environ Sci, 2013, 25(Suppl): S151–S154. |
| [10] | Suzuka T, Sueyoshi H, Maehara S, et al. Reactivity of aryl halides for reductive dehalogenation in (sea) water using polymer-supported terpyridine palladium catalyst[J]. Molecules, 2015, 20(6): 9906–9914. |
| [11] | Kara B Y, Yazici M, Kilbas B, et al. A practical and highly efficient reductive dehalogenation of aryl halides using heterogeneous Pd/AlO(OH) nanoparticles and sodium borohydride[J]. Tetrahedron, 2016, 72(39): 5898–5902. DOI:10.1016/j.tet.2016.08.027 |
| [12] | Cole-Hamilton D J. Homogeneous catalysis-new approaches to catalyst separation, recovery, and recycling[J]. Science, 2003, 299(5613): 1702–1706. DOI:10.1126/science.1081881 |
| [13] | Peris E, Crabtree R H. Recent homogeneous catalytic applications of chelate and pincer N-heterocyclic carbenes[J]. Coord Chem Rev, 2004, 248(21/24): 2239–2246. |
| [14] | Schorr L B. Within our reach: Breaking the cycle of disadvantage[M]. Human Rights Anchor, 1989, 16(2): 13. |
| [15] | Sheldon R A. Homogeneous and Heterogeneous Catalytic Oxidations with Peroxide Reagents[M]. Organic Peroxygen Chemistry, Springer Berlin Heidelberg, 1993, 24(33): 21-43. |
| [16] | Dong Yu-huan(董玉环), Meng Qing-zhao(孟庆朝), Wu Shu-xin(吴树新), et al. A novel bimetallic catalyst consisting two carriers for dehalogenation of aromatic halides in aqueous system(双负载双金属催化剂催化芳香卤化物水相脱卤的研究)[J]. J Mol Catal(China)(分子催化), 2009, 23(2): 125–129. |
| [17] | Dong Yu-huan(董玉环), Meng Qing-zhao(孟庆朝), Zhou Chang-shan(周长山). Preparation of PVP-PdCl2-SnCl4/MontK10-PEG400 and study on its catalyzing dehalogenation of aromatic halides in aqueous system(PVP-PdCl2-SnCl4/MontK10-PEG400的制备及催化芳香卤化物水相脱卤研究)[J]. J Mol Catal (China)(分子催化), 2003, 17(2): 124–128. |
| [18] | Zhen Xiao-li(甄小丽), Han Jian-rong(韩建荣), Kang Ru-hong(康汝洪), et al. Hydrogen transfer dehalogenation of organic halides catalyzed by PVP-MontK10 dually supported Pd-Sn catalyst in aqueous system(PVP-蒙脱土双负载Pd-Sn催化剂催化芳香卤化物水相脱卤)[J]. J Mol Catal(China)(分子催化), 2000, 14(5): 388–391. |
| [19] | Marafit M, Furimsky E. Hydroprocessing catalysts containing noble metals:deactivation, regeneration, metals reclamation, and environment and safety[J]. Energy Fuels, 2017, 31(6): 5711–5750. DOI:10.1021/acs.energyfuels.7b00471 |
| [20] | Chen Y L, Xiong L, Song X N, et al. Electrocatalytic hydrodehalogenation of atrazine in aqueous solution by Cu@Pd/Ti catalyst[J]. Chemosphere, 2015, 125: 57–63. DOI:10.1016/j.chemosphere.2015.01.052 |
| [21] |
a. Buonerba A, Cuomo C, Sanchez S O, et al. Gold nanoparticles incarcerated in nanoporous syndiotactic polystyrene matrices as new and efficient catalysts for alcohol oxidations[J]. Chem Eur J, 2012, 18(2):709-715. b. Wang Xiao-li(王晓丽),Wu Gong-de(吴功德),Liu Xian-feng(刘献锋), et al. Selective oxidation of glycerol to glyceric acid catalyzed by supported nanosized Au/Cr2O3(负载型纳米Au/Cr2O3催化甘油氧化合成甘油酸)[J]. J Mol Catal(China)(分子催化), 2017, 31(4):334-340. c. AI Sha·Nulahong(艾沙·努拉洪), Ma Ya-ya(马亚亚), Mo Wen-long(莫文龙), et al. Preparation of nano Au/TS-1 catalyst and catalytic performance for the carbonylation of methanol(纳米Au/TS-1催化剂的制备及用于甲醇羰基化体系)[J]. J Mol Catal(China)(分子催化), 2017, 31(2):121-131. d. Li Gui-xian(李贵贤), Li Qiang(李强), Zeng Xiao-liang(曾晓亮), et al. Preparation of Ru/NaY nanoparticle catalysts by microemulsion method for catalytic hydrogenation of hydroquinone(微乳法制备纳米Ru/NaY催化剂及其催化对苯二酚加氢)[J]. J Mol Catal(China)(分子催化), 2017, 31(4):316-324. |
| [22] | Martin-Martinez M, Gomez-Sainero L M, Palomar J, et al. Dechlorination of dichloromethane by hydrotreatment with bimetallic Pd-Pt/C catalyst[J]. Catal Lett, 2016, 146(12): 2614–2621. DOI:10.1007/s10562-016-1895-2 |
| [23] | Wang J P, Holt-Hindle P, MacDonald D, et al. Synthesis and electrochemical study of Pt-based nanoporous materials[J]. Electrochim Acta, 2008, 53(23): 6944–6952. DOI:10.1016/j.electacta.2008.02.028 |
| [24] | Chang F, Kim H, Lee B, et al. Pd-catalyzed dehalogenation of aromatic halides under solvent-free conditions using hydrogen balloon[J]. Bull Korean Chem Soc, 2011, 32(3): 1074–1076. DOI:10.5012/bkcs.2011.32.3.1074 |
| [25] | Nguyen Tri K, Kim S W, Yoo D-H, et al. Size-dependent work function and catalytic performance of gold nanoparticles decorated graphene oxide sheets[J]. Appl Catal A, 2014, 469(3): 159–164. |
| [26] | Luo Fa-guo(罗发国), Li Jun(李俊), Li Heng-feng(李衡峰). Green synthesis of carboxylic acid using poly(amic acid) salt-stabilized gold nanoparticles(聚酰胺酸盐稳定的金纳米催化剂用于羧酸的绿色合成)[J]. J Mol Catal(China)(分子催化), 2017, 31(1): 30–37. |
| [27] | Vayenas C G, Bebelis S, Ladas S. Dependence of catalytic rates on catalyst work function[J]. Nature, 1990, 343: 625–627. DOI:10.1038/343625a0 |
 2018, Vol. 32
2018, Vol. 32