2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
丙烯作为一种重要的基础化工原料及石油化工中间体, 可以用于生产聚丙烯、环氧丙烷、丁醇、苯酚、丙二醇、丙酮、丙烯酸、丙烯腈、辛醇以及异丙醇等.近年来, 北美页岩气革命对传统炼化乙烯产业造成巨大冲击的同时也促使了丙烷脱氢(PDH)产业的快速发展.目前, 国内已有十几套丙烷脱氢工业装置投产运行, 未来还将有数十套装置投建. PtSn/Al2O3是PDH最主要的催化剂, 但其在PDH的高温及还原气氛条件下, 易发生Pt烧结和裂解积炭, 导致催化剂快速失活, 催化剂需要频繁再生.因此, 如何提高催化剂稳定性是应用中的关键问题.
金属掺杂是提高催化剂稳定性的重要途径.例如掺杂Zn[1-2]与Sn[3]通过几何效应(减少Pt纳米粒子的密度)和电子效应(改变Pt的电子性质)来抑制脱氢过程中副反应的发生, 如焦炭的形成和异构化过程等.加入Ga[4-5]或In[6]一方面通过与Pt形成合金产生几何与电子效应来减少催化剂上积炭的沉积, 另一方面可以通过毒化催化剂表面的B酸位点来减少副反应的发生.
载体性质同样是影响催化剂稳定性的重要因素.氧化铝具有比表面积大、孔容孔径大、机械强度高等特性, 是PDH体系最常用的载体. Kwak等[7-9]通过核磁研究发现氧化铝表面配位不饱和的五配位铝是活性组分Pt簇团/颗粒的锚定位点, 合成富含五配位铝的载体可提高Pt的分散度和催化剂稳定性.例如Shi等[9]和Eun等[10]分别采用水热法合成了富含五配位铝的片状和纤维状氧化铝, 作为催化丙烷脱氢的载体, 提高了Pt的分散度, 改善了催化性能.或者通过在载体中掺入碱金属(Li, Na, K), 碱土金属(Mg, Ca)以及稀土金属(La, Ce)来改善载体性质[10-11], 例如Yu等[12]在Al2O3中掺入Ce, 作为催化丙烷脱氢的载体, 通过加强金属-载体相互作用使得催化剂稳定性提高.然而如何从载体出发进一步提高催化剂的稳定性仍然有待探索.
采用蒸发自组装法制备了不同硼铝比的铝硼复合氧化物载体, 真空配合浸渍法合成了Pt-Sn负载型催化剂, 并与同样方法制备的PtSn/Al2O3催化剂进行比较, 考察了其在丙烷脱氢制丙烯中的催化活性.采用N2物理吸附、SEM、X射线粉末衍射、H2-TPR、NH3-TPD、TG、TEM及ICP-OES对典型载体及催化剂进行表征.
1 实验部分 1.1 催化剂制备采用蒸发自组装法制备铝硼复合氧化物载体[14-17].将1.00 g P123(EO20PO70EO20, M=5800, Aldrich)溶解于20 mL无水乙醇中, 得到溶液A, 搅拌中加入1.6 mL硝酸(65%~68%(重量百分数)), 混合后加入2.04 g异丙醇铝(重量百分数≥98%, aladdin), 定量硼酸(重量百分数≥99.5%, 天津大茂化学试剂厂), 10%(重量百分数)丙三醇(重量百分数≥99%, 天津博迪化工股份有限公司), 搅拌至异丙醇铝完全溶解.放入60 ℃烘箱中静置蒸发48 h, 得淡黄色固体.将该淡黄色固体从室温缓慢升温至400 ℃(升温速率为1 ℃/min), 恒温4 h后, 再升温至600 ℃(升温速率为1 ℃/min), 焙烧4 h, 得到铝硼复合氧化物载体.作为对比, 试验合成了不添加硼的纯氧化铝载体, 其合成方法与铝硼复合氧化物载体合成方法基本一致, 区别在于不添加硼酸和丙三醇.上述载体记为(AlBx)2O3(简写为ABx)(其中x代表复合氧化物中硼和铝元素的摩尔比).
催化剂采用真空配合浸渍制备.将上述载体研磨筛分至粒径0.900~0.450 mm, 经过30 min真空预处理后, 均匀浸渍于理论量的氯铂酸和氯化亚锡乙醇配合液中, 之后于60~70 ℃真空干燥, 然后转移至烘箱中120 ℃烘干, 再转移至马弗炉中520 ℃焙烧4 h, 制得所需的丙烷脱氢制丙烯催化剂, 催化剂的理论负载量为Pt: 0.5%(重量百分数), Sn: 1.5%(重量百分数), 将催化剂记为Cat-ABx.
1.2 催化剂表征N2物理吸附:采用美国康塔仪器公司的NOVAe型全自动比表面和孔隙度分析仪, 所有样品预先在300 ℃高真空预处理5 h, 在液氮温度(-196 ℃)下, 测得N2吸附-脱附等温线.采用BET(Brunauer-Emmett-Teller)法计算样品的比表面积, 相对压力为0.0~1.0, 采用等温线的脱附支, 利用了BJH(Barrett-Joiner-Halenda)孔径模型计算样品的孔径分布, 总孔容采用吸附脱附最高点处的单点吸附容量.
SEM:采用JSM6360LV扫描电子显微镜, 性能指标为:加速电压为0.5~30 kV, 放大倍数为15~50 000倍, 分辨率:高真空3.0 nm, 低真空4.5 nm, 样品制备具体步骤为:研磨后粘牢在样品座导电胶上, 用洗耳球吹干净后进行抽真空, 喷金1~1.5 min后观察.
XRD:采用PanalyticalX’per PRO型的粉末衍射仪测定, 管电压为40 kV, 管电流为40 mA, 扫描的角度范围为10°~90°.
H2-TPR:采用浙江泛泰公司FINESORB-3010型的化学吸附仪测定, 称取0.05 g预先已经120 ℃烘干的样品置于U型石英反应管中.样品预先在300 ℃的Ar气(99.99%, 30 mL·min-1)中预先处理2 h, 冷却至室温后, 切换至10%H2-Ar, 以10 ℃/min的升温速率升温至600 ℃, 保持30 min, 升温过程中H2消耗量由TCD检测器进行测定.
NH3-TPD:采用浙江泛泰公司FINESORB-3010型的化学吸附仪测定, 称取0.05 g预先已经120 ℃烘干的样品置于U型石英反应管中, 在Ar气(99.99%, 30 mL·min-1)中于600 ℃预处理1 h后, 在100 ℃吸附NH3(15%NH3-Ar)达到饱和.随后, 以10 ℃ /min的速率升温至600 ℃, 通过TCD检测NH3的解吸.
TG:反应后催化剂上的积炭量采用WRT-1D型热重分析仪测定, 在50 mL/min的空气流中以3 ℃/min的速率升温至800 ℃进行测定.
TEM:采用FEI公司的Tecnai G2 F30 S-Twin型高分辨场发射透射电镜对催化剂中金属离子的分布及形貌进行观测.工作电压为300 kV.测试样品首先用玛瑙研钵研磨后, 分散于乙醇溶液中, 超声处理后, 用滴管吸取适量溶液滴于铜网上, 静置干燥后, 分析测试.
ICP-OES:反应前后催化剂中的硼溶出量使用PerkinElmer公司的ICP-OES 7300DV型电感耦合等离子体发射光谱仪测定, 测试表征前, 使用3%体积分数的稀盐酸作为背景.
1.3 催化剂性能评价反应温度为600 ℃, 反应压力为常压, 催化剂的装填量为0.15 g, 丙烷的重时空速为6 h-1, 氢烃摩尔比为0.5:1.反应的气相产物用气相色谱Agilent 7890(HP-Al2O3/KCl毛细管填充柱, FID检测器)在线分析.
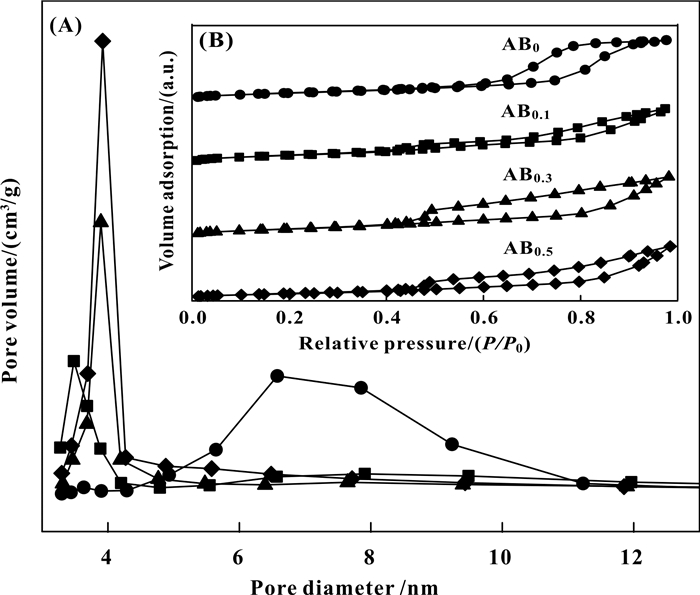
2 结果及讨论 2.1 载体N2物理吸附表征图 1为4种不同载体的N2吸附-脱附等温线及孔径分布.由图可知, 所有载体均表现出典型的Ⅳ型吸附等温线, AB0滞后回环呈H1型, ABx(x≠0)的滞后回环呈H4型, 这说明了所有样品均具有介孔结构, 且孔径分布较窄, ABx(x≠0)含有部分狭窄的裂隙孔[13].载体的织构性质见表 1, 由表 1可知, 铝硼复合氧化物的比表面积、总孔容、孔径均比氧化铝小, 且随着B含量的增加逐渐减小, 这可能是由于掺入B后形成铝硼复合氧化物, 引起了晶粒尺寸变小以及晶粒缺陷变少.
|
图 1 4种不同载体的孔径分布及N2吸附-脱附等温线 Fig.1 Pore distribution and N2 adsorption-desorption isotherms (insets) of four different supports |
| 表 1 4种不同载体的织构性质 Table 1 Textural properties of four different supports |
通过SEM进一步观察催化剂的表面结构, 结果如图 2所示. Cat-AB0的载体主要由细小(<1 μm)且表面粗糙的颗粒堆积而成, 因此缺陷位多, 表面积大;而Cat-ABx(x≠0)的载体则主要由颗粒尺寸较大(>1 μm)且表面相对光滑的颗粒堆积而成, 缺陷位少, 故而比表面积小, 这与N2物理吸附结果吻合.

|
图 2 不同催化剂样品的SEM图 Fig.2 SEM images of different catalyst samples (a) Cat-AB0; (b) Cat-AB0.1; (c) Cat-AB0.3; (d) Cat-AB0.5 |
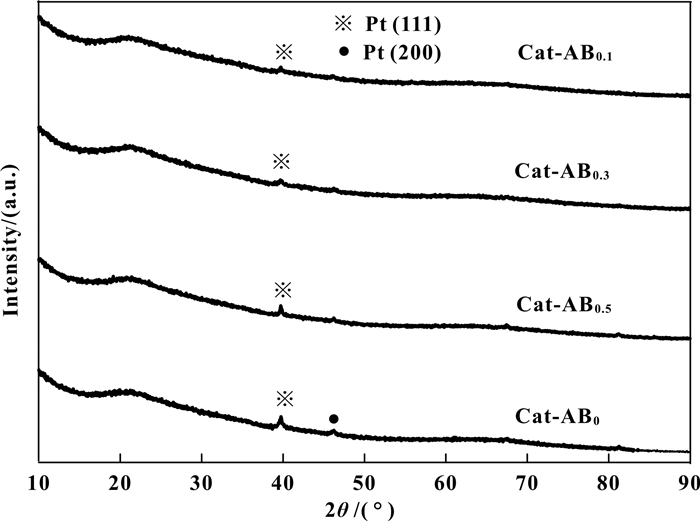
采用XRD进一步对催化剂结构进行表征, 结果如图 3所示.所有衍射图谱中均未显示γ-Al2O3、B2O3或铝硼酸盐的特征衍射峰[14], 说明载体均为无定型结构.所有谱图中均能在2θ=40°和47°附近观察到弱的Pt的(111)和(200)晶面的特征衍射峰[15].其中, Cat-AB0上Pt的衍射峰相对较强, 说明Pt晶粒较大, 分散度低.当载体中掺入少量B后, Cat-AB0.1的Pt特征衍射峰强度大幅减弱, 说明Pt在A0.9B0.1上的分散度较高.由于AB0.1具有比AB0更低的比表面积, 说明了硼有提高活性组分Pt分散度的作用.然而, 随着B掺入量的进一步提高, Cat-AB0.3和Cat-AB0.5上Pt的衍射峰逐渐增强, 说明其分散度降低, 但仍高于Cat-AB0.此时, Pt分散度的降低可能是由载体比表面积降低所导致的.
|
图 3 不同催化剂样品的XRD图谱 Fig.3 XRD patterns of different catalyst samples |
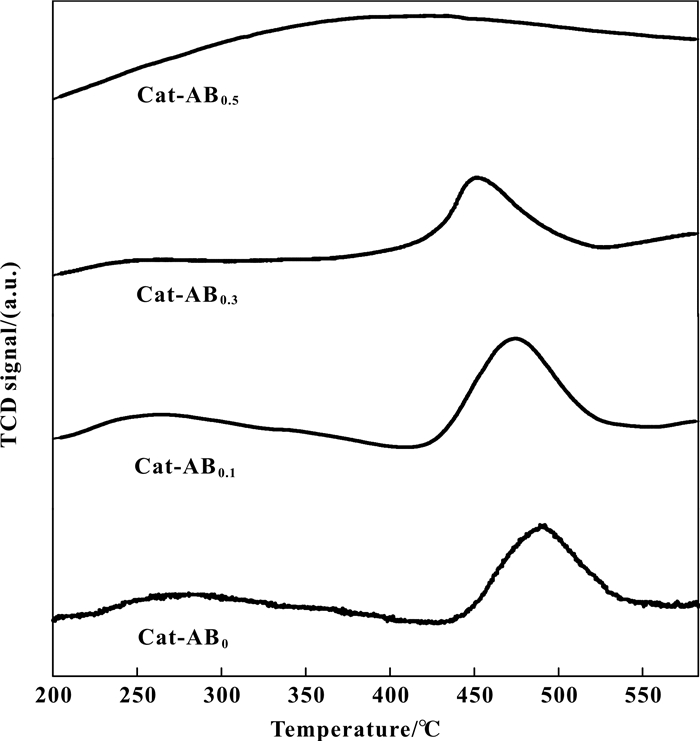
为研究催化剂活性组分的还原性质, 对催化剂进行H2-TPR分析.由图 4可知, Cat-AB0、Cat-AB0.1以及Cat-AB0.3在~270 ℃(峰Ⅰ)和~480 ℃(峰Ⅱ)左右出现还原峰. ~270 ℃的还原峰可以归属为Pt氧化物的还原[16], 而在~480 ℃的还原峰可以归属为SnⅣ到SnⅡ的还原[17].可以看出Cat-ABx(x≠0)相较于Cat-AB0, Sn的还原峰明显向低温迁移, 这可能是由于载体中掺入B会导致载体与Sn之间相互作用减弱, 使SnⅣ更容易被还原成SnⅡ, SnⅡ可以将更多电子转移到铂原子的5d轨道.其中, Cat-AB0.5的H2-TPR在300~500 ℃形成的宽泛的还原峰, 可能是由于SnⅣ/Ⅱ的还原峰继续向低温方向迁移, 并与Pt的还原峰发生了重叠.
|
图 4 不同催化剂样品的H2-TPR曲线 Fig.4 H2-TPR curves of the different catalyst samples |
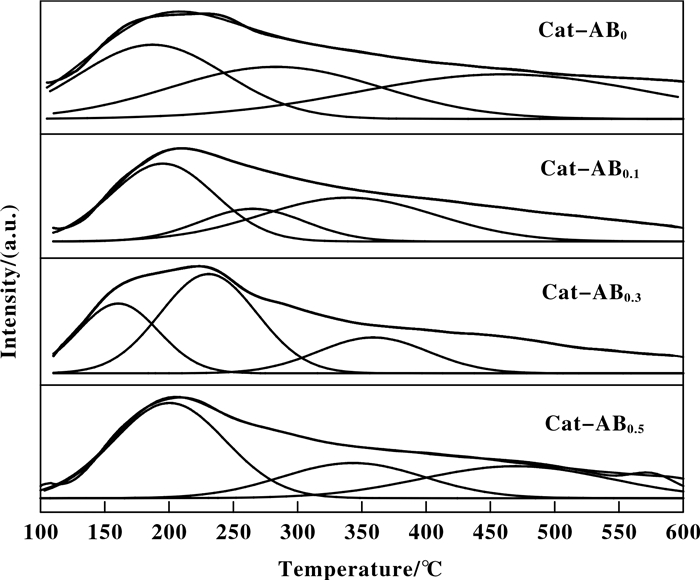
催化剂的酸性会显著影响催化剂的脱氢性能, 所以通过NH3-TPD来测定4种催化剂的酸性, 具体结果如图 5所示.采用高斯去卷积法对NH3-TPD曲线进行半定量分析, 结果如表 2所示, 所有样品曲线均可以拟合出3个峰. 170~280 ℃(峰Ⅰ), 340~380 ℃(峰Ⅱ)和460 ℃(峰Ⅲ)左右的峰应分别归属于弱酸位, 中强酸位和强酸位[18].由NH3-TPD曲线的总脱附面积可知4种催化剂的总酸量顺序如下: Cat-AB0.1>Cat-AB0.3>Cat-AB0.5>Cat-AB0.说明B掺入均可增加载体的总酸量, 其中Cat-AB0.1的总酸量是Cat-AB0的2.45倍.同时, 掺入B后可使载体的酸强度均明显变弱.掺入10%~30%的B后, Cat-AB0上原有的强酸性中心消失, Cat-AB0.1和Cat-AB0.3上只存在弱酸和中强酸性中心. Cat-AB0.3的酸强度达到最低, 其弱酸中心的NH3脱附温度低至160.5 ℃.而进一步增加B含量(Cat-AB0.5)时, 酸强度增加, 甚至高于Cat-AB0.此外, 随着B掺入量的增加, 总酸量逐渐减少, 但酸中心密度(Total acidity/SBET)逐渐增加, Cat-AB0.5的酸中心密度为Cat-AB0的4.3倍, 说明B的加入可提高载体表面酸密度, 而总酸量减少主要是由于比表面积下降.
|
图 5 4种不同催化剂的NH3-TPD曲线 Fig.5 NH3-TPD curves of the four different catalysts |
| 表 2 NH3-TPD曲线的半定量分析数据 Table 2 The semi-quantitative analysis data of NH3-TPD profiles |
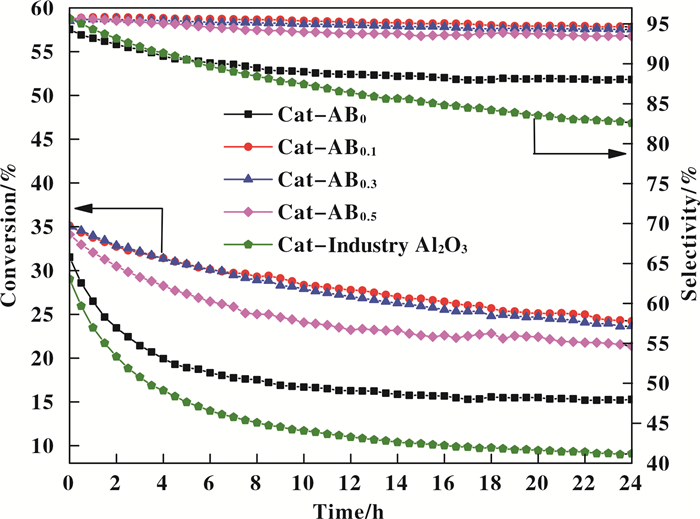
为考察PtSn/ABx催化剂的丙烷脱氢性能, 在相同实验条件下对催化剂进行反应评价, 结果如图 6.由图可知, Cat-ABx(x≠0)催化剂上的丙烯选择性均较高, 且差异不大(≈95%), 并远高于Cat-AB0.结合H2-TPR结果, Cat-ABx(x≠0)催化剂上Pt原子的电子密度大, 利于丙烯产物的脱附, 从而提高了Cat-ABx(x≠0)的丙烯选择性.铝硼复合氧化物负载的Cat-ABx(x≠0)的催化活性均远优于纯氧化铝负载的Cat-AB0, 且其催化活性规律如下: Cat-AB0.1>Cat-AB0.3>Cat-AB0.5>Cat-AB0. Cat-AB0.1催化剂的脱氢活性最好, 这与催化剂上Pt分散度规律和总酸量规律一致.此外, 铝硼复合氧化物负载的Cat-ABx(x≠0)的催化稳定性也远优于纯氧化铝负载的Cat-AB0, 且同样满足规律: Cat-AB0.1>Cat-AB0.3>Cat-AB0.5>Cat-AB0.反应前5 h内, Cat-AB0转化率由31.5%快速降至18.9%;而Cat-AB0.1和Cat-AB0.3则活性下降较为缓慢, 反应24 h后, 活性才分别从35.1%和35.1%降至24.2%和23.7%.为进一步确认B掺杂的影响, 我们对比了以PDH工业氧化铝(纯氧化铝, SBET=105 m2·g-1, Vtotal=0.72 cm3·g-1)为载体, 在完全相同的催化剂制备和反应评价条件下的催化性能(图 6, Cat-工业Al2O3). Cat-工业Al2O3催化剂虽具有比Cat-AB0更低的活性和选择性, 但与后者具有相似的快速失活趋势.由此可知, B掺杂的确可大幅提高催化剂的活性、稳定性及选择性.
|
图 6 不同催化剂样品上丙烷脱氢制丙烯的评价结果 Fig.6 Propane dehydrogenation to propene over different catalysts (Reaction condition: feed gas H2:C3H8=0.5:1, T=600 ℃, WHSV=6 h-1) |
由文献可知, 积炭和Pt聚集是导致催化剂快速失活的两个主要原因, 积炭主要发生在强酸中心[19-20].其中, Cat-AB0.1和Cat-AB0.3上同时具有相对较弱的酸中心(只有弱酸和中强酸)和高的Pt分散度, 均可抑制裂解和积炭等副反应, 对脱氢反应有利.但具有更强酸中心的Cat-AB0.5的稳定性仍然优于Cat-AB0, 说明积炭可能不是导致催化剂Cat-AB0快速失活的主要原因.
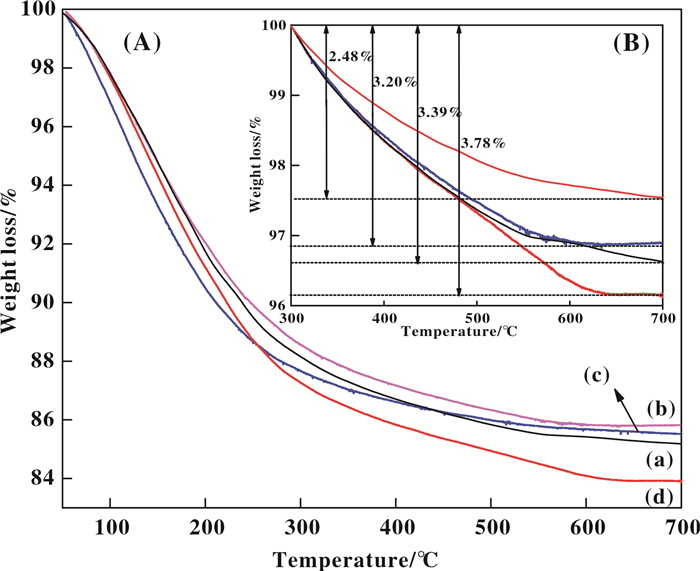
2.7 热重分析为进一步验证上述猜测, 采用热重分析了反应24 h后各催化剂上的积炭量, 结果如图 7所示. 图 7A中150 ℃以下的失重一般归因于水和低沸点有机物的脱附, 150~300 ℃的失重归因于焦油和分子量较大的副产物的分解, 300 ℃以上的失重是由于催化剂上焦炭的燃烧引起的[13].由图 7A, 7B均可以看出, 反应24 h后, 4个催化剂的总失重和300 ℃以上的烧炭失重顺序均为Cat-AB0.1<Cat-AB0.3<Cat-AB0<Cat-AB0.5, 这与催化剂上的酸强度规律完全一致, 说明酸强度是影响积炭的主要因素.此外, 虽然Cat-AB0.5具有比Cat-AB0更高的积炭量和更低的比表面积, 但却有大大优于Cat-AB0的催化稳定性, 说明导致Cat-AB0快速失活的主要因素并非积炭, 而是Pt的聚集.由于B掺入对Pt的分散具有稳定作用, 所以可以抑制反应过程中Pt的聚集, 从而提高催化剂稳定性.
|
图 7 7反应24 h后4种不同催化剂的TG曲线 Fig.7 TG curves of the four different catalysts after 24 h reaction (a) Cat-AB0; (b) Cat-AB0.1; (c) Cat-AB0.3; (d) Cat-AB0.5 |
为进一步明确反应前后Pt颗粒的尺寸变化, 采用TEM分析了Cat-AB0、Cat-AB0.1和Cat-AB0.5反应前后的3个样品, 结果如图 8所示.新鲜Cat-AB0、Cat-AB0.1和表面较均匀分布着2~3 nm左右的金属颗粒, Cat-AB0.5表面也有可见的2~3 nm左右的金属颗粒.反应后的催化剂表面金属颗粒数目明显变少, 且颗粒尺寸没有明显增大, 说明B对Pt的分散具有稳定作用.

|
图 8 反应前后3种催化剂的TEM图 Fig.8 TEM images of (a, b) fresh and deactivated Cat-AB0, (c, d) fresh and deactivated Cat-AB0.1, (e, f)fresh and deactivated Cat-AB0.5 |
由于B不仅可大幅增加载体的总酸量和酸中心密度, 降低酸强度, 而且对Pt的分散具有稳定作用, 从而抑制反应过程中Pt的聚集, 提高了催化剂稳定性.为明确催化剂中的B在反应后是否有流失, 采用ICP-OES分析了Cat-AB0.1和Cat-AB0.5两个样品反应前后的硼含量, 两催化剂反应前后的硼含量如表 3所示.由表可知反应前后催化剂中的硼含量变化很小, 说明催化剂中的B在反应过程中未流失.
| 表 3 两催化剂反应前后的硼含量 Table 3 The boron content before and after the reaction of the two catalysts |
采用蒸发自组装法制备了铝硼复合氧化物载体, 并采用真空络合浸渍法合成了Pt-Sn催化剂, 将其应用于丙烷脱氢反应中.铝硼复合氧化物载体对Pt的分散性能优于纯氧化铝, 使得Cat-ABx(x≠0)具有远优于Cat-AB0的催化丙烷脱氢反应活性和稳定性.此外, B的掺入可大幅提高载体的表面总酸量和酸中心密度, 随着B掺入量的增加, 表面总酸量逐渐减少, 酸中心密度增加.其中, B掺入量为Al的10%的铝硼复合氧化物所负载的Cat-AB0.1催化剂具有最优的丙烷脱氢性能.
| [1] |
Yu Chang-lin(余长林), Xu Heng-yong(徐恒泳), Ge Qing-jie(葛庆杰), et al. Effect of Zn on Sn activity and propane dehydrogenation in Pt-Sn / gamma-Al2O3 catalyst(Zn对Pt-Sn/-γ-Al2O3催化剂中Sn的活性状态及丙烷脱氢反应的影响)[J]. Chem J Chin Univer(高等学校化学学报), 2006, 13(8): 1492–1495.
DOI:10.3321/j.issn:0251-0790.2006.08.017 |
| [2] |
Zhang Y, Zhou Y, Huang L, et al. Structure and catalytic properties of the Zn-modified ZSM-5 supported platinum catalyst for propane dehydrogenation[J]. Chem Eng J, 2015, 270: 352–361.
DOI:10.1016/j.cej.2015.01.008 |
| [3] |
Lieske H, Sarkany A, Volter J. Hydrocarbon adsorption and coke formation on Pt/Al2O3 and Pt-Sn/Al2O3 catalysts[J]. Catal A-gen, 1987, 30(1): 69–80.
DOI:10.1016/S0166-9834(00)81012-X |
| [4] |
Liu X, Zhou Y, Zhang Y, et al. Effect of Ga addition on catalytic performance of PtSnNa/ZSM-5 catalyst for propane dehydrogenation[J]. Chin Pet Proce Pe, 2011, 13(4): 45–52.
|
| [5] |
Sattler J J H B, Gonzalez-Jimenez I D, Luo L, et al. Platinum-promoted Ga/Al2O3 as highly active, selective, and stable catalyst for the dehydrogenation of Propane[J]. Angew Chem Int Edit, 2014, 53(35): 9251–9256.
DOI:10.1002/anie.201404460 |
| [6] |
Sun P, Siddiqi G, Vining W C, et al. Novel Pt/Mg(In)(Al)O catalysts for ethane and propane dehydrogenation[J]. J Catal, 2011, 282(1): 165–174.
DOI:10.1016/j.jcat.2011.06.008 |
| [7] |
Kwak J H, Hu J, Mei D, et al. Coordinatively unsaturated Al3+ centers as binding sites for active catalyst phases of platinum on gamma-Al2O3[J]. Science, 2009, 325(5948): 1670–1673.
DOI:10.1126/science.1176745 |
| [8] |
Mei D, Kwak J H, Hu J, et al. Unique role of anchoring penta-coordinated Al3+ sites in the sintering of γ-Al2O3-supported Pt catalysts[J]. J Phys Chem Lett, 2010, 1(18): 2688–2691.
DOI:10.1021/jz101073p |
| [9] |
Shi L, Deng G M, Li W C, et al. Al2O3 nanosheets rich in pentacoordinate Al(3+) ions stabilize Pt-Sn clusters for propane dehydrogenation[J]. Angew Chem Inter Edit, 2015, 54(47): 13994–13998.
DOI:10.1002/anie.201507119 |
| [10] |
Jang E J, Lee J, Jeong H Y, et al. Controlling the acid-base properties of alumina for stable PtSn-based propane dehydrogenation catalysts[J]. Appl Catal A gen, 2019, 572: 1–8.
DOI:10.1016/j.apcata.2018.12.024 |
| [11] |
Zhang Qiao(张巧), Zhang Ke-ting(张客厅), Wang Cheng-guang(王晨光), et al. Study on dehydrogenation of propane by magnesium aluminum hydrotalcite supported by PtSn(负载PtSn金属助剂的镁铝水滑石上的丙烷脱氢反应研究)[J]. J Mol Catal(Chin)(分子催化), 2018, 32(4): 359–369.
|
| [12] |
Yu C, Ge Q, Xu H, et al. Effects of Ce addition on the Pt-Sn/gamma-Al2O3 catalyst for propane dehydrogenation to propylene[J]. Appl Catal A gen, 2006, 315: 58–67.
DOI:10.1016/j.apcata.2006.08.038 |
| [13] |
Shi Y, Li X, Rong X, et al. Influence of support on the catalytic properties of Pt-Sn-K/theta- Al2O3 for propane dehydrogenation[J]. RSC Adv, 2017, 7(32): 19841–19848.
DOI:10.1039/C7RA02141K |
| [14] |
Tang N, Cong Y, Shang Q, et al. Coordinatively unsaturated Al3+ sites anchored subnanometric ruthenium catalyst for hydrogenation of aromatics[J]. ACS Catal, 2017, 7(9): 5987–5991.
DOI:10.1021/acscatal.7b01816 |
| [15] |
张强.铂基复合催化剂的制备及电催化性能研究[D].苏州大学硕士论文, 2014.
Zhang Qiang. Preparation and electrocatalytic performance of platinum - based composite catalyst [D]. Master's thesis of suzhou university, 2014.
http://cdmd.cnki.com.cn/Article/CDMD-10285-1014267165.htm |
| [16] |
Carvalho L S, Pieck C L, Rangel M C, et al. Trimetallic naphtha reforming catalysts. I. Properties of the metal function and influence of the order of addition of the metal precursors on Pt-Re-Sn/gamma- Al2O3-Cl[J]. Appl Catal A gen, 2004, 269(1/2): 91–103.
|
| [17] |
Zhang Y, Zhou Y, Liu H, et al. Effect of La addition on catalytic performance of PtSnNa/ZSM-5 catalyst for propane dehydrogenation[J]. Appl Catal A gen, 2007, 333(2): 202–210.
DOI:10.1016/j.apcata.2007.07.049 |
| [18] |
Iengo P, Di Serio M, Solinas V, et al. Preparation and properties of new acid catalysts obtained by grafting alkoxides and derivatives on the most common supports. Part Ⅱ: Grafting zirconium and silicon alkoxides on gamma-alumina[J]. Appl Catal A gen, 1998, 170(2): 225–244.
DOI:10.1016/S0926-860X(98)00042-8 |
| [19] |
Li Q, Sui Z, Zhou X, et al. Coke formation on Pt-Sn/Al2O3 catalyst in propane dehydrogenation: coke characterization and kinetic study[J]. Top Catal, 2011, 54(13/15): 888–896.
|
| [20] |
何松波.长链烷烃(C10-C19)脱氢催化剂及积炭行为的研究[D].中国科学院大连化学物理研究所博士论文, 2009.
He Song-bo. Study on dehydrogenation catalyst and carbonation behavior of long chain alkane (C10-C19)[D]. Doctoral dissertation of dalian institute of chemical physics, 2009.
http://www.irgrid.ac.cn/handle/1471x/222561 |
 2019, Vol. 33
2019, Vol. 33


