2. 中国科学院兰州化学物理研究所 羰基合成与选择氧化国家重点实验室, 甘肃 兰州 730000;
3. 滨州学院 学报编辑部, 山东 滨州 256603
2. The State Key Laboratory of Oxo Synthesis and Selective Oxidation, Lanzhou Institute of Chemical Physics, Chinese Academy of Sciences, Lanzhou 730000, China;
3. Editorial Department of Journal, Binzhou University, 256603, China
低碳烯烃(C2~C4烯烃)是重要的化工原料, 可以用来生成聚乙烯、聚丙烯或者乙二醇等众多有机化合物, 是衡量一个国家化工行业发展水平的重要指标.目前, 低碳烯烃大部分来源于传统石油的蒸汽裂解, 但是石油短期内不可再生性使得低碳烯烃的生产迟早面临严峻的挑战[1].因此, 合成气(CO+H2)间接或直接的制备低碳烯烃受到了极大的关注.合成气制备低碳烯烃主要有以下3种工艺路线[2]: (1)合成气经由甲醇裂解或二甲醚制取低碳烯烃; (2)合成气经由氧化物-分子筛双功能催化剂制备低碳烯烃; (3)合成气经由费托合成过程(FTS)直接制备低碳烯烃(FTO).路线(1)是间接制备低碳烯烃, 间接法制备低碳烯烃选择性较高且工业应用已日趋成熟, 但分步反应需要的反应器、催化剂及能耗较多; 路线(2)反应需分两步, 两步反应需要的温度不同, 升高温度虽能提高C—C耦合过程效率但会导致CO活化效率降低; 合成气通过费托反应直接制取低碳烯烃符合绿色化学的低碳烯烃制备方法, 具有更大的经济效益, 因此由合成气经由费托合成过程直接制备低碳烯烃一直备受关注.
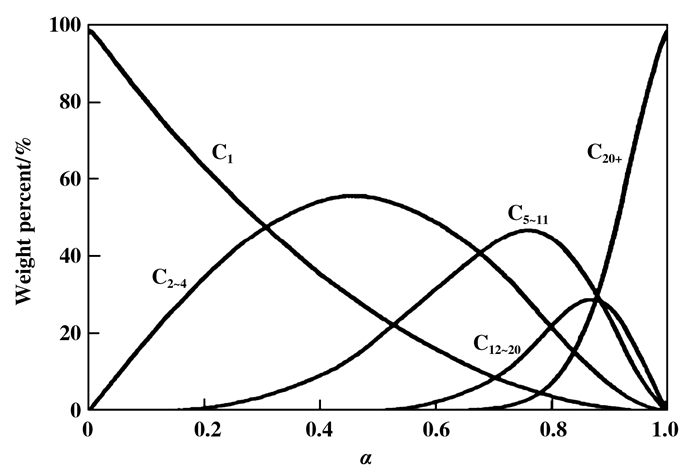
费托合成的原料只有CO还H2, 但其反应产物却极为复杂, 除了烃类化合物之外, 还有H2O、CO2以及醇醛酮类等.费托合成反应的机理虽已研究多年, 但尚未完全阐明, 其中碳化机理是被国内外学者普遍接受的.根据这一机理, 产物分布遵循Anderson-Schulz-Flory(ASF)分布[3], 如图 1所示.
|
图 1 Anderson-Schulz-Flory(ASF)产品分布预测图 Fig.1 Anderson-Schulz-Flory (ASF) model for the prediction of product distribution |
碳链增长因子α值决定了费托合成产物中烃类的碳数分布, 由图 1可知, 当链增长因子在0.4~0.5之间时, C2~C4烯烃的选择性达到最大值.工艺条件、催化剂类型以及化学助剂的加入都可影响α的数值.因此, 调节催化剂的链增长能力, 减少甲烷生成以及选择性地合成低碳烯烃是研究热点.催化剂的主体活性组分决定了产物的分布, 可用于FTO反应的催化剂的活性组分有Fe、Co、Ni、Ru、Rh等.其中, 只有Fe、Co具有实际应用性, 研究也较多.我们主要围绕Fe、Co催化剂在CO加氢直接制备低碳烯烃反应中的研究展开综述, 评述该反应中催化剂方面研究所取得的进展.
1 Fe基催化剂对于CO加氢制备低碳烯烃的反应, Fe是一种较为理想的活性金属组分. Fe价格低, 具有较高水煤气变换反应活性, 在高温下铁基催化剂表现出较高低碳烯烃选择性和较低CH4选择性.影响Fe基催化剂生成低碳烯烃的因素有很多, 活性金属的分散度、活性相、粒径、载体、助剂等都可直接影响催化剂的活性和低碳烯烃的选择性.
1.1 Fe基催化剂活性组分Fe基催化剂在反应过程中活性相转化十分复杂.一般而言, Fe基催化剂初始大都以Fe2O3形式存在, 然而在合成气反应过程中, Fe基催化剂存在Fe0、Fe2O3、Fe3O4、FeO以及ε-Fe2C、ε′-Fe2.2C、χ-Fe5C2、θ-Fe3C、Fe7C3等众多物相[4-7], 且各种碳化铁物种在反应过程中会发生转变, 碳化铁也可以被反应中生成的H2O重新氧化为Fe3O4.这使得催化剂表征和反应过程分析变得十分复杂, 活性相难以确定.
研究发现, Fe2.2C和Fe2C的生成温度<250 ℃, 而在250~350 ℃则更易生成Fe5C2, Fe3C的生成则需要高于350 ℃, Fe7C3生成的条件更为苛刻, 只在SiO2担载的催化剂中有少许发现[7]. DE SMIT等[8]运用原位表征手段(XAFS、XRD和RS等), 结合DFT计算, 发现碳化铁的生成不但与还原条件和温度有关, 还与化学势μc有关, 其研究结果如图 2所示. FTS常采用的反应温度在240~360 ℃, 这是生成Fe5C2理想条件, 因此在众多碳化物中, Fe5C2被普遍认为是FTS反应过程中的主要活性相, 也是低碳烯烃生成的活性相[7]. 表 1列出了几种不同碳化物催化剂反应性能, 可以看出Fe2C、Fe3C以及Fe5C2都具有CO加氢反应活性, 同时具有一定的C2~C4烯烃生成能力, 真正起催化作用以及对生成低碳烯烃有利的活性物质仍存在争议.

|
图 2 碳化铁结构原子热力学研究定性解释物相转变[8] Fig.2 Qualitative interpretation of the ab initio atomistic thermo dynamics study of the iron carbide structures |
| 表 1 不同碳化铁催化剂反应性能 Table 1 Reaction performance of different iron carbide catalysts |
活性金属前驱体影响催化剂的CO加氢活性及低碳烯烃选择性, 研究表明羰基金属制备的催化剂具有更好的催化性能. Basset等[9]以Fe4(CO)13H2为前驱体制备了Fe/α-Al2O3催化剂, 在0.9 MPa, 290 ℃, 和H2/CO= 0.9反应条件下发现C2~C4烯烃的选择性高达49%, 但催化剂活性较差.兰化所胡斌课题组[10]分别以Fe(CO)5与Fe(NO3)3为前驱体制备了Fe-K-Mn/MgO催化剂, 发现与硝酸铁相比, Fe(CO)5制备的催化剂具有更高低碳烯烃选择性(55.9%). Commereus等[11]将Fe(CO)5和Fe3(CO)12分别负载于SiO2、MgO等载体, 催化剂在反应90 h后C2~C5烯烃的选择性仍达到40%以上.羰基铁为活性金属前驱体制备催化剂促进了Fe粒子的分散, 同时制备过程中Fe0的存在形式改变了活性金属与载体之间强的相互作用, 使得两者在充分接触的同时又避免了金属化合物的生成, 因此增强了催化剂的活性和促进了低碳烯烃的生成.但在反应过程中, 铁纳米粒子逐渐聚合降低了烯烃的选择性, 另外羰基金属价格昂贵, 也限制了其进一步应用.
1.3 助剂单纯使用Fe作为活性金属制备催化剂不仅降低了催化剂的稳定性和活性, 同时也达不到低碳烯烃的选择性要求, 因此助剂的添加是催化设计研究中重要的一步.在CO加氢制备低碳烯烃的研究中, 碱金属和Mn是较常用的助剂.
碱金属一般都是电子给予体, 它们的加入可以增加催化剂表面的电子密度, 导致CO化学吸附增强和解离速率增快, 抑制了H2的吸附和烯烃的二次吸附, 碱性越强对烯烃的吸附再加氢抑制作用越强[12]; 在产物上表现为抑制甲烷的生成, 增加烯烃和高碳链产物的选择性, 但是随着碱金属离子半径的增大, 会一定程度上覆盖活性金属, 进而影响其活性[13].
碱性助剂对产物选择性和催化活性的影响与助剂的浓度、制备方法、反应条件密切相关.而K在CO加氢制备低碳烯烃中是最常用的碱金属. Cheng等[14]以还原后的石墨烯(rGO)为载体, 考察了0~2%含量K对Fe基催化剂的影响, 在340 ℃、2 MPa、H2/CO = 1反应条件下, 1%K的催化剂长时间反应的稳定最好; 2%K的催化剂烯烃选择性达到了68%. Kang等[15]分别使用共沉淀法和溶胶凝胶法制备了Fe-Cu-Al-K催化剂, 发现在300 ℃, 1 MPa、H2/CO=2的条件下, 溶胶凝胶法制备的催化剂具有很高的CO转化率(96%), 更高的C2~C4产物选择性(21%), 其中烯烃的选择性为(11%).尽管K作为助剂有利于低碳烯烃的生成, 但过量的K使得Fe在反应过程中发生烧结聚集, CO转化率大大降低.
在CO加氢制备低碳烯烃中, Mn是一种常用的助剂.研究表明, Mn的加入不仅可以增加CO转化率, 降低CH4的选择性, 还能增加C2~C4烯烃及C5+的选择性.研究表明适量Mn的加入一是可抑制反应过程中碳化铁的氧化, 阻止水汽反应的进一步发生; 二是可以提高催化剂表面的碱性, 阻止了烯烃的二次吸附和加氢, 提高了低碳烯烃和C5+产物的选择性.但是Mn的作用机理一直不够明确, 有研究表明Mn在一定制备方法下还可以影响Fe基催化剂中碳化铁的生成种类. Liu等[16]制备了Fe3O4微米球, 并用MnOx修饰其表面, Mn的加入增加了Fe3O4向Fe3C的转化, 而Fe5C2的量减少; 用于FTO反应时, 在320 ℃、1.0 MPa、H2/CO=1条件下, CO转化率为41.5%, 低碳烯烃的选择性达到60.1%, 而甲烷的选择性只有9.7%.另外催化剂组成、预处理和反应条件的不同都可影响Mn助剂的提升效果.例如, 催化剂在制备过程中, Fe与Mn生成Fe3-yMnyO4(y随Mn的加入量变化)类化合物, 抑制了Fe的还原及FexC的生成, 降低了催化剂的活性[17].
研究表明, K和Mn助剂的协同作用提高了低碳烯烃选择性和催化活性. Wang等[18]使用KMnO4为K和Mn的来源制备了Fe/MnK-CNTs催化剂, 主金属与载体相互作用明显减弱, 催化剂具有更好的分散度; 220 ℃煅烧的催化剂低碳烯烃选择性超过50%(270 ℃, 2 MPa, H2/CO=1). Chen等[19]制备了Fe/MnK-CNTs催化剂, 随着K和Mn含量的增加, 催化剂的活性受到一定的抑制, 但低碳烯烃的选择性稳步上升, 催化剂Fe/Mn16.5K1.2-CNTs展示了最高的低碳烯烃选择性.可见助剂与活性相之间在制备过程中产生一定的相互作用, 从而改变催化剂催化性能.
S一直被认为是催化剂中毒的原因之一.但研究表明, 在FTO反应中少量S经过煅烧和还原转化为SO42-, 可增加铁的分散度、降低还原温度, 促进碳化铁的生成; 过量的S则在催化剂中仍以S2-的形式存在, 加速了催化剂的钝化[20-21]. Xu等[21]研究了S在Fe/α-Al2O3中的作用, 发现S的加入抑制了C5+产物的选择性, 增加了C2~C4产物的选择性. Torres Galvis等[22-23]使用含有少量Na和S的柠檬酸为前驱体, 制备了Fe/CNF、Fe/α-Al2O3、Fe/Si和Fe/γ-Al2O3一系列负载型催化剂, 在340 ℃、2 MPa、H2/CO=1的下, C2~C4烯烃的选择性达到53%, 甲烷的选择性则为11%. S的加入弱化了Fe-CO之间的作用力, 而S和Na的协同作用减小了Fe的颗粒, 增加了Fe的分散度, 降低了碳沉积的速率, 提高了催化剂的活性和低碳烯烃的选择, 但是S和Na必须在一个合适的比例下才能将协同作用发挥至最大.其他金属元素Mg、Ca、Zn、Ag、V等也被用于催化剂改性中, 表 2中列举了部分助剂掺杂后催化剂反应性能.
| 表 2 不同助剂对Fe基催化剂反应性能的影响 Table 2 Effect of different promoters on the reaction performance of Fe-based catalysts |
在FTO催化反应中, 载体的使用增加了活性组分的分散度, 使得铁纳米颗粒具有相对窄的尺寸分布和均匀的空间分布, 从而使聚集体的形成最小化.载体的使用也可影响CO和H2以及产物的吸脱附性能等.
氧化物载体尤其是SiO2和Al2O3是常用的载体. SiO2与Al2O3热稳定性好且具有很好的机械强度, 因此在催化领域广泛应用.但是由于金属与载体之间强的相互作用, 阻碍Fe的还原, 进而阻碍碳化铁的形成, 不仅降低了催化剂的活性, 也对低碳烯烃的生成造成了影响, 因此简单使用SiO2与Al2O3作为载体并不能提高低碳烯烃的选择性, 通常通过添加助剂等方式减弱金属与SiO2、Al2O3之间的相互作用.例如, Qing等[31]使用ZrO2修饰Fe/SiO2催化剂, ZrO2的加入明显弱化了Fe与SiO2之间的相互作用, 促进了Fe的还原和碳化铁的生成, 提高了低碳烯烃的选择性. Zhou等[32]使用S修饰多层结构的Fe/Al2O3催化剂, 在350 ℃、1 MPa、H2/CO=1条件下, 低碳烯烃的选择性最高达到了68%.除了SiO2、Al2O3载体外, MgO、ZrO2等也用于FTO反应研究中, 并收到了一定的效果[33-34].
碳材料一般具有较高的比表面积、独特的孔道与表面结构、良好的化学及水热稳定性.更重要的是碳材料作为一种惰性载体, 相较于氧化物载体, 碳材料减弱了金属-载体之间强的相互作用.活性炭(AC)、碳纳米管(CNT)、石墨烯(GO)等常被用来作为FTO催化剂的载体材料. Tian等[27]使用KMnO4对活性炭(AC)表面进行预处理, 增加了活性炭上氧化基团, 制备的Fe-MnK/AC催化剂中Fe分散度增加、颗粒度减小; 在320 ℃、2 MPa、H2/CO=1、GHSV=3000 h-1反应条件下CO的转化率高达85.0%, 低碳烯烃的选择性则为39.4%. Chen等[35]将Fe负载于CNTs内部, 不仅增加了催化剂的稳定性, 在0.5 MPa、320 ℃, H2/CO=2反应条件下, 低碳烯烃的选择性达到了45%. Schulte等[36]使用HNO3和氨水对CNTs进行功能化, 得到了O-CNTs和N-CNTs载体, 制备的Fe基催化剂具有很高的C3-C6烯烃选择性(SC3-C6>85%), 认为使用O或N掺杂后, 为Fe颗粒的负载提供了更多的位点同时促进了Fe5C2的生成. Lu等[37]使用吡啶为前驱体采用化学沉积的方法, 制备了N掺杂的碳纳米管(NCNTs), N的掺杂增加了载体的碱性, 提高了CO的解离吸附和烯烃的脱附, 促进了Fe的还原和活性组分Fe5C2的生成, 催化剂Fe/NCNTs的低碳烯烃选择性达到了46.7%, 活性和稳定性也得到了很大的提高.石墨烯是一种二维结构的碳材料, 具有较大的表面积和良好的导电导热性能. Cheng等[14]制备了FeK/rGO催化剂, 在340 ℃、2 MPa、H2/CO=1反应条件下C2~C4烯烃选择性达68%, 而此时的CO转化率约为60%. Cheng等[25]在FeK/rGO中加入Mg制得FeMgK/rGO催化剂, 低碳烯烃选择性仍达到了65.0%, 且CO2的选择性大大降低.
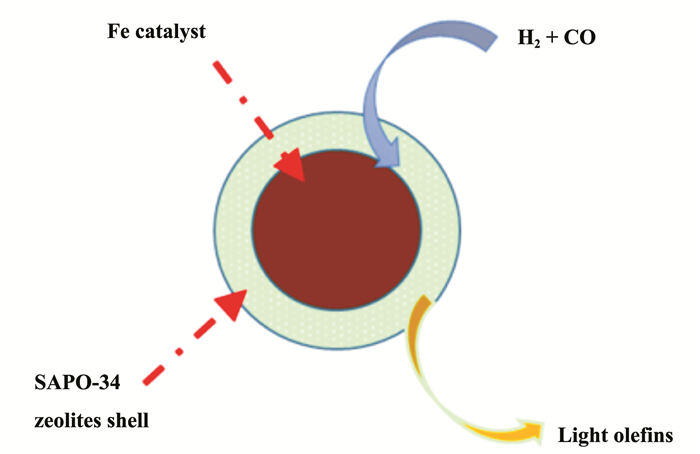
碳材料减弱了金属与载体之间的相互作用, 极大的提高了铁的活性, 促进了铁和化学促进剂之间的密切接触, 但这种表面与铁纳米粒子之间的弱物理结合极易造成Fe纳米颗粒的流失.壳核结构载体不仅提高了催化剂的稳定性, 还有效的阻止了金属粒子烧结, 同时通过调变孔径结构对产物选择性也可产生影响. Ni等[38]以聚乙烯吡咯烷酮(PVP)和四乙基原硅酸盐(TEOS)等为原料, 采用水热沉积法制备了Fe@SiO2-GC催化剂, 催化剂中Fe粒子具有很高分散度和较好的还原性, 壳核结构还进一步限制了Fe颗粒的烧结, 使得催化剂具有很高的活性, 同时壳核结构的空间作用限制了碳链的增长, 极大的促进低碳烯烃的生成. Di等[39]使用沉淀的方式制备了FeMn催化剂并采用水热合成方法制备了SAPO-34分子筛, 采用物理粘合法制备了SAPO-34分子筛包裹的FeMn@SAPO催化剂(图 3), 低碳烯烃的选择性达到52.0%, 远高于FeMn和FeMn/SAPO-34催化剂, 可见壳核结构在限制低碳烯烃的二次加氢方面具有十分重要的作用.
|
图 3 FeMn@SAPO-34壳核结构催化剂[39] Fig.3 FeMn@SAPO-34 shell core catalyst |
在CO加氢中, Co催化剂在反应过程中所需要的温度和压力远低于Fe基催化剂, 催化剂也具有更好的稳定性, Co基催化剂主要侧重于长链烃的生成, 因此单纯使用Co作为催化剂制备低碳烯烃并不能达到理想的效果.通过添加助剂改性等方法增加Co基催化剂的低碳烯烃选择性仍得到了广泛的关注和研究.
应用于Co基催化剂的助剂与Fe基催化剂类似, 有Mn、碱金属、Zn、Ce以及S等, 其中Mn是应用最为广泛且效果较好的助剂. Pedersen等[40]使用不同的负载顺序制备了CoMn/γ-Al2O3催化剂, Mn助剂的加入降低了CH4的选择性, 提高了C2~C4烯烃和C5+产物的选择性, 同时催化剂的活性也得到提高; 理论计算表明Mn的加入可以改变Co结合能, 加速了CO的解离吸附, 并且阻止了CH2-的进一步加氢, 减少了CH3-和CH4的形成. Co和Mn的比例也可产生重要的影响, Dinse等[41]研究了SiO2担载的CoMn催化剂, 发现当Mn:Co的比例高于0.05时, Mn的促进作用不再明显. Johnson等[42]则进一步研究发现, 当Mn:Co比例高于0.1时, Mn则会集中于SiO2表面, 对催化作用完全起不到任何作用.在负载型催化剂中, 尽管有研究可以将Mn:Co提高到0.45, 这需要催化剂具有合适的制备方法, 否则Mn的过度加入只能起到负面的效应[43].
除了Mn以外, Zn、S等也被用于Co催化剂的助剂并收到了不错的效果. Feyzi等[44]制备了Zn提升的Co/TiO2催化剂, 发现Zn的加入在一定程度上能提升催化剂的活性和低碳烯烃的选择性. Barrientos等[45]具体考察了S的含量对Pt提升的Co/γ-Al2O3催化剂在CO加氢方面的影响, 发现S的加入可以阻碍烯烃的二次加氢, 并减少长链烃的生成.
S+Na协同作用在Co基催化剂中也可抑制1-烯烃的异构化, 提高低碳烯烃的选择性, Xie等[46]制备了Co/Mn/Na/S催化剂, 评价结果显示, 在240 ℃、0.1 MPa条件下, 催化剂Co1Mn3-Na2S与CoMn催化剂比较, 甲烷的选择性大幅度降低, C2~C4烯烃选择性增加(54%), 当压力提高到1 MPa, 烯烃选择性仍为30%.可见, Na和S的协同作用不仅对于Fe基催化剂有效果, 对于Co基催化剂也具有同样的效果.
3 结论与展望经由FTS过程直接制备低碳烯烃仍存在很多问题: CO具有很高的转化率, 催化剂中低碳烯烃的选择性较低; 催化剂尽管具有很高的低碳烯烃选择性, 但CO转化率过低, 提高反应温度后CH4和C5+选择性增加, 低碳烯烃产率降低; 催化剂水煤气变换反应转化活性较高, CO2选择性过高致使催化剂碳利用率降低; 在FTO反应催化剂中, 不仅面临活性金属流失、金属与载体强的相互作用等问题, 同时也要面对催化剂表面积炭致使反应器发生堵塞、催化剂活性覆盖等问题.
对于以上问题, 需要从以下几个方面加强对催化剂及其反应体系的研究.一是加强机理的研究, 尤其是加入助剂在催化剂表明的作用机理; 二是增加对主金属及助剂协同作用的研究, 单一的助剂不能满足低碳烯烃的选择性, 需要多种助剂与主金属相互配合使用, 精确各个组分含量, 构建有效的催化剂反应体系; 三是增加新型载体的研发, 避免催化剂在反应过程中出现烧结、金属流失、过度加氢等问题.
| [1] |
Wang Ye(王野), Kang Jin-can(康金灿), Zhang Qing-hong(张庆红). Research advancein catalysts for Fischer-Tropsch synthesis(费托合成催化剂的研究进展)[J]. Petro Technol(石油化工), 2009, 38(12): 1255–1263.
DOI:10.3321/j.issn:1000-8144.2009.12.001 |
| [2] |
Ren Cheng(任诚). Production technology & industry for eground about the production of light olefins with non-oil route(非石油路线制取低碳烯烃的生产技术及产业前景)[J]. Fine Chem Inter(精细化工中间体), 2007, 37(5): 6–9.
DOI:10.3969/j.issn.1009-9212.2007.05.002 |
| [3] |
Henrici-Olivé G, Olivé S. The Fischer-Tropsch synthesis: Molecular weight distribution of primary products and reaction mechanism[J]. Angew Chem Inter Edit, 1976, 15(3): 136–141.
DOI:10.1002/anie.197601361 |
| [4] |
Teng X S, Huang S Y, Wang J, et al. Fabrication of Fe2C embedded in hollow carbon spheres: a high-performance and stable catalyst for Fischer-Tropsch synthesis[J]. Chem Cat Chem, 2018, 10(17): 3883–3891.
|
| [5] |
Zhao X, Lv S A, Li W G, et al. Comparison of preparation methods of iron-based catalysts for enhancing Fischer-Tropsch synthesis performance[J]. Mol Catal, 2018, 449: 99–105.
DOI:10.1016/j.mcat.2018.02.022 |
| [6] |
Yang C, Zhao H B, Hou Y L, et al. Fe5C2 Nanoparticles: A Facile bromide-induced synthesis and as an active phase for Fischer-Tropsch synthesis[J]. J Am Chem Soc, 2012, 134(38): 15814–15821.
DOI:10.1021/ja305048p |
| [7] |
Chang Q, Zhang C H, Liu C W, et al. Relationship between iron carbide phases (#-Fe2C, Fe7C3, and #-Fe5C2) and catalytic performances of Fe/SiO2 Fischer-Tropsch catalyst[J]. ACS Catal, 2018, 8(4): 3304–3316.
DOI:10.1021/acscatal.7b04085 |
| [8] |
deSmit E, Cinquini F, Beale A M, et al. Stability and reactivity of ε-χ-θ iron carbide catalyst phases in Fischer-Tropsch synthesis: controlling μc[J]. J Am Chem Soc, 2010, 132(42): 14928–14941.
DOI:10.1021/ja105853q |
| [9] |
BassetJ, Chauvin Y, Commereuc D, et al. FR Patent 2391978[P], 1977.
|
| [10] |
Tang L P, Song C L, Li M L, et al. Study of K/Mn-MgO supported Fe catalysts with Fe(CO)5 and Fe(NO3)3 as precursors for CO hydrogenation to light alkenes[J]. Chin J Chem, 2013, 31(10): 1263–1268.
DOI:10.1002/cjoc.201300514 |
| [11] |
Commereuc D, Chauvin Y. Catalytic synthesis of low molecular weight olefins from CO and H2 with Fe(CO)5, Fe3(CO)12, and [HFe3(CO)11]- supported on inorganic oxides[J]. J Chem Soc Chem Commun, 1980, 1980(4): 154–155.
|
| [12] |
Ribeiro M C, Jacobs G, Davis B H, et al. Fischer-Tropsch synthesis: An in-situ TPR-EXAFS/XANES investigation of the influence of group I alkali promoters on the local atomic and electronic structure of carburized iron/silica catalysts[J]. J Phys Chem C, 2010, 114(17): 7895–7903.
DOI:10.1021/jp911856q |
| [13] |
Ngantsoue-Hoc W, Zhang Y Q, O'Brien R J, et al. Fischer-Tropsch synthesis: activity and selectivity for group I alkali promoted iron-based catalysts[J]. Appl Catal A Gener, 2002, 236(1/2): 77–89.
|
| [14] |
Cheng Y, Lin J, Xu K, et al. Fischer-Tropsch synthesis to lower olefins over potassium-promoted reduced graphene oxide supported iron catalysts[J]. ACS Catal, 2016, 6(1): 389–399.
DOI:10.1021/acscatal.5b02024 |
| [15] |
Kang S H, Bae J W, Prasad P S S, et al. Effect of preparation method of Fe-based Fischer-Tropsch catalyst on their light olefin production[J]. Cata Lett, 2009, 130(3/4): 630–636.
|
| [16] |
Liu Y, Chen J F, Bao J, et al. Manganese-modified Fe3O4 microsphere catalyst with effective active phase of forming light olefins from syngas[J]. ACS Catal, 2015, 5(6): 3905–3909.
DOI:10.1021/acscatal.5b00492 |
| [17] |
Xu J D, Zhu K Y, Weng X F, et al. Carbon nanotube-supported Fe-Mn nanoparticles: A model catalyst for direct conversion of syngas to lower olefins[J]. Catal Today, 2013, 215(15): 86–94.
|
| [18] |
Wang D, Ji J, Chen B X, et al. Novel Fe/MnK-CNTs nanocomposites as catalysts for direct production of lower olefins from syngas[J]. AI Ch E J, 2017, 63(1): 154–161.
DOI:10.1002/aic.15490 |
| [19] |
Chen B X, Zhang X X, Chen W Y, et al. Tailoring of Fe/MnK-CNTs composite catalysts for the Fischer-Tropsch synthesis of lower olefins from syngas[J]. Indus Eng Chem Res, 2018, 57(34): 11554–11560.
DOI:10.1021/acs.iecr.8b01795 |
| [20] |
Wu B S, Bai L, Xiang H W, et al. An active iron catalyst containing sulfur for Fischer-Tropsch synthesis[J]. Fuel, 2004, 83(2): 205–212.
|
| [21] |
Xu J D, Chang Z Y, Zhu K T, et al. Effect of sulfur on α-Al2O3-supported iron catalyst for Fischer-Tropsch synthesis[J]. Appl Catal A Gen, 2016, 514(25): 103–113.
|
| [22] |
Torres Galvis H M, Bitter J H, Khare C B, et al. Supported iron nanoparticles as catalysts for sustainable production of lower olefins[J]. Science, 2012, 335(6070): 835–838.
DOI:10.1126/science.1215614 |
| [23] |
Torres Galvis H M, Koeken A C J, Bitter J H, et al. Effects of sodium and sulfur on catalytic performance of supported iron catalysts for the Fischer-Tropsch synthesis of lower olefins[J]. J Catal, 2013, 303: 22–30.
DOI:10.1016/j.jcat.2013.03.010 |
| [24] |
Li T Z, Wang H L, Yang Y, et al. Effect of manganese on the catalytic performance of an iron-manganesebimetallic catalyst for light olefin synthesis[J]. J Energ Chem, 2013, 22(4): 624–632.
DOI:10.1016/S2095-4956(13)60082-0 |
| [25] |
Cheng Y, Lin J, Wu T J, et al. Mg and K dual-decorated Fe-on-reduced graphene oxide for selective catalyzing CO hydrogenation to light olefins with mitigated CO2 emission and enhanced activity[J]. Appl Catal B Environ, 2017, 204(5): 475–485.
|
| [26] |
Zhang Y L, Ma L L, Wang T J, et al. Synthesis of Ag promoted porous Fe3O4 microspheres with tunable pore size as catalysts for Fischer-Tropsch production of lower olefins[J]. Catal Commun, 2015, 64: 32–36.
DOI:10.1016/j.catcom.2015.01.033 |
| [27] |
Tian Z P, Wang C G, Si Z, et al. Fischer-Tropsch synthesis to light olefins over iron-based catalysts supported on KMnO4 modified activated carbon by a facile method[J]. Appl Catal A Gen, 2017, 541: 50–59.
DOI:10.1016/j.apcata.2017.05.001 |
| [28] |
Oschatz M, Hofmann J P, van Deelen T W, et al. Effects of the functionalization of the ordered mesoporous carbon support surface on iron catalysts for the Fischer-Tropsch synthesis of lower olefins[J]. Chem Catal Chem, 2017, 9(4): 620–628.
|
| [29] |
Gao X H, Zhang J L, Chen N, et al. Effects of zinc on Fe-based catalysts during the synthesis of light olefins from the Fischer-Tropsch process[J]. Chin J Catal, 2016, 37(4): 510–516.
DOI:10.1016/S1872-2067(15)61051-8 |
| [30] |
Wang G C, Zhang K, Liu P, et al. Synthesis of light olefins from syngas over Fe-Mn-V-K catalysts in the slurry phase[J]. J Ind Eng Chem, 2013, 19(3): 961–965.
DOI:10.1016/j.jiec.2012.11.017 |
| [31] |
Qing M, Yang Y, Wu B S, et al. Modification of Fe-SiO2 interaction with zirconia for iron-based Fischer-Tropsch catalysts[J]. J Catal, 2011, 279(1): 111–122.
DOI:10.1016/j.jcat.2011.01.005 |
| [32] |
Zhou X P, Ji J, Wang D, et al. Hierarchical structured α-Al2O3 supported S-promoted Fe catalysts for direct conversion of syngas to lower olefins[J]. Chem Commun, 2015, 51(42): 8853–8856.
DOI:10.1039/C5CC00786K |
| [33] |
Lødeng R, Lunder O, Lein J E, et al. Synthesis of light olefins and alkanes on supported iron oxide catalysts[J]. Catal Today, 2018, 299: 47–59.
DOI:10.1016/j.cattod.2017.06.039 |
| [34] |
Zhang H, Chen W, Zhou J, et al. React. Effects of potassium on MgO-supported Fe-Mn catalysts for the hydrogenation of carbon monoxide to light alkenes[J]. React Kinet Catal Lett, 2008, 94(1): 139–147.
DOI:10.1007/s11144-008-5314-6 |
| [35] |
Chen X Q, Deng D H, Pan X L, et al. Iron catalyst encapsulated in carbon nanotubes for CO hydrogenation to light olefins[J]. Chin J Catal, 2015, 36(9): 1631–1637.
DOI:10.1016/S1872-2067(15)60882-8 |
| [36] |
Schulte H J, Graf B, Xia W, et al. Nitrogen- and oxygen-functionalized multiwalled carbon nanotubes used as support in iron-catalyzed, high-temperature Fischer-Tropsch synthesis[J]. Chem Catal Chem, 2012, 4(3): 350–355.
|
| [37] |
Lu J Z, YangL J, Xu B L, et al. Promotion effects of nitrogen doping into carbon nanotubes on supported iron Fischer-Tropsch catalysts for lower olefins[J]. ACS Catal, 2014, 4(2): 613–621.
DOI:10.1021/cs400931z |
| [38] |
Ni Z J, Qin H F, Kang S F, et al. Effect of graphitic carbon modification on the catalytic performance of Fe@SiO2-GC catalysts for forming lower olefins via Fischer-Tropsch synthesis[J]. J Coll Interf Sci, 2018, 516: 16–22.
DOI:10.1016/j.jcis.2018.01.017 |
| [39] |
Di Z X, Zhao T J, Feng X L, et al. A newly designed core-shell-like zeolite capsule catalyst for synthesis of light oleins from syngas via Fischer-Tropsch synthesis reaction[J]. Catal Lett, 2019, 149(2): 441–448.
DOI:10.1007/s10562-018-2624-9 |
| [40] |
Pedersen E Ø, Svenumb I H, Blekkan E A. Mn promoted Co catalysts for Fischer-Tropsch production of light olefins-An experimental and theoretical study[J]. J Catal, 2018, 361: 23–32.
DOI:10.1016/j.jcat.2018.02.011 |
| [41] |
Dinse A, Aigner M, Ulbrich M, et al. Effects of Mn promotion on the activity and selectivity of Co/SiO2 for Fischer-Tropsch synthesis[J]. J Catal, 2012, 288: 101–114.
|
| [42] |
Johnson G R, Bell A T. Effects of lewis acidity of metal oxide promoters on the activity and selectivity of Co-based Fischer-Tropsch synthesis catalysts[J]. J Catal, 2016, 338: 250–264.
DOI:10.1016/j.jcat.2016.03.022 |
| [43] |
Morales F, Smit E D, Groot F M F D, et al. Effects of manganese oxide promoter on the CO and H2 adsorption properties of titania-supported cobalt Fischer-Tropsch catalysts[J][J]. J Catal, 2007, 246: 91–99.
DOI:10.1016/j.jcat.2006.11.014 |
| [44] |
Feyzi M, Khodaei M M, Shahmoradi J. Effect of preparation and operation conditions on the catalytic performance of cobalt-based catalysts for light olefins production[J]. Fuel Process Technol, 2012, 93(1): 90–98.
DOI:10.1016/j.fuproc.2011.09.021 |
| [45] |
Barrientosa J, Montesb V, Boutonneta M, et al. Further insights into the effect of sulfur onthe activity and selectivity of cobalt-based Fischer-Tropsch catalysts[J]. Catal Today, 2016, 275: 119–126.
DOI:10.1016/j.cattod.2015.10.039 |
| [46] |
Xie J X, Paalanen P P, Deelen T W V, et al. Promoted cobalt metal catalysts suitable for the production of lower olefins from natural gas[J]. Nat Commun, 2019, 10: 167–177.
DOI:10.1038/s41467-018-08019-7 |
 2019, Vol. 33
2019, Vol. 33


