2. 中国科学院大学, 北京 100049;
3. 中国科学院兰州化学物理研究所 苏州研究院, 江苏 苏州 215123;
4. 南京尊龙新材料科技有限公司, 江苏 南京 211516
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. Suzhou Research Institute of LICP, Chinese Academy of Sciences, Suzhou 215123, China;
4. Nanjing Zunlong New Material Technology Co., Ltd, Nanjing 211516, China
植物油的氢化在煎炸油、起酥油、人造黄油、工业油和润滑油的生产中非常重要.油脂催化加氢可以降低油脂的不饱和程度, 氢化过程会改善油的色泽和风味[1], 提高其熔点并保持油的品质, 氢化油在室温下呈固体或半固体状态[2-4], 有效提高了产品的抗氧化性和化学稳定性, 使该产品既可以用作人类的主要营养物质和主要食物之一, 也是一种重要的工业原料.
镍基催化剂由于其高活性、低成本以及反应后易于从产物中分离的特点至今仍然成为植物油加氢中使用最广泛的一类催化剂[5-6]. Cepeda E A等[1]研究金属活性组分对氢化活性的影响, 提出了以下顺序: Pd>Pt>Ni>Co>Cu, 虽然Ni并非活性最高, 但是在目标碘值(人造奶油)为70时, 负载型镍催化剂产生的反式异构体最少.常用的制备负载型镍催化剂的方法有共沉淀法、浸渍法、化学混合法、液相还原法等, 其中沉淀法是该类催化剂在工业上更为普遍采用的.影响镍基催化剂催化性能的因素有很多, 诸如助剂、载体种类、沉淀剂的种类、焙烧温度、还原温度等等.刘伟等[7]研究了载体对镍催化剂性能的影响.发现载体上的催化活性为:自制氧化铝>工业氧化铝>二氧化硅>硅藻土.薛冬等[8]研究了柠檬酸的添加方式对Mo-Ni-P/Al2O3催化剂加氢活性的影响, 发现经柠檬酸后处理的催化剂具有较好的金属分散度从而提高了其加氢活性.目前很多研究[9-11]报道了沉淀剂的种类(如NaOH、Na2CO3、NH3·H2O)对催化剂活性的影响, 但对于催化剂中残留的碱性金属离子(Na)对镍催化剂加氢活性影响缺少系统的研究, 只是通常认为Na应该越低越好.在Cu/SiO2加氢催化剂中, 发现微量Na的存在对催化剂最终稳定性有较大影响[12-14]. Jun等[15]报道了残留的Na对甲醇合成的Cu/ZnO/Al2O3催化剂具有抑制活性作用. Mirzaei, Ali A等[16]发现残留的表面碱金属阳离子是CO氧化过程中的催化剂毒物.我们采用共沉淀法以Na2CO3为沉淀剂制备了Ni-Mg/SiO2催化剂, 通过洗涤次数的不同, 控制催化剂中残留Na的含量, 考察了其催化大豆油加氢活性, 并与结构表征进行了关联.
1 实验部分 1.1 试剂原料: Ni(NO3)·6H2O(西陇科学股份有限公司), Mg(NO3)·6H2O、Na2SiO3·5H2O(天津市科密欧化学试剂有限公司), 无水Na2CO3(四川西陇化工有限公司), 均为分析纯, 食用大豆油(金龙鱼, 碘值Iv=130/100 g).
1.2 催化剂制备将一定量的Ni(NO3)·6H2O和Mg(NO3)·6H2O在搅拌下溶于去离子水中, 向其中逐滴滴加Na2SiO3·5H2O溶液Ni:Si=1:1(molar ratio), 然后用一定浓度的Na2CO3溶液调节混合溶液的pH值至9~10, 60 ℃下老化1 h后过滤, 用去离子水洗涤至pH=7, 分别收集洗涤0、2、4、6、8次的滤饼置于120 ℃下干燥, 所得催化剂前驱体在300 ℃下焙烧4 h, 再于400 ℃的管式炉中氢气气氛下还原2 h, 分散于保护油中备用.采用ICP-AES测得焙烧后未经还原处理的催化剂中残留的钠含量, 结果如表 1所示. Na含量随洗涤次数的增加而减小, 当洗涤4次以后Na含量降为0.23%, 洗涤次数继续增加时, Na含量基本不变.选择典型残留钠的样品(未洗涤、洗涤2次和8次, 根据Na含量分别记作7Na、1Na、0.2Na)进行表征与反应评价.
| 表 1 ICP-AES测得的残留Na含量 Table 1 Residual Na content measured by ICP-AES |
采用Smartlab-SE X射线衍射仪(XRD)测定催化剂的物相结构, 测试条件: Cu Kα(λ = 0.154 18 nm), Ni滤光片, 工作电压40 kV, 电流40 mA, 扫描步长0.01°, 扫描范围: 5°~80°.
催化剂的H2-TPR在ChemBET Pulsar TPR/TPD(Quantachrome Instruments U.S.)仪器上进行:将10 mg焙烧后未经还原处理的催化剂装入U型石英管中在10%H2/Ar混合气(40 mL/min)中从室温以20 ℃/min的速率升至900 ℃, H2的消耗TCD检测器采集.
热重-差示扫描量热(TG-DSC)在同步热分析仪(STA NETZSCH 449F3, 德国NETZSCH)上测定.分析条件:样品在空气气氛下10 ℃/min升温到800 ℃.
场发射扫描电子显微照片在超高分辨场发射扫描电子显微镜(SU8020, 日本日立)上获得.
BET表面积的测量在Micromeritics ASAP 2010仪器上在液氮温度下进行.使用JSM-6701F扫描电子显微镜研究了样品的微观结构.
催化剂中残留Na元素含量用电感耦合等离子体原子发射光谱(ICP-AES, 型号: PQ9000)测得.
1.4 催化剂活性评价将大豆油和一定质量的催化剂(mcatalyst/msoybean oil=0.2%)加入干燥洁净的带聚四氟乙烯内衬的100 mL不锈钢高压反应釜中, 密封反应釜, 用氢气置换釜内的空气4~5次.升温至150 ℃, 调整搅拌速率至700 r·min-1, 补充H2压力为0.4 MPa, 保持恒压反应2 h.反应结束后, 待温度降至90 ℃左右时, 放出釜中物料, 过滤催化剂, 用Wijis法滴定氢化油碘值.
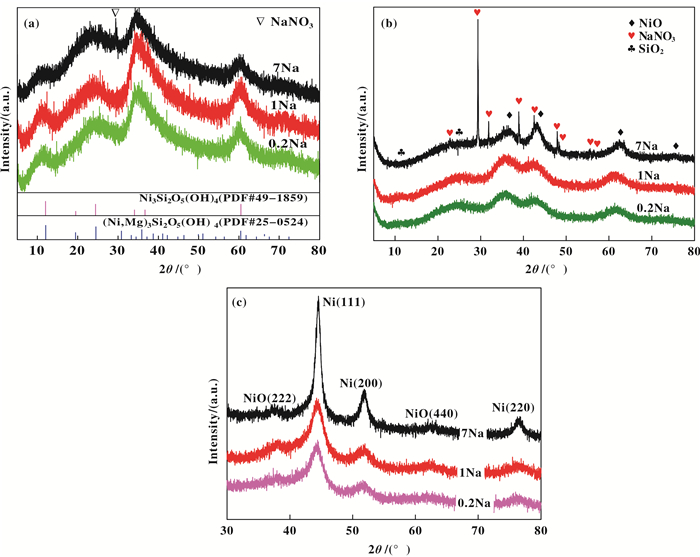
2 结果与讨论 2.1 XRD分析采用XRD对制备过程中不同阶段的催化剂进行了物相分析, 结果如图 1a-c所示.图 1(a)显示了干燥后、未焙烧样品呈现相似的衍射峰, 无论钠含量的高低, 均在2θ=11.32°、24.36°、34.82°、60.52°出现强度不同的宽峰, 经检索可归属于Ni3Si2O5(OH)4[17]物相, 没有出现任何形式的Mg的特征峰, 表明少量Mg助剂以高分散的形式存在[18]或低含量的镁可能嵌入到Ni3Si2O5(OH)4的晶格中形成(Ni, Mg)3Si2O5(OH)4相, 导致衍射峰的重叠或宽化、偏移.此外, 在高Na含量样品中(7Na)观察到2θ=29.4°处有一弱衍射峰, 可归属于NaNO3结晶. 300 ℃焙烧后(图 1b)该峰变得较为尖锐, 并且在31.83°、38.98°、42.40°、47.92°又产生了新的特征峰, 这表明焙烧过程中NaNO3微晶进一步发生团聚, 结晶度提高. 3个样品在2θ=35.56°、43.07°、62.02°、75.62°处的衍射峰为NiO的特征峰, 随Na含量的降低, 峰变弱.此外, 无定型SiO2的弥散峰(2θ=11.1°和24.3°)在3个样品中也都出现, 高Na样品更微弱一些, 这些物相说明在焙烧阶段, 前驱体已得到分解.经还原之后(图 1c), Ni成为主要物相, 可以清楚的看到高Na含量时, Ni的衍射峰更加尖锐, 同时NaNO3衍射峰消失.表明在还原过程中, NaNO3进一步分解.这一点在后面的TG-DSC分析中也得到验证.同时发现有少量NiO存在, 可能是催化剂没有被完全还原或者是在催化剂倒入保护油的过程中有少量的金属镍与空气接触被氧化.通过Scherrer公式: d=Κλ/Bcosθ(K—Scherrer常数, 通常为0.89)可计算出还原后金属Ni的平均晶粒尺寸(数据列于表 2).随着残留Na量的降低, Ni的颗粒尺寸下降, 0.2Na的样品尺寸降至3.3 nm.过去的研究表明, Ni颗粒尺寸是影响油脂加氢活性的关键因素[19], 尺寸越小, 活性越高.因此, 催化剂中残留Na可能通过影响Ni的粒径影响加氢活性.
|
图 1 不同Na含量样品的XRD图 Fig.1 XRD patterns of the samples with different Na content a. dried sample; b. calcined sample; c. reduced sample |
| 表 2 不同Na含量Ni-Mg/SiO2催化剂的特性及活性评价结果 Table 2 Characterization and activity evaluation results of Ni-Mg/SiO2 catalysts with different Na content |
不同钠含量的Ni-Mg/SiO2催化剂经焙烧后的样品进行了SEM分析, 如图 2a-c所示, 从图中可以看出, 高Na样品板结现象比较严重, 随着Na量的降低, 催化剂颗粒之间松散程度增加, 至0.2Na时, 催化剂颗粒更小、且分散更均匀, 能够看到更多的空隙.如上述XRD表征结果, 7Na样品检测NaNO3晶体, 而NaNO3的熔点为306 ℃, 在焙烧过程中, 可能在催化剂表面发生熔融聚集和粘接, 导致不同Na含量样品的形貌和颗粒大小的差异.

|
图 2 焙烧后样品的SEM图 Fig.2 SEM images of the calcined samples: a. 7 Na; b. 1 Na; c. 0.2 Na |
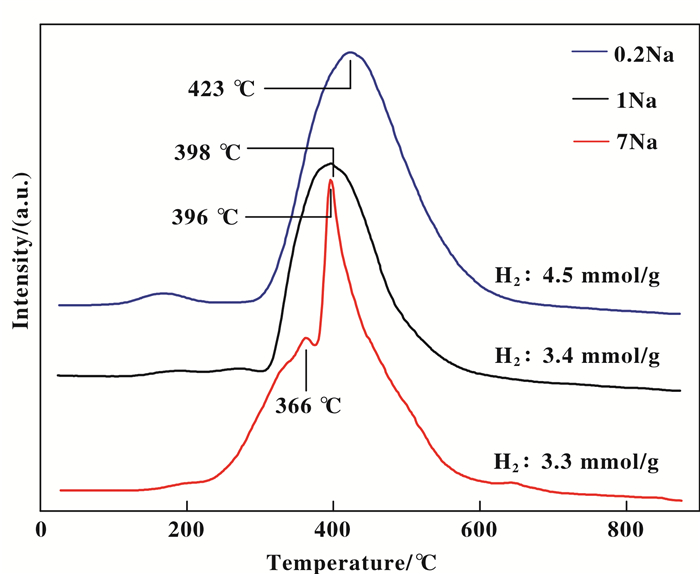
为了考察不同残留Na量是否影响Ni与载体的相互作用及催化剂的还原性质, 采用H2-TPR对7Na、1Na、0.2Na 3个样品进行了表征, 图 3显示了不同钠含量催化剂的H2-TPR曲线. 3个样品在400 ℃附近NiO的还原峰随残留Na量的不同, 在峰型和最高还原温度上有明显区别.对于高Na样品(7Na), NiO还原峰裂分为两个, 峰值分别为366和396 ℃, 且起始还原温度在220 ℃左右, 远低于低Na含量的两个样品(300 ℃).这表明一方面Na含量高时, 负载的镍是不均匀分散的[20].根据400 ℃附近的还原峰面积计算了氢消耗量, 与样品中残留Na量呈负相关, Na含量从6.86%降至0.2%, 还原耗氢量则从3.3提高至4.5 mmol/g, 说明随着残留Na量的降低, Ni的相对还原度增加.此外, 由H2-TPR还观察到NiO的还原峰随Na的降低而向高温区移动, 0.2Na的样品, 最高还原温度提高至423 ℃, 也说明降低Na, 可使催化剂表面NiO颗粒尺寸减小, 并增强与SiO2载体的相互作用[21-24], 这与XRD表征结果相吻合.
|
图 3 不同Na含量的焙烧后催化剂的H2-TPR图 Fig.3 H2-TPR profiles of the calcined catalysts with different Na content |
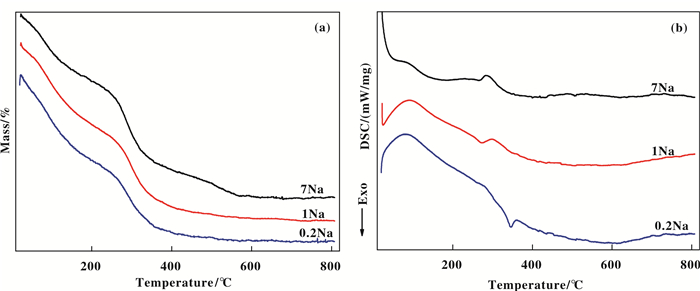
采用TG-DSC对催化剂前驱体的热分解行为进行了进一步的表征, 其结果如图 4所示.对比TG曲线(图 4(a)), 1Na和0.2Na样品热失重相似, 在250~300 ℃发生主要的质量损失, 根据XRD表征, 这是由于催化剂在沉淀时形成的前驱体Ni3Si2O5-(OH)4分解.但DSC分析(图(4b))显示出分解产生的吸热峰温不同, 当Na量从1Na降至0.2Na后, 吸热峰温度提高了约50 ℃.高Na样品(7Na)中, 除了有前驱体Ni3Si2O5(OH)4分解失重以外, 在400~600 ℃有缓慢的质量损失, 伴随着一定的吸热, 这可能与该样品中存在大量NaNO3有关.通常, NaNO3自380 ℃开始发生分解[25], 经历如下过程:
| $ \begin{array}{ll} {380^{\circ} \mathrm{C}} & {2 \mathrm{NaNO}_{3} \rightarrow 2 \mathrm{NaNO}_{2}+\mathrm{O}_{2}} \\ {400 \sim 600^{\circ} \mathrm{C}} & {4 \mathrm{NaNO}_{2} \rightarrow 2 \mathrm{Na}_{2} \mathrm{O}+2 \mathrm{N}_{2}+\mathrm{O}_{2}} \end{array} $ |
|
图 4 不同Na含量的催化剂的TG-DSC图 Fig.4 TG-DSC curves of the catalysts with different Na content |
同时还应注意到Ni前驱体分解吸热峰温度比低Na样品降低了约20 ℃, 按Na含量从高到低, 分解吸热温度7Na(280 ℃) < 1Na(300 ℃) < 0.2Na(350 ℃).因此, DSC与TG的分析也表明催化剂中高Na含量导致Ni与SiO2的相互作用减弱, Na越少, 相互作用越强.
此外, 3个样品在200 ℃之前发生的失重, 通常是由于吸附的水分、沉淀物所含的结构水等引起, 质量损失在15%~17%之间.
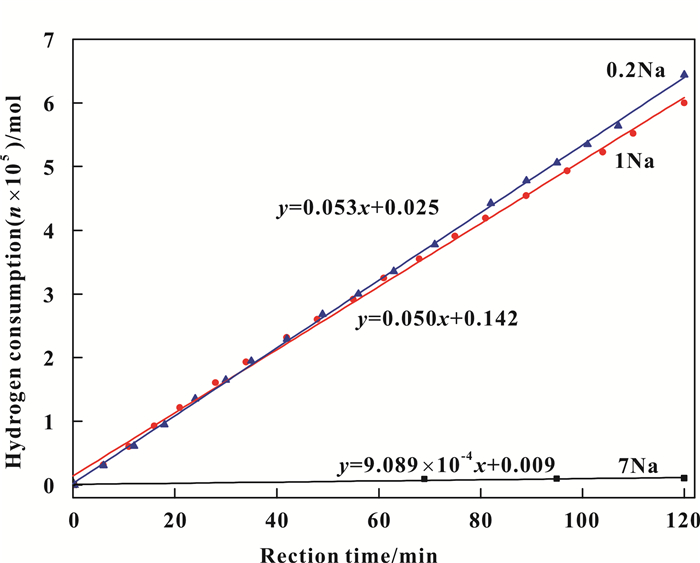
2.5 Ni-Mg/SiO2催化剂活性分析Na含量与催化剂加氢活性的关系如表 2所示, 通过N2吸脱附测得的不同残留Na含量催化剂的比表面积(SBET)、平均孔径(dp)也列于表 2.催化剂中残留的Na含量对比表面积和孔径分布有显著的影响.随着Na含量从7Na降到0.2Na, 催化剂的比表面积SBET由16.6逐渐增大到245.4 m2·g-1, 正如XRD结果表明, 这是NaNO3微晶堵塞孔所导致[26]. 1Na和0.2Na样品的平均孔径和孔体积差别不大, 而7Na样品的平均孔径为11.99 nm, 比前者大很多, 也是由于高含量的Na堵塞了小孔, 从而孔体积也较小.随着洗涤次数增多, 孔道中残留的Na被洗掉, 暴露出大量的小孔, 所以平均孔径减小, 孔体积增大.随着比表面积和孔体积的增大, 加氢活性呈上升趋势, 因为有更多的孔道可供油脂分子利用, 从而使更多的反应物吸附在活性中心上进行反应[27].从表 2可以看出, 催化剂中Na含量越低, 氢化油的碘值越低. 7Na样品的氢化油碘值Iv=125/100 g, 此时催化剂基本没有活性, 结合XRD、H2-TPR和SEM结果可以得出, 高含量Na的存在会导致活性组分镍的严重团聚, 粒径增大, 从而降低了催化剂的加氢活性.不同Na含量的催化剂的耗氢速率曲线如图 5所示, 耗氢曲线斜率越大, 则催化剂加氢速率越快, 活性越好.高Na含量催化剂耗氢曲线斜率k≈0, 所以其基本无活性, 碘值(Iv=125/100 g)与大豆油(Iv=130/100 g)接近.比较1Na和0.2Na两个催化剂, 反应时间小于50 min时, 二者的耗氢速率大致相同. 50 min以后, 反应时间越长, 0.2Na含量的催化剂耗氢速率越大, 说明低Na含量催化剂具有较好的可持续加氢能力.
|
图 5 不同Na含量的催化剂耗氢速率曲线 Fig.5 Hydrogen consumption rate curves of catalysts with different Na contents |
在共沉淀法制备油脂加氢镍基催化剂时, 催化剂中残留的Na含量对加氢活性有较大影响, 通过催化剂不同阶段的结构表征, 其根本原因在于活性组分Ni的颗粒尺寸、形貌、分散度以及与载体SiO2的相互作用差异所致.在制备过程中, Na洗涤的越干净, 残留Na越低, Ni的尺寸越小, 加氢活性则越高.但试验表明, 当Na降低至0.2%后, 通过一般洗涤手段很难再进一步下降.此时Ni0的平均粒径可减小至3 nm左右, 催化剂具有较高的加氢活性.
| [1] |
Cepeda E A, Iriarte-Velasco U, Calvo B, et al. Hydrogenation of sunflower oil over M/SiO2 and M/Al2O3 (M= Ni, Pd, Pt, Co, Cu) catalysts[J]. J Am Oil Chem Soc, 2016, 93(5): 731–741.
|
| [2] |
Belkacemi K, Boulmerka A, Arul J, et al. Hydrogenation of vegetable oils with minimum trans and saturated fatty acid formation over a new generation of Pd-catalyst[J]. Top Catal, 2006, 37(2): 113–120.
|
| [3] |
Choo H P, Liew K Y, Liu H, et al. Activity and selectivity of noble metal colloids for the hydrogenation of polyunsaturated soybean oil[J]. J Mol Catal A: Chem, 2003, 191(1): 113–121.
|
| [4] |
Jovanovic D, cupic Ž, Stankovic M, et al. The influence of the isomerization reactions on the soybean oil hydrogenation process[J]. J Mol Catal A: Chem, 2000, 159(2): 353–357.
|
| [5] |
Jang E S, Jung M Y, Min D B. Hydrogenation for low trans and high conjugated fatty acids[J]. Compr Rev Food Sci F, 2005, 4(1): 22–30.
|
| [6] |
Li T L, Zhang W N, Lee R Z, et al. Nickel-boron alloy catalysts reduce the formation of Trans fatty acids in hydrogenated soybean oil[J]. Food Chem, 2009, 114(2): 447–452.
|
| [7] |
Liu Wei(刘伟), Yu Hai-bin(于海斌), Chen Yong-sheng(陈永生), et al. Effects of support on nickel-based catalysts for hydrogenation of unsaturated oil(载体对镍基催化剂不饱和油脂加氢性能的影响)[J]. Inorg Chem Indus(无机盐工业), 2015, 47(03): 76–78.
|
| [8] |
Xue Dong(薛冬), Lv Zhen-hui(吕振辉). Effect of addition method of critric acid on hydrogenation performance of avtivity of Mo-Ni-P/Al2O3 catalyst(柠檬酸添加方式对Mo-Ni-P/Al2O3催化剂加氢活性的影响)[J]. J Mol Catal(China)(分子催化), 2017, 31(04): 382–389.
|
| [9] |
Li Q Y, Wang R N, Nie Z R, et al. Preparation and characterization of nanostructured Ni(OH)2 and NiO thin films by a simple solution growth process[J]. J Colloid Interfac Sci, 2008, 320(1): 254–258.
|
| [10] |
Zanella R, Giorgio S, Shin C H, et al. Characterization and reactivity in CO oxidation of gold nanoparticles supported on TiO2 prepared by deposition-precipitation with NaOH and urea[J]. J Catal, 2004, 222(2): 357–367.
|
| [11] |
Li J, Xiao B, Yan R, et al. Preparation of NiO nanoparticles by homogeneous precipitation method at optimized process conditions[J]. Chem Eng (China), 2007, 2007(8): 13.
|
| [12] |
Huang Z, Cui F, Kang H, et al. Characterization and catalytic properties of the CuO/SiO2 catalysts prepared by precipitation-gel method in the hydrogenolysis of glycerol to 1, 2-propanediol: Effect of residual sodium[J]. Appl Catal A: Gen, 2009, 366(2): 288–298.
|
| [13] |
Balakos M W, Chuang S S C. A temperature-programmed reaction and X-ray photoelectron spectroscopy study of coprecipitated Na-Mn-Ni catalysts[J]. J Catal, 1992, 138(2): 733–745.
|
| [14] |
Akiyoshi M, Hattori H, Tanabe K J J o T J P I. Effect of the method of preparation of Ni/SiO2-MgO catalysts on decomposition of methanol[J]. J Jpn Petrol Inst, 1988, 31(2): 163–171.
|
| [15] |
Jun K W, Shen W J, Rama Rao K S, et al. Residual sodium effect on the catalytic activity of Cu/ZnO/Al2O3 in methanol synthesis from CO2 hydrogenation[J]. Appl Catal A: Gen, 1998, 174(1): 231–238.
|
| [16] |
Mirzaei A A, Shaterian H R, Joyner R W, et al. Ambient temperature carbon monoxide oxidation using copper manganese oxide catalysts: Effect of residual Na+ acting as catalyst poison[J]. Catal Commun, 2003, 4(1): 17–20.
|
| [17] |
Gabrovska M, Shopska M, Shtereva I, et al. Effect of the preparation method on the reducibility and the crystal size of the Ni-Mg/SiO2 precursors as catalysts for edible oil hydrogenation[C]. Proc. 1st International Workshop on Nanoscience & Nanotechnology IWON 2005.
|
| [18] |
Zhao Fang(赵芳), Wang Chang-zhen(王长真), Tian Ya-ni(田亚妮), et al. Metal promoter effect of Ni-M/SiO2 in hydrogenation of 1, 4-butynediol(Ni-M/SiO2催化1, 4-丁炔二醇加氢的金属助剂效应)[J]. J Mol Catal(China)(分子催化), 2019, 33(01): 83–89.
|
| [19] |
He Xin-xiu(何新秀), Liu Hua(刘华), Xu Qing-huai(许清淮). Study on the relationship between nickel grain size and activity of oil hydrogenation catalyst(油脂加氢催化剂镍晶粒度与活性的关系研究)[J]. Chemistry(化学通报), 1998, 1998(8): 33–35.
|
| [20] |
Hadjiivanov K, Mihaylov M, Klissurski D, et al. Characterization of Ni/SiO2 catalysts prepared by successive deposition and reduction of Ni2+ ions[J]. J Catal, 1999, 185(2): 314–323.
|
| [21] |
Pompeo F, Nichio N N, González M G, et al. Characterization of Ni/SiO2 and Ni/Li-SiO2 catalysts for methane dry reforming[J]. Catal Today, 2005, 107: 856–862.
|
| [22] |
Haller G L, Resasco D E. Metal-support interaction: Group VⅢ metals and reducible oxides[J]. Advances Catal, 1989, 36: 173–235.
|
| [23] |
Resasco D E, Haller G L. A model of metal-oxide support interaction for Rh on TiO2[J]. J Catal, 1983, 82(2): 279–288.
|
| [24] |
Gai Yuan-yuan(盖媛媛), Li Jian-fa(李建法), Sun Rui-xia(孙瑞霞), et al. Hydrogenation of levulinic acid to γ-valerolactone catalyzed by Ni/SiO2-Al2O3(Ni/SiO2-Al2O3催化乙酰丙酸加氢制γ-戊内酯)[J]. J Mol Catal(China)(分子催化), 2018, 32(05): 415–424.
|
| [25] |
Zou Mei-shuai(邹美帅), Guo Xiao-yan(郭晓燕), Yang Rong-jie(杨荣杰), et al. Thermal analysis of viton A /Mg /NaNO3 fuel rich system(氟橡胶/镁/硝酸钠富燃料体系的热分析)[J]. Chin J Expl Propell(火炸药学报), 2009, 32(04): 56–59.
|
| [26] |
Chary K V R, Sagar G V, Naresh D, et al. Characterization and reactivity of copper oxide catalysts supported on TiO2-ZrO2[J]. J Phys Chem B, 2005, 109(19): 9437–9444.
|
| [27] |
An Juan-juan(安娟娟), Wang Shun(王顺), Wang Shan-min(王善民), et al. Hierarchical porous Ni/SAPO-5 catalysts of hydrogenation from naphthalene to decalin(多级孔Ni/SAPO-5萘加氢制十氢萘催化剂)[J]. J Mol Catal(China)(分子催化), 2017, 31(5): 438–445.
|
 2019, Vol. 33
2019, Vol. 33


