甘肃省矿产资源丰富, 据《2010年全国主要矿产资源储量通报》统计, 在已查明的矿产中, 甘肃省资源储量名列全国第1位的矿产有12种, 居前5位的有29种, 居前10位的有58种.其中钨、磷矿分别居第4、第19位[1].有效利用这些资源对于地方经济和科技发展具有重要意义.杂多酸盐作为一类酸碱性与氧化还原性兼具的双功能固体催化剂[2]是近几年来的研究热点[2-16], 其合成原料恰恰需要钨钼钒磷等矿产资源, 此类催化剂在使用过程中达到绿色催化的理念, 但其制备路线繁琐、缺乏安全性, 因为制备过程中需要逐步加入不同组分的原料, 且每一步之后都需使用酸碱调节pH, 因此需要寻找一种绿色便捷的制备方法, 使得催化剂在制备与使用的整个过程都能达到绿色催化的理念.离子液体热合成手段是一种新型的合成先进催化剂材料的方法[17], 其较传统的共沉淀法、水热合成法等具有诸多的优势, 不仅缩减了制备过程的步骤, 还省略了使用酸碱试剂调节pH值的步骤, 制备过程更加精简安全, 符合绿色催化的理念.通过离子热合成法合成的杂多酸盐可以兼具离子液体的优点以及杂多酸盐的催化活性.
环己酮是一种重要的有机化工原料和工业溶剂, 也是制造尼龙、己内酰胺和己二酸的主要中间体.传统的制环己酮的生产工艺主要有两种方法:一是催化脱氢法, 即将环己醇在催化剂存在下脱氢生成酮;二是化学氧化法, 化学氧化法使用的氧化剂如Cr(Ⅵ)和Mn(Ⅴ)类无机氧化剂对环境危害很大[18].近几年, 使用杂多酸催化环己醇生成环己酮的工艺已经成为研究热点[12],因此, 以杂多酸盐为催化剂、H2O2为氧化剂的新型反应工艺具有环境友好、生产成本低廉等优点, 是一类较有前景的环己酮制备工艺.我们利用离子热合成法制备具有特定形貌的磷仲钨酸铯杂多酸盐为催化剂, H2O2为氧化剂, 用于催化环己醇生成环己酮评估该催化剂性能, 旨在实现绿色制备催化剂工艺和提高催化剂的催化活性.
1 实验部分 1.1 主要试剂N-甲基咪唑(C4H6N2)、仲钨酸铵((NH4)6- H2W12O42·xH2O), AR, 阿拉丁;溴代正丁烷(C4H9Br), AR, 麦克林;乙酸乙酯(C4H8O2), AR, 天津市北联精细化学品开发有限公司;磷酸(H3PO4), AR, 天津市恒信化学试剂制作有限公司;碳酸铯(Cs2CO3), AR, 萨恩化学技术有限公司;环己醇(C6H12O), AR, 天津市凯信化学工业有限公司;过氧化氢(H2O2), AR, 天津市大茂化学试剂厂;环己酮((CH2)5CO), AR, 天津市致远化学试剂有限公司;乙腈(C2H3N), AR, 国药集团化学试剂有限公司.
1.2 离子液体的制备离子液体溴代1-正丁基-3-甲基咪唑([bmim]Br)的制备参照文献[19].称取250 g溴代正丁烷和100 g N-甲基咪唑置于50 mL的三口烧瓶中, 在水浴锅50 ℃以下搅拌并冷却回流5 h, 反应结束后, 将三口烧瓶移出水浴锅, 静置待温度降至室温, 将溶液移至烧杯并加入50 mL乙酸乙酯, 使用玻璃棒搅拌均匀, 随后将此溶液迅速移入分液漏斗静置, 下层黏液即为所需产物.用乙酸乙酯洗涤3次后, 放入干燥箱在80 ℃下干燥5 h, 即可得到所需离子液体, 其颜色呈淡黄色.
1.3 催化剂的制备表 1将不同物料的量分别加入到6个安装在油浴锅上的三口烧瓶中(50 mL), 在60 ℃温度下搅拌并冷却回流5 h后, 立即移入50 mL晶化釜中, 在真空干燥箱150 ℃温度下反应72 h, 反应结束后取出晶化釜并静置降温至室温, 分别用去离子水和无水乙醇进行洗涤过滤, 洗涤次数为3次, 之后在80 ℃下干燥8 h[20], 干燥后取出并研磨即得到白色粉末, 所得样品1~5号为离子液体热合成法合成的磷仲钨酸铯杂多酸盐, 分别记作为: CsPW’-100、CsPW’-80、CsPW’-60、CsPW’-40、CsPW’-20. 6号为水热合成法合成的磷仲钨酸铯杂多酸盐, 记作: CsPW’-W.
| 表 1 合成催化剂各组分的量 Table 1 Amount of each component of the synthesis catalyst |
样品红外测试采用美国的Nicolet Avatr360型傅立叶红外光谱, KBr压片, 扫描3次, 测试范围为500~4000 cm-1. XRD测试采用日本岛津XRD-6000衍射仪, 扫描范围为5°~60°. SEM测试采用日本电子光学公司的JSM-6701F冷场发射型扫描电镜.使用Quantachrome, Autosorb-iQ仪器在-196 ℃下通过氮气物理吸脱附实验对样品进行比表面积以及孔径分布的测试, 在测试之前, 需将催化剂在真空中于300 ℃下脱气10 h.
1.5 催化性能评价将装有磁子的50 mL两口圆底烧瓶安装于油浴锅上, 称取2.02 g(0.02 mol)环己醇, 乙腈溶剂5 mL, 催化剂0.2 g于圆底烧瓶中, 当油浴锅温度为70 ℃时, 量取8.1 mL(0.08 mol)双氧水置于恒压漏斗中并在20 min内滴入反应体系, 搅拌反应8 h.反应结束后, 将液相反应产物冷却至室温, 用TG18G台式高速离心机在转速为6000 r/min离心2 min, 此时催化剂已经沉到离心管的底部, 将溶液倒入分液漏斗中, 静置到液体分层.上层为有机相, 下层为水相, 取上层滤液进行气相色谱GC7890Ⅱ分析.分析条件: SE-30毛细管柱(0.53 mm×1 μm×50 m), 高纯度氮气(体积分数99.99%, 压力: 0.1 MPa)为载气, 进样量为0.2 μL, FID检测:柱温140 ℃, 进样口温度260 ℃, 检测器温度280 ℃.采用分析方法为面积归一法.环己醇转化率CNOL、环己酮选择性SCYC的具体计算公式如下:
| $ \begin{array}{l} {{\rm{C}}_{{\rm{NOL}}}}(\% ) = \left( {1 - \frac{{{\rm{ cyclohexanol}}\;{\rm{in}}\;{\rm{product }}}}{{{\rm{ cyclohexanol}}\;{\rm{in}}\;{\rm{reactant }}}}} \right) \times 100\% \\ {{\rm{S}}_{{\rm{CYC}}}}(\% ) = \frac{{{\rm{ cyclohexanone}}\;{\rm{in}}\;{\rm{product }}}}{{{\rm{ cyclohexanol}}\;{\rm{in}}\;{\rm{reaction }}}} \times 100\% \end{array} $ |
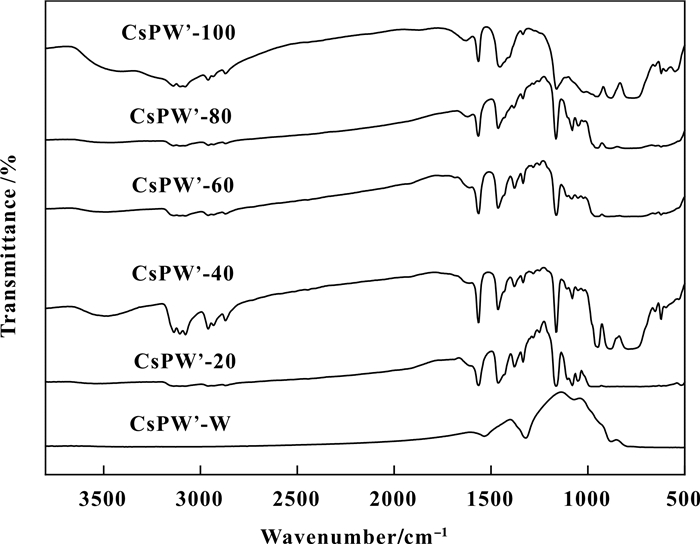
图 1为水热合成法与离子热合成法合成的一系列磷仲钨酸铯杂多酸盐的红外光谱分析图, 由图 1可知, 两种合成方法合成的产物均在1634、1162、956、890、797 cm-1处出现特征吸收峰, 这4种峰为磷钨酸铯杂多酸盐的特征峰[12], 其中1634 cm-1处的特征峰归属于水的-OH的对称和反对称伸缩振动峰, 1162 cm-1位置出现的特征峰属于P—O键的伸缩振动峰;952 cm-1位置出现的特征峰属于W=O对称伸缩振动峰;890位置和797 cm-1位置分别为W—Ob—W和W—Oc—W反对称伸缩振动峰[21].以上测试结果表明两种方法合成的催化剂均为磷仲钨酸铯杂多酸盐.然而不同的是离子热合成的磷仲钨酸铯杂多酸盐在3149 cm-1处出现特有的特征峰, 此特征峰归属于有机配体[Bmim]+的伸缩振动峰[22], 表明溴代1-正丁基-3-甲基咪唑([bmim]Br)离子液体有机配体[Bmim]+与磷仲钨酸铯杂多酸盐能够有效结合, 且CsPW’-40催化剂与CsPW’-100在3149 cm-1的特征峰最为明显, 这是因为当离子液体占比为20时, 离子液体占比还很小, 对催化剂的峰值影响较小, 所以CsPW’-20催化剂的红外光谱图与CsPW’-W相似, 而CsPW’-40催化剂中离子液体占比已比较多, 所以对于离子液体有机配体[Bmim]+的伸缩振动峰表现明显, 再随着离子液体占比的增多, 离子液体与催化剂的结合趋于稳定, 当合成催化剂的溶剂全部为离子液体时, 离子液体占比最多, 所以催化剂在3149 cm-1的特征峰更明显.相比较而言, CsPW’-60与CsPW’-80催化剂的离子液体与杂多酸盐的结合最为稳定.
|
图 1 不同种磷仲钨酸铯盐的FTIR图 Fig.1 FTIR spectra of cesium salts of different phosphorous paratungstates |
图 2为水热合成法与离子热合成法合成的不同磷仲钨酸铯杂多酸盐的XRD图.由图 2中可以看出6种催化剂均在2θ为7°~10°、14°~16°、25°~32°、46°~51°处出现特征衍射峰, 这是磷钨酸铯杂多酸盐的结构特征衍射峰[23], 说明合成了目标催化剂, 但随着离子占比的增加, 衍射峰的强度都渐渐减弱, 衍射峰变低, 这是因为峰值的大小取决于结构中的含量, 随着离子液体含量的增加, 使得杂多酸盐其他含量相对减少.但CsPW’-80催化剂在2θ=25°~32°的峰值都比其他离子热合成的催化剂在2θ=25°~32°处峰值明显, 这是因为离子占比在80%能最好的保证杂多酸盐的结构, 这也是CsPW’-80催化剂催化性能最好的原因之一.

|
图 2 不同磷仲钨酸铯杂多酸盐的XRD图 Fig.2 XRD patterns of cesium heteropolyphosphates with different phosphorous paratungstates |
催化剂CsPW’-100、CsPW’-80、CsPW’-60、CsPW’-40、CsPW’-20、CsPW’-W的SEM图分别如图 3(a、b、c、d、e、f)所示.由图可以看出CsPW’-W催化剂呈现球形的形貌, CsPW’-20催化剂的形貌与CsPW’-W催化剂的形貌相似, CsPW’-80、CsPW’-60、CsPW’-40催化剂均有块状型的形貌, 且随着离子液体占比的增加, 催化剂颗粒越小, 从(b)中可以清晰的看出CsPW’-80催化剂呈六棱台形貌. CsPW’-100催化剂虽然也有块状结构, 但明显粘连严重.主要原因在于当离子液体占比太小时, 不足以影响到催化剂成晶型, 而离子液体占比太大时, 因离子液体粘度大, 使得在合成催化剂时, 会出现催化剂粘合的情况.

|
图 3 磷仲钨酸铯杂多酸盐的SEM图 Fig.3 SEM image of cesium heteropoly phosphite |
不同催化剂的比表面积、孔径等结构参数见表 2.从表 2可以看出, CsPW’-80催化剂的比表面积比CsPW’-W催化剂的要小一半左右;两种催化剂的总孔体积相差较小, CsPW’-80催化剂的总孔体积比CsPW’-W催化剂的小0.4 cm3·g-1左右.主要原因在于离子液体与水作为溶剂在合成催化剂时, 会出现催化剂粘合的情况, 会堵塞部分孔道.
| 表 2 不同催化剂的结构参数 Table 2 Structural parameters of different catalysts |
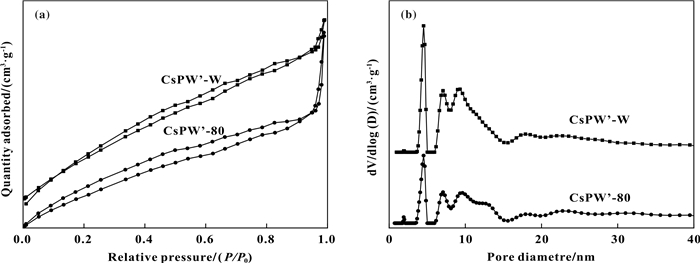
图 4中(a)为CsPW’-W催化剂与CsPW’-80催化剂的N2吸附-脱附等温线, (b)为CsPW’-W催化剂与CsPW’-80催化剂的孔径分布图.由图 4中(a)可知, CsPW’-W催化剂与CsPW’-80催化剂的N2吸附-脱附等温线属于典型的Ⅳ型等温线, 对应含中孔, 即所制催化剂为介孔材料;从图 4(b)也可以看出, CsPW’-W催化剂和CsPW’-80催化剂孔径基本为介孔, 且介孔孔径大小为4.5 nm最多、其次是7、然后是9.5 nm等. CsPW’-80催化剂的介孔数量要比CsPW’-W催化剂的少, 这可能是因为离子液体进入孔道造成部分孔径堵塞[22], 使得孔数量减少, 比表面积与总孔体积都有所减少, 此结论与表 2中的数据相吻合.
|
图 4 催化剂的N2吸附-脱附等温线(a)及孔分布(b) Fig.4 N2 adsorption-desorption isotherm of catalyst (a) and aperture distribution (b) |
表 3为不同催化剂在最优条件下的催化性能评价结果: 1~5号为不同离子液体占比下合成的磷仲钨酸铯杂多酸盐催化剂的催化性能;6号为水热合成法合成的磷仲钨酸铯杂多酸盐催化剂的催化性能.由表 3可以看出, 在最优条件下, CsPW’-80催化剂的催化性能最好.因为当离子液体占比为80%时, 溴代1-正丁基-3-甲基咪唑离子液体有机配体[Bmim]+能与磷仲钨酸铯杂多酸盐有效结合呈现六棱台晶型结构且形貌规整, 同时CsPW’-80催化剂能保持磷仲钨酸铯盐杂多酸盐的结构, 使得所制催化剂兼具咪唑类离子液体稳定性高与耐温的优点和磷钨酸铯盐的催化活性[22-23].但是水与离子液体作为溶剂在合成催化剂时, 会出现催化剂粘合的情况, 故而会造成CsPW’-80表面积降低.综上所述, 通过性能评估可知CsPW’-80催化剂的催化性能最好, 其合成方法中水与离子液体比例是影响催化剂性能的主要原因.在最优条件下:环己醇转化率为100%, 环己酮的选择性为98.5%.
| 表 3 不同催化剂下的催化性能评价结果 Table 3 Comparison of catalytic performance under different catalysts |
将CsPW’-80催化剂用于环己醇生成环己酮反应进行工艺条件优化, 分别改变氧化剂与反应物n(30% H2O2)/n(cyclohexanol)比、反应温度、反应时间与催化剂的质量, 研究这几种因素对反应效果的影响, 从而找到反应的最优条件.各种影响因素对反应的影响如图 5中所示.
|
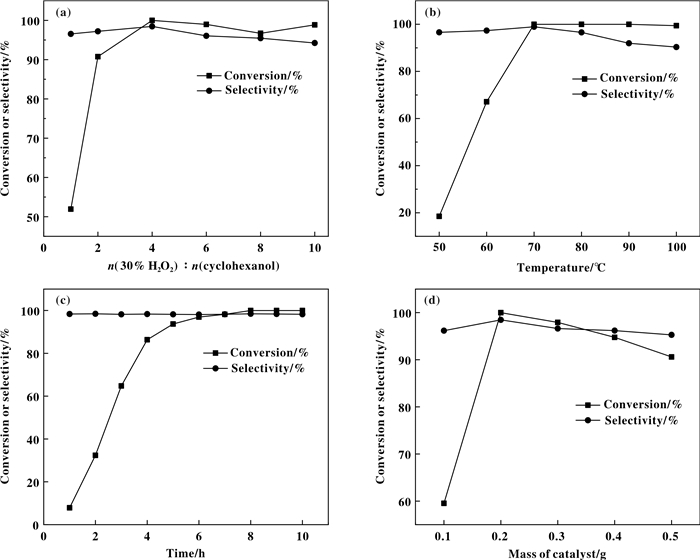
图 5 氧化剂与反应物n(30% H2O2)/ n(cyclohexanol)比对反应的影响(a)、反应温度对反应的影响(b)、反应时间对反应的影响(c)与催化剂质量对反应的影响(d)图 Fig.5 Effect of oxidant and reactant n(30% H2O2) /n(cyclohexanol) ratio on the reaction (a), reaction temperature on the reaction (b), reaction time on the reaction (c) and catalyst amount on the reaction (d) |
图 5中(a)表示氧化剂与反应物n(30% H2O2)/n(cyclohexanol)比对反应的影响, (b)表示反应温度对反应的影响, (c)表示反应时间对反应的影响, (d)表示催化剂质量对反应的影响.由图 5中(a)可知, 最佳氧化剂与反应物n(30% H2O2):n(cyclohexanol)为4, 相比文献[21]中离子热合成磷酸氧钒催化剂催化环己醇氧化环己醇的最优氧化剂与反应物n(H2O2)/n(cyclohexanol)=6中对H2O2利用率有所提升, 对H2O2利用率达到75%;(b)中可得最佳温度为70 ℃;(c)中可得最优时间为8 h, 且在反应时间的影响中, 环己酮选择性几乎没有变化, 所以在足够的时间内, 环己醇转化率达到100%;(d)中可得最优催化剂质量为0.2 g.由图 5中4图综合可得随着影响因素的变化, 反应中环己酮的选择性变化范围在90.3%~98.5%之间, 选择性持续保持在90.0%以上, 相比文献[12-22], 反应选择性变化幅度小, 因此CsPW’-80催化剂稳定性好, 更耐温.
由2.2.1中表 3与图 5综合可得催化剂催化环己醇氧化生成环己酮反应中的最优条件为:合成催化剂溶剂最佳离子液体积占比=80%, 溶剂5 mL, 氧化剂与反应物n(30% H2O2):n(cyclohexanol)=4, 反应温度70 ℃, 反应时间8 h.
3 结论 3.1利用离子热合成法制备得到六棱台形貌的介孔材料磷仲钨酸铯杂多酸盐的催化剂, 实现了杂多酸盐催化剂的绿色制备工艺.通过FTIR分析、XRD分析、SEM分析与BET分析可知, 合成方法能将溴代1-正丁基-3-甲基咪唑([bmim]Br)离子液体的有机配体[Bmim]+有效引进催化剂中, 使得所制催化剂兼具咪唑类离子液体稳定性高与耐温的优点与磷钨酸铯盐的催化活性, 增强了催化剂高效性, 从而提高催化经济性.
3.2实验表明, 磷仲钨酸杂多酸盐催化剂催化氧化环己醇生成环己酮的最优条件为以CsPW’-80为催化剂、溶剂乙腈5 mL、氧化剂与反应物n(30% H2O2):n(cyclohexanol)=4、在反应温度70 ℃、反应时间8 h的条件下, 环己醇转化率为100.0%, 环己酮的选择性为98.5%.
| [1] |
Zhang Yong-xia(张永霞), Xie Jian-qiang(谢建强), Liu Dong-xiao(刘东晓). Analysis of the current status of important mineral resources conservation and comprehensive utilization in Gansu Province(甘肃省重要矿产资源节约与综合利用现状分析)[J]. Gansu Geology(甘肃地质), 2019, 2019(Z1): 9–15.
|
| [2] |
Bi L H, Wang E B, Peng J, et al. Crystal structure and replacement reaction of coordinated water molecules of the heteropoly compounds of sandwich-type tungstoarsenates[J]. Inorg Chem, 2000, 39(4): 671.
|
| [3] |
Wen Lang-you(温朗友). New progress in the research of solid heteropoly acid catalysts(固体杂多酸催化剂研究新进展)[J]. Petrochem Indus(石油化工), 2000, 29(1): 49–55.
|
| [4] |
Zhang Z, Lin Q, Kurunthu D, et al. Synthesis and photocatalytic properties of a new heteropolyoxoniobate compound:K10[Nb2O2(H2O)2][SiNb12O40)·12H2O[J]. J Am Chem Soc, 2011, 42(32): 6934–6937.
|
| [5] |
Masahiro Egi, Megumi Umemura, Takuya Kawai, et al. Heteropoly compound catalyzed synthesis of both Z-and E-α, β-unsaturated carbonyl compounds[J]. Angew Chem Int Ed, 2011, 50(51): 12197–12200.
|
| [6] |
Fabrizio Cavani. Heteropoly compound-based catalysts:A blend of acid and oxidizing properties[J]. Catal Today, 1998, 41(1): 73–86.
|
| [7] |
Nowińska K, Fórmaniak R, Kaleta W, et al. Heteropoly compounds incorporated into mesoporous material structure[J]. Appl Catal Gen, 2003, 256(1): 115–123.
|
| [8] |
Okuhara T. New catalytic functions of heteropoly compounds as solid acids[J]. Cheminform, 2002, 34(1): 167–176.
|
| [9] |
Guixian Li, Qi Zhang, Weiguo Fang, et al. Lonothermal synthesis and selective oxidation performance of a crytalline vanadium phosphate catalyst[J]. Energy Environ Focus, 2015, 4(4): 301–306.
|
| [10] |
Guixian Li, Yong Ding, Jianming Wang, et al. New progress of keggin and wells-dawson type polyoxometalates catalyze acid and oxidative reactions[J]. J Mol Catal A Chem, 2007, 262(1/2): 67–76.
|
| [11] |
Yang H W, Qi X F, Wen L, et al. Regioselective mononitration of aromatic compounds using keggin heteropolyacid anion based Brønsted acidic ionic salts[J]. Indus & Eng Chem Res, 2011, 50(19): 58–63.
|
| [12] |
Mao Li-ping(毛丽萍), Yu Yi-cong(玉轶聪), Shi Yan(史妍), et al. Synthesis of cyclohexanone catalyzed by Keggin type Sn monosubstitutedheteropoly acid salt(Keggin型Sn单取代的杂多酸盐催化合成环己酮)[J]. Fine Chem(精细化工), 2017, 34(3): 300–306.
|
| [13] |
Li Gui-xian(李贵贤), Shi Yan(史妍), Yu Yi-cong(玉轶聪), et al. Catalytic oxidation of cyclohexane hydroxide by cerium phosphorus molybdenum vanadium heteropoly acid salt(铈磷钼钒杂多酸盐催化过氧化氢氧化环己烷)[J]. Fine Chem(精细化工), 2016, 33(12): 1358–1363.
|
| [14] |
Fan Zong-liang(范宗良), Wei Hui-juan(魏慧娟), Li Gui-xian(李贵贤), et al. Dawson-type phosphoplatinum vanadium heteropolyacid catalyzed synthesis of diphenylmethane(Dawson型磷铂钒杂多酸盐催化合成二苯基甲烷)[J]. Fine Chem(精细化工), 2015, 32(5): 543–547.
|
| [15] |
Li Gui-xian(李贵贤), Zhang Qi(张琪), Ji Dong(季东), et al. Synthesis and application of amorphous vanadium phosphate phosphate catalysts in eutectic mixture system(低共熔混合物体系中合成无定型的磷酸氧钒催化剂及应用)[J]. J Mol Catal(China)(分子催化), 2014, 28(2): 105–111.
|
| [16] |
Zhao Shan(赵鹬), Li Gui-xian(李贵贤), Zhang Qi(张琪). Vanadium phosphate catalyst and its preparation method and use(磷酸氧钒催化剂及其制备方法与用途)[P]. Chinese Invention Patent(中国发明专利), CN201310540657.2, 2013-10.
|
| [17] |
Das S, Heasman P, Ben T, et al. Porous organic materials:Strategic design and structure-function correlation[J]. Chem Rev, 2017, 117(3): 1515–1563.
|
| [18] |
Hoops M D, Ault B S. Matrix isolation study of the photochemical reaction of cyclohexane and cyclohexene with CrCl2O2[J]. J Mol Struct, 2007, 826(1): 36–47.
|
| [19] |
Laali , Kenneth K. Ionic Liquids in Synthesis[J]. Synthesis, 2003, 2003(11): 1752–1752.
|
| [20] |
Lopez-Sanchez J A, Griesel L, Bartley J K, et al. High temperature preparation of vanadium phosphate catalysts using water as solvent[J]. Cheminform, 2003, 34(46): 89–105.
|
| [21] |
Wang Shi-dong(王世栋), Zhao Shan(赵鹬), Zhao Xin-hong(赵新红), et al. Research progress in synthesis and catalytic oxidation performance of vanadyl phosphate catalysts(磷酸氧钒催化剂的合成及催化氧化性能研究进展)[J]. Indus Catal(工业催化), 2019, 124(5): 67–70.
|
| [22] |
He Yun-peng(何云鹏), Guo Gai-juan(郭改娟), Wu Shuang(吴双), et al. Preparation and adsorption properties of H6P2W18O62/MIL-101(Fe) materials(H6P2W18O62/MIL-101(Fe)材料的制备及其吸附性能)[J]. Fine Chem(精细化工), 2019, 36(9): 1911–1915.
|
| [23] |
Ning Jian-mei(宁建梅), Peng Kun(彭坤), Yang Li-xia(杨丽霞), et al. Synthesis of heteroplyacid ionic liquids and their application in clean oxidation(杂多酸型离子液体的合成及在清洁氧化中的应用)[J]. J Petrochem Univer(石油化工高等学校学报), 2015, 28(6): 14–19.
|
 2020, Vol. 34
2020, Vol. 34

