2. 云南省生态环境科学研究院, 云南 昆明 650034
2. Yunnan Research Academy of Eco-Environmental Sciences, Kunming 650034, China
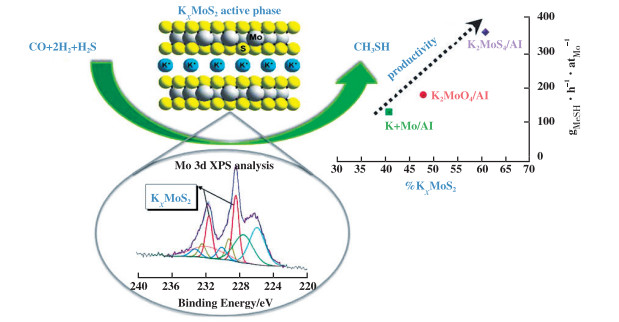
甲硫醇(CH3SH)是一类重要的化工原料, 在医药、农药、饲料和有机材料等领域得到了广泛应用[1-2], 最典型的应用是以CH3SH为原料生产蛋氨酸.[3]蛋氨酸是人体必需氨基酸之一, 人体自身不能产生, 需从动物中摄取.由于甲硫醇和蛋氨酸的合成方法被法国安迪苏、德国赢创、美国诺伟司和日本住友等企业垄断, 国内的蛋氨酸普遍依赖进口.[2-3]甲硫醇合成传统方法是以甲醇(CH3OH)和硫化氢(H2S)为原料, 在钼钨基催化剂上催化合成.[1] Olin等[4]提出CO/H2/H2S一步合成CH3SH的新思路, 反应方程式为CO + 2H2 + H2S → CH3SH + H2O, 该法理论上只生成CH3SH和水, 是一条绿色经济环保的路径, 同时能有效缓解蛋氨酸进口紧缺问题, 近年来成为国内外学者的研究热点[2, 5].
钾钼基催化剂由于具有强抗硫性能和高CH3SH选择性, 成为CO/H2/H2S一步法合成CH3SH研究最高效和最广泛的材料[2, 6]. 该体系普遍存在转化率和选择性较低的问题(CO转化率约为30%~50%, CH3SH选择性约为40%~50%)[2, 7], 其原因在于对钾钼基催化剂上活性中心缺乏深入认知, 难以有效调控活性物种微观结构, 实现CH3SH定向合成, 从而限制该法的进一步发展[1-2, 5-6]. 研究人员提出钾钼基催化剂上存在3类活性相: 纯MoS2相、K修饰型MoS2相和K插入型MoS2相(下文依次简称为MoS2相、K-MoS2相和KxMoS2相), 并认为活性相和甲硫醇定向合成密切相关. 我们将对CO/H2/H2S一步法合成CH3SH催化剂上活性相的研究现状、作用机理及活性相合成等关键因素进行综述, 并对一步法合成CH3SH的未来发展进行了展望.
1 一步法合成CH3SH活性相种类 1.1 “K-S-Mo”活性相深入认知活性相是实现钾钼基催化剂高性能的前提和关键. 杨意泉团队[6, 8]首先关注了钾钼基催化剂的活性物种. 通过制备系列催化剂并对比其XRD衍射峰, 发现K2CO3/MoS2/Al2O3催化剂在衍射角为29.8°和30.8°处出现了新的衍射峰[6]. 经过与系列催化剂比较, 如Al2O3、K2CO3、MoS2、K2CO3/Al2O3、MoS2/Al2O3和K2CO3/MoS2, 推测出这两个峰来源于K2CO3和MoS2相互作用产生的“K-S-Mo”微晶相. 建立反应活性与催化剂的关系后, 推测“K-S-Mo”相为活性中心. 活性相的形成机理为K通过硫桥转移电子至Mo上, 当CO分子吸附到Mo表面时, 电子会反馈给CO, 增强Mo-C键同时削弱了C-O三键[6, 8], 从而增强反应活性.
之后, 相关课题组对比研究了(Mo/SiO2、MoCo/SiO2、KMo/SiO2和K-MoCo/SiO2)催化剂, 通过CO-TPD、电子自旋共振(ESR)和XPS等表征技术证明“K-S-Mo”相结构中存在两类活性物质(低价态硫(如S22-)和高价态钼(Mo5+)), 并提出了更为详细的反应机理[9]. 钾的添加有助于生成更多低价硫物种, 促进K-S或K-SH键的形成, 该活性物种有利于CO的非选择性插入形成COSads和HOCSads中间体, 进一步加氢促进CH3SH的生成[9]. 上述结果虽然说明了Mo/SiO2催化剂中助剂K和Co对合成CH3SH催化性能提升的原因, 但对活性中间物种(COSads和HOCSads)的检测缺乏实验依据, 需要进一步深入探究.
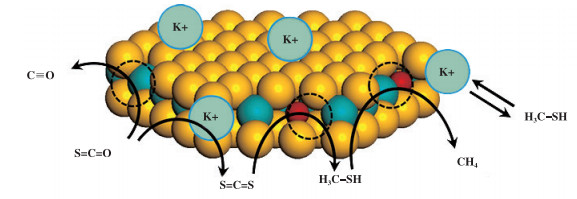
1.2 MoS2相和K-MoS2相钾钼基催化剂活性相结构的认知吸引了大量研究团队对一步法合成CH3SH的关注. Lercher课题组[10-11]提出钾钼基催化剂上可能存在的MoS2相和K-MoS2相与催化剂高性能密切相关. 首先通过制备硫化的K2MoO4/SiO2催化剂, 并对原料使用进行特定设计, 即先采用CO和硫磺合成COS, 接着以其为原料(COS/H2/H2S)合成CH3SH, 结果表明CO和COS转化率均达到100% [12]. 其次通过设计H2S/COS和H2/COS的比例进行活性评价实验, 并结合Raman、XRD和NO脉冲技术提出K-MoS2相的存在. XRD结果只观察到MoS2相的衍射峰, 说明K与MoS2相的作用是非结构性连接, 即K修饰在MoS2相的边缘位点上, 如图 1所示. 另外, 研究人员通过原位Raman表征空气氧化后的样品, 发现了MoO3物种, 由此推测纯MoS2相的存在[10]. 基于反应产物中的新物种-二硫化碳(CS2)的存在, 研究者提出了不同活性相上的反应机理, 即MoS2相有助于COS加氢分解为CO和H2S, 不利于CH3SH的生成; K-MoS2相有助于COS歧化成CS2及CS2进一步加氢生成CH3SH[10-11]. 虽然这些研究大大推进了一步法合成CH3SH反应催化剂上“K-S-Mo”活性相的理论认识, 但是缺乏直接证据证明K-MoS2相和MoS2相的存在. 值得注意的是, Lercher课题组采用CO、硫磺、H2和H2S为原料, 所获CO和COS转化率可以达100%. 结合目前以CO为原料所获CO转化率较低以及国内硫磺产品生产过剩和价格低廉的现状, 以CO、硫磺、H2和H2S为原料合成CH3SH显然具有更突出的工业化应用前景.
|
图 1 K-MoS2相的构型图[11](黄色球为硫, 蓝色球为钼, 红色球为钴) Fig.1 Schematic illustration of K-decorated MoS2[11](yellow: S, blue: Mo, red: Co) |
K-MoS2相与MoS2相的结构均为低价态硫(S2-和S22-)和低价态钼(Mo4+), 与杨意泉课题组[11]“K-S-Mo”相结构(低价态S22-和高价态Mo5+)相矛盾, 难以明确一步法合成甲硫醇反应的催化活性中心. 基于此, 昆明理工大学罗永明课题组[13]采用不同碱金属有效调控了Mo4+(S)物种的含量, 并建立了Mo4+(S)物种含量与CH3SH选择性之间的构效关联. 结果显示CH3SH选择性与Mo4+(S)物种的相对含量存在正向关联, 即Mo4+(S)物种的相对含量越高, CH3SH选择性越高[13]. 该结果为“K-S-Mo”活性相中有低价态钼(Mo4+)和低价态硫(S2-和S22-)的K-MoS2相与MoS2相提供了有力的证据. Lamonier团队[14]认为MoS2相的Mo4+相对含量与CO转化率存在负相关性. 他们制备了系列不同前驱体的钼基催化剂, 并结合XPS技术得出MoS2相的相对含量越高, CO转化率越低的结论. 综上可见钾钼基催化剂体系中活性相结构与催化剂性能之间的关联没有一致的结论. 这种争议有两个方面的原因, 第一, 在建立构效关系时, 罗永明和Lamonier团队[13-14]没有明确MoS2相中的具体物种, XPS结果无法准确区分K-MoS2相与MoS2相的含Mo4+的物种. 由Gutiérrez等[10]的研究可知, K-MoS2相的Mo4+物种可极大提高CH3SH的产率, 而MoS2相的Mo4+物种不利于CH3SH的生成. 因此, 基于XPS结果得出的Mo4+物种含量与催化性能的构效关系难以明确活性相. 第二, 该结果说明控制CO转化和CH3SH合成的活性相不一样. 由反应方程式可知, CO先和H2S反应生成COS, COS进一步歧化或加氢生成CH3SH[15]. 这表明一步法合成CH3SH为两步串联反应, 前者在MoS2相上发生, 后者则主要发生在K-MoS2相. 综上可知, 这种矛盾现象是合理的, 即XPS结果中Mo4+物种的相对含量越高可能导致CO转化率越低和CH3SH选择性越高.
1.3 KxMoS2相除了上述K-MoS2相与MoS2相, 研究人员发现钾钼基催化剂上存在KxMoS2相[10, 14]. Gutiérrez等[10]用XRD表征硫化后的K2MoO4/SiO2催化剂, 发现衍射角为10.3°处的衍射峰归属于KxMoS2相. 但反应一段时间后, XRD检测不到该结晶相, 由此认为KxMoS2相并非一步法合成CH3SH的活性相. Lamonier课题组[14]制备了硫化的K/Al2O3、Mo/Al2O3和K-Mo/Al2O3催化剂, 并通过XPS技术发现K-Mo/Al2O3催化剂上电子结合能在228.9 eV处的MoS2相, 同时也发现了228.4 eV处新的峰. 电子结合能的细微差别表明K的加入引起了电子转移和结构的变化, K有可能插入二硫化钼的层中间, 形成了KxMoS2相. 由KxMoS2相的相对含量与CH3SH产率之间的正向线性关联, 可证明KxMoS2相是一步法合成CH3SH的反应活性相, 如图 2所示[14].
国内外学者对于KxMoS2相是否为CH3SH合成反应的活性相存在较大的争议. 经过仔细对比上述两课题组制备催化剂的过程, 发现在硫化温度、时间、气氛、压力以及反应压力上存在明显差别. 例如, Gutiérrez等[10]所用工作态的催化剂主要在10% H2S/H2气氛和3 MPa压力下, 经400 ℃硫化12 h获得, 催化性能评价主要在3 MPa下进行; 而Lamonier团队所用工作态的催化剂首先在纯H2S气氛中250 ℃硫化1 h, 随后在25% H2S/H2气氛和常压下, 经350 ℃硫化1 h获得, 催化性能评价在1 MPa下进行[14]. 由此可见, 钾钼基催化剂制备过程中的硫化过程和反应条件对催化剂活性相的种类和性质有着不可轻忽的作用.
2 控制活性相的关键因素 2.1 硫化过程和反应条件鉴于催化剂制备过程中的硫化过程和反应条件对活性相的重要影响, 研究人员对硫化过程中的温度、时间、气氛、压力以及反应过程的压力和温度等进行了深入研究. 钾钼基催化剂广泛用于合成气制备混合醇的研究, 但该领域尚无KxMoS2相存在的报道. 混合醇领域中硫化过程和活性反应普遍在7~9 MPa的压力下进行, 而合成CH3SH所需硫化和反应压力为1~3 MPa, 因此推测硫化和反应压力会影响KxMoS2相的生成. Hensen课题组[16]利用原位XPS技术在1 MPa压力下观测钾钼基催化剂的活性物种, 发现硫化后的催化剂上普遍存在KxMoS2相, 但是在350 ℃和1 MPa反应数小时后, KxMoS2相逐渐减少并消失. 由此说明高温高压下KxMoS2相不稳定, 难以长时间存在, 同时直接有力地证明了反应压力和反应时间对KxMoS2相形成的重要影响.
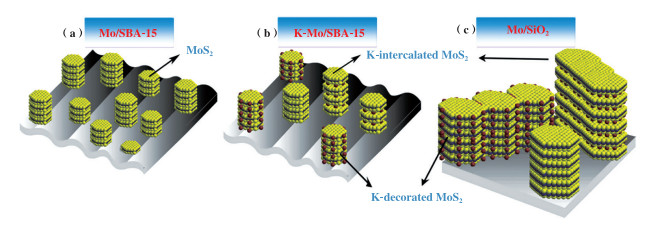
除了硫化压力和反应压力, 硫化温度和反应温度也会影响KxMoS2相的形成和转变. 罗永明课题组[17]关注了硫化温度和反应压力对MoS2相结构相变的影响. 当硫化温度为280 ℃及硫化和反应压力都为0.2 MPa时, 采用XRD表征反应前后的催化剂, 发现反应前后的样品中均存在KxMoS2相. XPS和高倍电镜发现同一催化剂中K-MoS2相和MoS2相皆存在. 另外, 高脚环形暗场扫描透射电镜从分子原子水平证实KxMoS2相、K-MoS2相和MoS2相均存在于反应过程中, 这些物种均为一步法合成CH3SH的活性相[17], 如图 3所示. 综上可知, 硫化过程和反应条件对活性相的生成有直接且关键的作用, 在高温高压的硫化和反应条件下, 钾钼基催化剂主要存在K-MoS2相和MoS2相; 在低温低压的硫化和反应条件下, 钾钼基催化剂上同时存在KxMoS2相、K-MoS2相和MoS2相.
|
图 3 钼基催化剂上3类MoS2活性相的分布图[17] Fig.3 Schematic illustration of distributions of three kinds of MoS2 over Mo based catalysts[17] (黄色球为硫, 蓝色球为钼, 红色球为钾) (yellow: S, blue: Mo, red: K) |
碱金属对MoS2相结构具有不可轻忽的调控作用. 纯MoS2相是一种典型的层状结构, 层与层之间由弱的范德华力结合, 而每一层则由强S-Mo-S化学键结合. MoS2相上存在大量的配位不饱和位点(Mo-CUS), 即当连接Mo的S被脱除, 便会暴露出缺S的空位. 当MoS2相处于CO/H2/H2S反应体系中时, CO分子在Mo-CUS上发生非解离吸附并活化, H2和H2S发生解离性吸附活化[17]. 因此, Mo/SBA-15催化下的产物主要以COS形成存在, 几乎不产生CH3SH; 加入K后, K-Mo/SBA-15催化下的产物以CH3SH为主, 说明K对MoS2相的性质产生了重要的影响[11, 13, 17]. 由文献可知[10, 17], K可自由分散在纯MoS2相表面, 理论上可能发生三种相互作用, 一为K离子沉积在MoS2相基平面或载体表面, 形成纯MoS2相; 二为K修饰在MoS2相的边缘位点上, 形成K修饰型MoS2相; 三为K插入到MoS2相的弱范德华层中间, 形成K插入型MoS2相. 这些相的形成既取决于K的覆盖度, 也取决于硫化过程和反应条件的影响. 罗永明课题组[7]采用超声诱导浸渍法快速合成不同K覆盖度的钾钼基催化剂, 并对比了硫化过程的影响, 发现K覆盖度决定着K-MoS2相的形成, 而硫化过程决定着KxMoS2相的形成. 另外, K-Mo/SBA-15催化剂在400 ℃硫化12 h后, 无论K覆盖度为多少, 该催化剂上只有MoS2相和K-MoS2相, 无KxMoS2相.
K改性MoS2催化剂最早应用于合成气制备混合醇, 纯MoS2基催化剂主要生成碳氢化合物, K改性MoS2催化剂生成混合醇, 说明K可稳定C-O键[18-19]. Gutirrez等[20]对比探究了加K和不加K催化剂反应产物的变化趋势, 推测K可稳定吸附中间物种COS. 罗永明课题组[7]通过对不同K负载量的钾钼基催化剂进行H2-TPR实验, 直接证实K可以稳定吸附COS. 随着K负载量的增加, TPR还原峰往高角度方向移动; 继续增加K负载量, TPR还原峰反而往低角度方向移动. 由于钾钼基催化剂在H2-TPR上的还原峰表示H2对MoS2相上表面活性硫的消耗, 因此还原温度可代表MoS2相上Mo-S键的强度. 随着K负载量的增加, Mo-S键增强; 当K负载量达到K/Mo=2后继续增加, Mo-S键反而减弱, 总体呈现火山曲线关系. 结合催化剂的活性实验发现CH3SH的选择性与Mo-S键强度的变化一致, 均呈现火山曲线关系. 由COS-TPD和密度泛函理论计算结果可知, 当Mo-S键强度太弱时, 不足以活化COS; 当Mo-S键强度太强时, COS分子中C-S键容易断裂生成CO2和H2S等副产物, 说明COS与Mo-S键强度是实现CH3SH合成的关键. K可调控Mo-S键至适当的强度, 以活化和稳定中间物种COS, 进一步加氢生成CH3SH[7].
尽管K对钾钼基催化剂上活性相的生成及在CH3SH合成中的作用机理已取得重要进展, 但是无法从分子原子水平直接观察到K在MoS2相上的位置. 高角环形暗场扫描透射电镜(HAADF-STEM)技术可成像观察绝大多数金属. 由于K为轻金属, 其在HAADF像中散射电子强度非常低, 通常无法直接观察到[21]. 因此, 需要采用更多先进的物理化学表征技术观察K在MoS2相上具体位置, 为K对钾钼基催化剂的调控作用提供直接而有力的证据. 例如, 环形明场(ABF)像衬度与Z1/3成正比, 因而对轻金属元素的测定更为敏感; 电子能量损失谱(EELS)不仅可以提高电子显微镜的衬度和分辨率, 还能提供催化剂样品元素的原子尺度分布图, 特别是对轻金属元素较为敏感[21].
此外, 载体也会影响KxMoS2相和K-MoS2相的形成, 进而影响CH3SH合成的催化活性. 罗永明比较了SBA-15和SiO2载体制备的钾钼基催化剂, 发现SBA-15负载的催化剂与MoS2相有较弱的相互作用, 容易形成K-MoS2相; SiO2载体与MoS2相作用力较强, 容易形成KxMoS2相, K-MoS2相对合成CH3SH具有更好的催化性能. 由于SBA-15负载的催化剂上活性相具有更高的分散程度, 因此很难获得载体影响CH3SH合成的直接证据. 如何保持在相同分散度情况下, 比较载体对K-MoS2相和KxMoS2相形成的影响是合成CH3SH领域的一大难点.
3 结论和展望钾钼基催化剂是一步法合成CH3SH应用最广泛的催化剂. MoS2相特有的层状结构和K的物理化学特性引发了K和MoS2之间复杂的相转化行为, 即MoS2相、K-MoS2相和KxMoS2相. 催化剂活性相的形成取决于硫化过程、反应条件和K的调控作用. 未添加K的催化剂几乎不产生CH3SH, 加入K后大大提高了CH3SH生成. K可调控MoS2表面的Mo-S键强度以稳定活化COS中间物种, 进一步加氢生成CH3SH. 由于缺乏直接证据, 一步法合成CH3SH催化剂上活性相的存在与种类一直存在争议. 因此在未来的研究中, 一方面需要更系统地探究硫化过程(硫化温度、压力、时间和气氛等)和反应条件(反应温度、压力和时间)对活性相合成的影响; 另一方面需要结合更先进的物理化学表征手段(如ABF像和EELS等)从分子原子水平认知活性相的结构和性质以及K在MoS2相上的具体位置和作用; 针对催化剂上活性相的清楚认识, 对开发高温高压、高毒性易爆气氛下的原位表征技术提出了更高的要求.
| [1] |
Liu Pan(刘攀), Lu Ji-chang(陆继长), Xu Zhi-zhi(许志志), et al. Effect of K cation on the one-step synthesis of CH3SH using molybdenum based catalysts(钾离子对一步法制甲硫醇钼基催化剂的影响)[J]. Chem Ind Eng Prog(化工进展), 2018, 37(7): 2644–2648.
|
| [2] |
Xu Zhi-zhi(许志志), Lu Ji-chang(陆继长), Liu Pan(刘攀), et al. Development in the methanthiol by high H2S-Containing syngas(高硫合成气法合成甲硫醇研究进展)[J]. J Mol Catal(China)(分子催化), 2017, 31(4): 390–400.
|
| [3] |
Tan Sheng-jun(谭圣君), Shao You-yuan(邵友元), Li Wei(李卫). Research status of methionine and its app-lication prospects(蛋氨酸的研究现状及其应用前景)[J]. J Hubei Univer Technol(湖北工业大学学报), 2006, 21(6): 66–71.
DOI:10.3969/j.issn.1003-4684.2006.06.019 |
| [4] |
Olin J, Buchholz B, Loev B, et al. Process for pre-paration of methyl mercaptan[P]. US: 3070632, 1962.
|
| [5] |
Barraul J, Boulinguiezb M. Synthesis of methyl mercaptan from carbon oxides and H2S with tungsten-alumina catalysts[J]. Appl Catal, 1987, 33: 309–330.
DOI:10.1016/S0166-9834(00)83064-X |
| [6] |
Yang Y Q, Dai S J, Yuan Y Z, et al. The promoting effects of La2O3 and CeO2 on K2MoS4/SiO2 catalyst for methanthiol synthesis from syngas blending with H2S[J]. Appl Catal A: Gen, 2000, 192: 175–180.
DOI:10.1016/S0926-860X(99)00342-7 |
| [7] |
Lu J C, Fang J, Xu Z Z, et al. Facile synthesis of few-layer and ordered K-promoted MoS2 nanosheets supported on SBA-15 and their potential application for heterogeneous catalysis[J]. J Catal, 2020, 385: 107–119.
DOI:10.1016/j.jcat.2020.03.017 |
| [8] |
Yang Yi-quan(杨意泉), Wang Qi(王琪), Dai Shen-jun(戴深峻), et al. Preparation of Mo-S-based catalysts for methanthiol synthesis from high H2S-containing syngas(高硫合成气制甲硫醇钼硫基催化剂的制备)[J]. Chin J Appl Chem(应用化学), 1999, 16(4): 47–51.
|
| [9] |
Chen A P, Wang Q, Li Q L, et al. Direct synthesis of methanethiol from H2S-rich syngas over sulfided Mo-based catalysts[J]. Mol Catal, 2008, 283: 69–76.
DOI:10.1016/j.molcata.2007.12.014 |
| [10] |
Gutiérrez O Y, Kaufmann C, Hrabar A, et al. Syn-thesis of methyl mercaptan from carbonyl sulfide over sulfide K2MoS4/SiO2[J]. J Catal, 2011, 280: 264–273.
DOI:10.1016/j.jcat.2011.03.027 |
| [11] |
Gutierrez O Y, Kaufmann C, Lercher J A. Synthesis of methanethiol from carbonyl sulfide and carbon disulfide on (Co)K-promoted sulfide Mo/SiO2 catalysts[J]. ACS Catal, 2011, 1: 1595–1603.
DOI:10.1021/cs200455k |
| [12] |
Kaufmann C, Gutierrez O Y, Zhu Y Z, et al. Effect of H2 in the synthesis of COS using liquid sulfur and CO or CO2 as reactants[J]. Res Chem Inter, 2010, 36: 211–225.
DOI:10.1007/s11164-010-0131-8 |
| [13] |
Liu P, Lu J C, Xu Z Z, et al. The effect of alkali met-als on the synthesis of methanethiol from CO/H2/H2S mixtures on the SBA-15 supported Mo-based catalysts[J]. Mol Catal, 2017, 442: 39–48.
DOI:10.1016/j.mcat.2017.08.022 |
| [14] |
Cordova A, Blanchard P, Lancelot C, et al. Probing the nature of the active phase of molybdenum-supported catalysts for the direct synthesis of methylmercaptan from syngas and H2S[J]. ACS Catal, 2015, 5: 2966–2981.
DOI:10.1021/cs502031f |
| [15] |
Lu J C, Liu P, Xu Z Z, et al. Investigation of the reac-tion pathway for synthesizing methyl mercaptan (CH3SH) from H2S containing syngas over K-Mo-type materials[J]. RSC Adv, 2018, 8: 21340–21353.
DOI:10.1039/C8RA03430C |
| [16] |
Yu M, Kosinov N, Haandel L, et al. Investigation ofthe active phase in K-promoted MoS2 catalysts for methanethiol synthesis[J]. ACS Catal, 2020, 10: 1838–1846.
DOI:10.1021/acscatal.9b03178 |
| [17] |
Lu J C, Luo Y M, He D D, et al. An exploration into pot-assium (K) containing MoS2 active phases and its transformation process over MoS2 based materials for producing methanethiol[J]. Catal Today, 2020, 339: 93–104.
DOI:10.1016/j.cattod.2019.01.012 |
| [18] |
Ao M, Pham G H, Sunarso J, et al. Active centers ofcatalysts for higher alcohol synthesis from syngas: A review[J]. ACS Catal, 2018, 8: 7025–7050.
DOI:10.1021/acscatal.8b01391 |
| [19] |
Claure M T, Chai S H, Dai S, et al. Tuning of higher alcohol selectivity and productivity in CO hydrogenation reactions over K/MoS2 domains supported on mesoporous activated carbon and mixed MgAl oxide[J]. J Catal, 2015, 324: 88–97.
DOI:10.1016/j.jcat.2015.01.015 |
| [20] |
Gutirrez O Y, Kaufmann C, Lercher J A. Influence ofpotassium on the synthesis of methanethiol from carbonyl sulfide on sulfided Mo/Al2O3 catalyst[J]. ChemCatChem, 2011, 3: 1480–1490.
DOI:10.1002/cctc.201100124 |
| [21] |
Jia Zhi-hong(贾志宏), Ding Li-peng(丁立鹏), Chen Hou-wen(陈厚文). Principle and application of high reso-lution scanning transmission electron microscope(高分辨扫描透射电子显微镜原理及其应用)[J]. Physics(物理), 2015, 44: 446–452.
|
 2021, Vol. 35
2021, Vol. 35