苯酚在纤维、塑料、医药、农药、香料、涂料、染料和炼油等工业领域中, 应用范围颇广, 属于大吨位需求产品[1-2]. 工业上90%以上的苯酚来源于异丙苯工艺, 但此工艺仍存在反应流程较长、原子利用率低、污染严重且产率较低等问题, 其原因在于苯酚分子结构中氧原子为sp2杂化, 氧原子提供一对孤电子与苯环碳原子共同形成离域键, 且羟基的推电子效应又加强了O-H键的极性[3]; 然而, 苯环中的C-H键的低反应性[4], 使酚羟基中的氢容易分解而发生二次反应转变为二酚或醌副产物[5], 从而大大降低了苯酚的选择性.
据不完全统计用于苯羟基化制苯酚的催化剂, 主要是以钒、铁、铜及镍为活性中心的催化剂. 如Elmetwally等[6]采用化学气相转变法制备了FeOCl催化剂, 由于FeOCl拥有自氧化还原电位和在短时间内产生大量羟基自由基的优越性, 使其用于苯羟基化反应制苯酚中, 选择性高达100%. Yue等[7]按照含铁沸石晶种的方向并通过干凝胶转化法制备了Fe-MFI沸石, 通过一系列表征发现, 含铁沸石晶种溶胶增强了铁物种的分布, 苯酚选择性可达97%. 王旭等[8]以汞灯照射为光源, 采用沉积沉淀法制备NiOx/介孔杭锦2#土催化剂, 进行苯羟基化光催化研究, 经过反应条件优化, 苯酚的选择性和产率可达93%和56%, 且催化剂使用3次活性无明显下降. 而含钒催化剂目前研究较多, 且此类催化剂在苯羟基化制苯酚中表现出了较高的催化活性, 选择性均高于90%[9]. 如罗茜等[10]以自制的两种硅钼钒和硅钨钒Keggin型杂多酸作催化剂, 以冰醋酸作溶剂进行苯羟基化制苯酚, 选择性达90.3%和87.4%. 表明钒取代的杂多酸对苯直接羟基化制苯酚具有高的催化选择性. 李贵贤等[11]采用分步反应、分步酸化法制备了Keggin型磷钼钒缺位型杂多酸, 研究结果表明适当提高多酸盐中钒取代量有利于增加催化剂的氧化能力, 在苯羟基化反应中苯酚的收率、选择性分别可达27.9%和89.0%. Shijina等[12]通过湿式浸渍法制备了V2O5-Al2O3催化剂, 并在苯羟基化反应中有良好的催化活性, 经过表征分析, 催化剂中的无定型表面钒活性中心是影响苯酚选择性的主要原因. 然而, 以上催化剂虽然呈现出高的选择性, 但催化剂稳定性较差, 其主要原因在于活性中心容易流失, 活性中心的分散度不好等. 其次, 不同的氧化剂对苯羟基化反应制苯酚的转化率和选择性起到至关重要的作用. 目前苯羟基化合成苯酚的氧化剂主要有N2O、H2O2、O2等[13]. 其中H2O2成为苯羟基化制苯酚的主导氧化剂, 其主要原因在于反应副产物仅为H2O, 产物选择性高, 原子利用率高且对环境没有污染. 若以N2O作氧化剂, 反应后含氮化合物对环境有影响, 生产和运输的成本都比较高且来源范围小; 而采用O2做氧化剂苯酚产物的收率太低. 因此, 以H2O2为氧化剂并使用钒类催化剂催化氧化苯制苯酚是取代异丙苯法路线生产苯酚的绿色环保路线[14-16].
我们通过水热合成法合成VOx/SiO2-Al2O3催化剂, 并采用XRD、SEM、TEM、XPS、NH3-TPD、N2物理吸脱附等技术对催化剂物化性质进行表征; 同时研究VOx/SiO2-Al2O3催化剂催化苯羟化制苯酚反应的催化性能.
1 实验部分 1.1 催化剂的制备 1.1.1 SiO2-Al2O3复合氧化物的制备将9.3438 g硅溶胶和1.1897 g环己胺混合配成悬浊液. 将0.3428 g NaOH加入另一个装有一定量蒸馏水的烧杯中使其溶解, 再加入0.2639 g NaAlO2粉末搅拌至溶解. 将以上两种溶液混合搅拌3 h, 得到白色硅铝凝胶. 将其装入聚四氟乙烯内衬放入反应釜中; 然后转入均相反应器, 在170 ℃、20 r/min的条件下晶化24 h之后, 冷却、抽滤、洗涤, 最后将固体物质在110 ℃下干燥12 h, 然后在马弗炉中550 ℃焙烧6 h. 将制备好的样品用1 mol/L NH4NO3溶液进行离子交换3次, 然后将其在干燥箱中110 ℃下干燥12 h, 在马弗炉中550 ℃焙烧6 h得到SiO2-Al2O3(实测Si/Al=2.55)复合氧化物.
1.1.2 VOx/SiO2-Al2O3催化剂的制备将一定量的V2O5加入60 mL去离子水中, 搅拌的同时再加入SiO2-Al2O3复合氧化物, 继续搅拌20 min后移至100 mL聚四氟乙烯内衬, 转入高压反应釜中并用去离子水填充至容量的80%左右, 将高压反应釜密封并在170 ℃保持24 h, 然后冷却至室温进行抽滤, 并用去离子水洗涤3次, 最后将固体样品在110 ℃下干燥24 h, 在马弗炉中550 ℃焙烧6 h得到a%VOx/SiO2-Al2O3系列催化剂(若钒含量为4%时催化剂样品记作4%VOx/SiO2-Al2O3).
1.2 催化剂的表征XRD测试通过D/MAX-2400X射线衍射仪(布鲁克AXS公司)测定. Cu-kɑ辐射(λ=0.1542 nm), 测试电流为50 mA, 测试电压为40 kV, 其扫描范围为2θ=5°~60°, 扫描速率为10°/min. 催化剂的表面形貌通过JSM-6701F型扫描电子显微镜(日本电子光学公司)观察, 并采用TECNAI G2透射电子显微镜(美国FEI公司)观察催化剂的形貌结构. 催化剂N2物理吸/脱附采用Autosorb-iQ气体吸附分析仪(美国康塔仪器公司)在-196 ℃下通过氮气物理吸/脱附实验测定. 利用PHI5702X-ray光电子能谱仪(美国物理电子公司)对样品中的待测元素进行价态分析, 激发光源为Al靶, 功率为250 W, 电压为14 kV. 催化剂的NH3-TPD分析在Quantachrome公司Autosorb-iQ-Cchemisorption分析仪上进行. 采用Nicolet Nexus 670傅里叶变换红外光谱仪(美国Nicolet公司)进行红外光谱的测定, 设备分辨率为4 cm-1, 扫描范围是500~4000 cm-1.
1.3 催化剂的性能评价采用苯羟化制苯酚反应来评价催化剂的催化性能. 具体步骤如下: 将15 mL乙腈、0.2 g催化剂、4 mL苯加入装有回流冷凝管的100 mL三颈圆底烧瓶中, 加热到70 ℃后逐滴滴加12.5 mL 30%H2O2, 滴加完毕后继续反应6 h. 反应结束后将产物与催化剂离心分离, 产物用气相色谱分析. 气相色谱分析条件: 离子火焰(FID)检测器, SE-30毛细管柱(30 m×0.53 mm×1 μm), 进样口温度240 ℃, 分流检测器温度240 ℃. 柱温采用程序升温, 初始温度60 ℃, 初始时间3 min, 以15 ℃/min的速率升温至200 ℃, 恒温保持1 min.
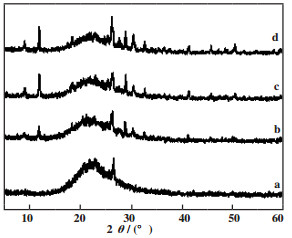
2 结果与讨论 2.1 VOx/SiO2-Al2O3系列催化剂物化性质表征图 1为SiO2-Al2O3复合氧化物和VOx/SiO2-Al2O3系列催化剂的XRD谱图. 由图 1可以看出, SiO2-Al2O3复合氧化物的表征结果显示在2θ为22.8°左右处出现了宽而弥散的无定形峰, 说明合成的复合氧化物表面仍有较多的羟基存在[17]. 而负载型VOx/SiO2-Al2O3催化剂谱图中可以看出, 负载钒后未改变此复合氧化物的结构, 而在2θ为9.16°、11.98°、15.86°、20.61°、21.26°、30.51°和32.75°出现了特征衍射峰, 均为钒氧化物的特征峰[18], 其它衍射峰是由于钒氧化物的聚集所造成的, 这表明钒活性中心被分散于SiO2-Al2O3复合氧化物表面.
|
图 1 SiO2-Al2O3复合氧化物及VOx/SiO2-Al2O3系列催化剂的XRD谱图 Fig.1 XRD spectra of SiO2-Al2O3 composite oxide and VOx/SiO2-Al2O3 series catalysts (a. SiO2-Al2O3; b. 3%VOx/SiO2-Al2O3; c. 4%VOx/SiO2-Al2O3; d. 5%VOx/SiO2-Al2O3) |
图 2为SiO2-Al2O3复合氧化物及VOx/SiO2-Al2O3系列催化剂SEM和TEM表征结果. 由图 2可以看出, SiO2-Al2O3形貌为规则的层片状形态, 而VOx/SiO2-Al2O3系列催化剂形貌略有不同, 呈现碎片化“积雪堆”状态. 同时基于TEM表征发现, SiO2-Al2O3为规则的层片状形态, 而VOx/SiO2-Al2O3系列催化剂呈现“珊瑚”状态. 其次, 催化剂表面没有明显金属氧化物颗粒存在, 这表明活性中心钒在催化剂表面分散均匀. 为了能够更直观地测定钒活性中心的分散程度, 对催化剂4%VOx/SiO2-Al2O3进行Mapping测试. 由图 3可以看出, 钒活性中心呈均匀的分布状态而分散于SiO2-Al2O3复合氧化物表面.

|
图 2 SiO2-Al2O3复合氧化物及VOx/SiO2-Al2O3系列催化剂的SEM和TEM图 Fig.2 SEM and TEM photos of SiO2-Al2O3 composite oxide and VOx/SiO2-Al2O3 series catalysts (SEM: a. SiO2-Al2O3; b. 3%VOx/SiO2-Al2O3; c. 4%VOx/SiO2-Al2O3; d. 5%VOx/SiO2-Al2O3; e. 4%VOx/SiO2-Al2O3 after the reaction; TEM: a. SiO2-Al2O3; b. 3%VOx/SiO2-Al2O3; c. 4%VOx/SiO2-Al2O3; d. 5%VOx/SiO2-Al2O3; e. 4%VOx/SiO2-Al2O3 after the reaction) |

|
图 3 4%VOx/SiO2-Al2O3催化剂Mapping图 Fig.3 Mapping photos of 4%VOx/SiO2-Al2O3 catalyst |
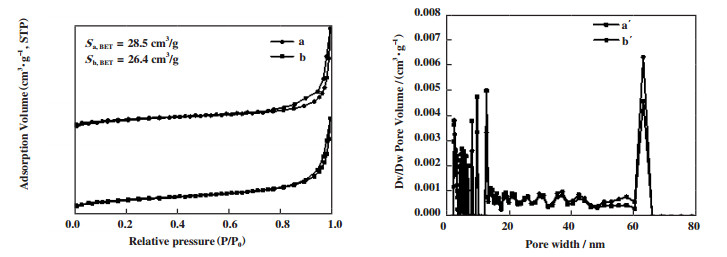
图 4为SiO2-Al2O3复合氧化物和4%VOx/SiO2-Al2O3催化剂的N2吸附等温线. 由图 4可看出, 样品的N2吸附/脱附等温线在P/P0=0.8处开始出现滞回环, 在低压范围内吸脱附曲线没有显著的凹凸, 说明此催化剂不具有微孔[19]; 根据IUPAC分类, 该等温线属于典型的II型和IV型之间的过渡状态和典型的H3型回滞环, 即介孔载体的典型特征[20-21]. 同时从粒径分布图可知, 此催化剂孔结构相当不规则, 但是钒的负载对其孔结构的影响很小[19], 而在60~65 nm的大孔可能是由于在合成复合氧化物时颗粒之间大量堆积形成的大孔[22].
|
图 4 SiO2-Al2O3复合氧化物和4%VOx/SiO2-Al2O3催化剂的N2吸附/解吸等温线和孔径分布图 Fig.4 N2 adsorption/desorption isotherms and pore size distribution of SiO2-Al2O3 composite oxide and 4%VOx/ SiO2-Al2O3 catalysts (SiO2-Al2O3(a), 4%VOx/SiO2-Al2O3 (b), SiO2-Al2O3(a´), 4%VOx/SiO2-Al2O3(b´)) |
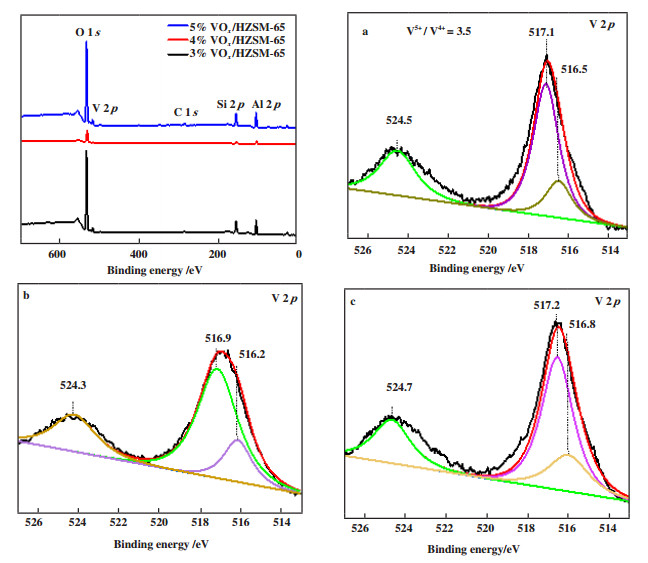
为了研究催化剂表面的元素状态和相对含量, 对VOx/SiO2-Al2O3系列催化剂进行了XPS表征如图 5所示. 由图 5可以看出, VOx/SiO2-Al2O3催化剂在V 2p区域发生分裂说明存在V5+和V4+, 其中[23]在结合能为516.2和516.1 eV属于V 2p3/2区域的V4+, 对应的钒氧化物可能以VO2为主; 结合能为517.0、517.1和571.3 eV属于V 2p3/2区域的V5+峰、结合能在524 eV左右为中心的峰为V 2p1/2区域的V5+峰[24], 对应的钒氧化物可能以V2O5为主. 然而, 随着负载量的增加, 钒更易堆积而使得V4+峰逐渐减少[25]. 综上说明催化剂中钒以混合价态的形式存在, 且当负载量为4%时, V5+与V4+的比值最小, 说明与其他催化剂相比, 4%VOx/SiO2-Al2O3催化剂中V4+含量最多. 据文献报道[26], 催化剂以钒为活性中心在苯羟基化直接制苯酚反应中V4+起主要作用.
|
图 5 VOx/SiO2-Al2O3系列催化剂XPS光谱图 Fig.5 XPS spectra of VOx/SiO2-Al2O3 series catalysts (3%VOx/SiO2-Al2O3(a), 4%VOx/SiO2-Al2O3(b), 5%VOx/SiO2-Al2O3(c)) |
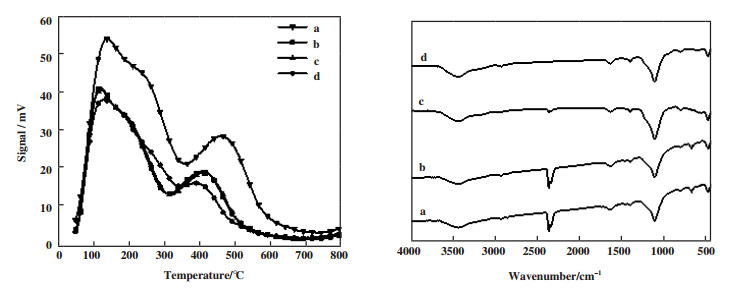
粉末状晶态V2O5本身具有一定的酸性, 但是钒氧化物被均匀分散到催化剂表面时, 会大大降低催化剂酸性[22]. 因此为了弥补匹配高效氧化反应的酸性环境, 合成了拥有一定酸量的VOx/SiO2-Al2O3催化剂. SiO2-Al2O3复合氧化物和VOx/SiO2-Al2O3系列催化剂的NH3-TPD谱图和FT-IR谱图如图 6所示. 由图 6可看出, 在100~200 ℃和350~500 ℃均出现脱附峰, 分别对应催化剂弱酸位和中强酸位[27], 发现随着钒负载量的增加各酸位均向低温区偏移, 且峰面积减小, 说明随着钒量的增加催化剂酸量逐渐减少. 然而, 催化剂的活性变化与酸性位的强弱相关, 活性中心钒的负载使得总酸性降低, 当酸性为特定值时苯羟基化活性达到最优[28]. 同时苯羟基化制苯酚过程中苯酚的生成是由于反应中双氧水在酸性条件下生成羟基自由基·OH直接与苯环发生加成反应生成苯酚[18], 而过量的钒将使得过氧化氢产生较少的·OH. 因此钒的负载量将决定催化剂酸性以及促使过氧化氢有效生成羟基自由基, 从而影响催化剂的催化活性. 由图 6中FT-IR谱图可看出, 在引入钒氧化物后各峰变化较小, 在466 cm-1处呈现的吸收峰属于Si-O键的弯曲振动峰, 584 cm-1附近呈现的吸收峰属于五元环弯曲振动特征峰[29], 在1102 cm-1附近的吸收峰归属于(Si, Al)O四面体的面内反对称拉伸振动[30], 在793 cm-1附近属于(Si, Al)O四面体的面对称拉伸振动, 在3793和2357 cm-1附近呈现的吸收峰为-OH基团的伸缩振动峰[20], 而在2357 cm-1附近呈现的吸收峰随着钒负载量的增加而减少, 960 cm-1出没有吸收峰说明钒氧化物没有进入分子筛骨架[31], 由此可进一步说明钒氧化物并没有进入SiO2-Al2O3复合氧化物的骨架结构, 而是均匀分散在复合氧化物表面.
|
图 6 SiO2-Al2O3复合氧化物和VOx/SiO2-Al2O3系列催化剂的NH3-TPD及FT-IR谱图 Fig.6 NH3-TPD and FT-IR spectra of SiO2-Al2O3 composite oxide and VOx/SiO2-Al2O3 series catalysts (SiO2-Al2O3(a), 3%VOx/SiO2-Al2O3(b), 4%VOx/SiO2-Al2O3(c), 5%VOx/SiO2-Al2O3(d)) |
由表 1可知, SiO2-Al2O3复合氧化物对苯羟化制苯酚反应基本没有催化性能. 若用V2O5作为催化剂, 苯的转化率为23.1%, 苯酚的选择性为91.1%. 而对于负载型催化剂, 随着钒负载量的增加, 苯酚的选择性均较高, 而苯的转化率呈现先上升再下降的趋势, 可能由于钒氧化物以VO4孤立四面体形式增多、催化剂呈现片状结构及短孔道结构而有利于产物的扩散, 并且载体所提供的适量酸性及载体与钒物种的相互作用, 使得催化剂具有较好的催化性能. 钒负载量大于4%时, 活性位的数量基本不变, 过量的钒氧化物在复合氧化物载体表面发生团聚[32], 造成活性中心分散的不均匀、V4+的量减少或V5+的增加促使氧化剂分解成自由基的量减少以及催化酸环境的微小改变等. 因此, 我们认为拥有特定酸量、高含量V4+和活性中心高分散的催化剂才能够高效催化苯羟化制苯酚.
| 表 1 不同催化剂催化苯羟化反应活性 Table 1 Activity of different catalysts for hydroxylation of benzene |
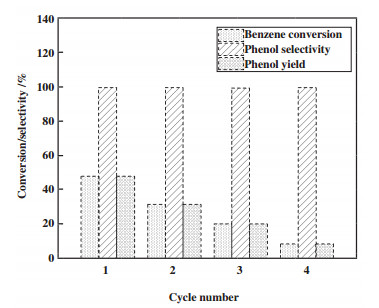
催化剂的循环稳定性数据如图 7所示. 通过实验结果可以看出催化剂重复4次后, 产物苯酚的选择性基本保持不变, 但是苯的转化率出现降低, 其主要原因可能在于钒活性中心的流失以及钒(V4+)量的减少. 其次, 反应体系中的有机物被吸附而覆盖了催化剂活性中心, 占据了催化剂的活性位点, 降低了催化剂的吸附性能, 从而影响催化剂的催化活性. 总之从实验结果表明, 4%VOx /SiO2-Al2O3催化剂具有很好的活性, 但是催化剂活性的再生问题仍需要突破.
|
图 7 催化剂的循环稳定性 Fig.7 The Cycle stability of the catalyst |
采用水热合成法合成了SiO2-Al2O3复合氧化物, 其结构为无定形. 然而以SiO2-Al2O3为载体合成的VOx /SiO2-Al2O3系列催化剂, 在苯羟化制苯酚反应中却表现出良好的催化性能. 主要原因在于制备的催化剂中拥有高的V4+活性中心且能够均匀分散于SiO2-Al2O3复合氧化物表面上, 同时V5+含量的减少和特定的酸含量将有效促进氧化剂高效分解为氢氧自由基, 从而有利于催化剂在反应中表现出较高的催化活性. 基于最优条件, 获得优越的催化活性(48.1%)和选择性(99.6%).
| [1] |
a. Boz I, Altincekic T G. Liquid phase hydroxylation of benzene to phenol over Cu/ZnO catalysts[J]. React Kinet Mech Catal, 2011, 102(1): 195-205. b. Yu Tian-hua(余天华), Huang Qi-peng(黄启鹏), SiTu Cheng(司徒成), et al. Study on the structure of Cu/SiO2 and their catalytic performance in the reaction of phenol hydroxylation(Cu/SiO2结构及其催化苯酚羟基化反应性能的研究)[J]. J Mol Catal(China)(分子催化), 2020, 34(2): 97-104. |
| [2] |
a. Zhang F, Chen X, Zhuang J, et al. Direct oxidation of benzene to phenol by N2O over meso-Fe-ZSM-5 catalysts obtained via alkaline post-treatment[J]. Catal Sci Tech, 2011, 1(7): 1250-1255. b. Lu Jin-zhi(鲁金芝), Ma Zhan-wei(马占伟), Wei Xue-mei(魏雪梅), et al. CeO2 supported NiCo bimetal catalyzes liquid phase hydrogenation of phenol(CeO2负载NiCo双金属催化苯酚液相加氢)[J]. J Mol Catal(China)(分子催化), 2020, 34(1): 36-44. c. Quan Xiao-qi(权晓琪), Xu Pei-yao(许佩瑶), Yang Fan(杨帆), et al. Degradation of acetaminophen in water by molecular sieve catalyst-sulfite system(分子筛催化剂-亚硫酸盐体系降解水中对乙酰氨基苯酚)[J]. J Mol Catal(China)(分子催化), 2019, 33(6): 561-569. |
| [3] |
Li Na (李娜). Vanadium-Zirconium Catalyst for Aerobic Oxidation of Benzene to Phenol(钒锆催化剂催化氧气氧化苯制备苯酚)[D]. XiAn(西安): Shanxi University of Science and Technology (陕西科技大学), 2018.
|
| [4] |
Lu E, Wu J, Yang B, et al. Selective hydroxylation of benzene to phenol over Fe nanoparticles encapsulated within N-Doped carbon shells[J]. ACS Appl Nano Mater, 2020, 3(9): 9192–9199.
DOI:10.1021/acsanm.0c01824 |
| [5] |
Gao Xiao-han(高肖汉), Lv Xue-chuan(吕雪川), Xu Jie(徐杰). Research progress on direct catalytic oxidation of benzene to Phenol(苯直接催化氧化合成苯酚的研究进展)[J]. J Mol Catal(China)(分子催化), 2008, 22(4): 379–384.
|
| [6] |
Elmetwally A E, Eshaq G, Yehia F Z, et al. Iron oxychloride as an efficient catalyst for selective hydroxylation of benzene to phenol[J]. ACS Catal, 2018, 8: 10668–10675.
DOI:10.1021/acscatal.8b03590 |
| [7] |
Yue M, Jiang X, Zhang H, et al. Quasi-solid-phase synthesis of Fe-MFI zeolites by using Fe-containing zeolite seed sol for hydroxylation of benzene with H2O2[J]. Micropor Mesopor Mat, 2020, 294: 109891.
DOI:10.1016/j.micromeso.2019.109891 |
| [8] |
Wang Xu(王旭), Bai Sagala(萨嘎拉), Bao Zhaorigetu(照日格图). Hydroxylation of benzene to phenol by photocatalysis on NiOx/meso Hangjin2~#Clay(NiOx/介孔杭锦2~#土的制备及其对苯羟基化光催化性能研究)[J]. J Mol Catal(China)(分子催化), 2015, 29(3): 266–274.
|
| [9] |
Wei M, Han W W, Li J, et al. Direct hydroxylation of benzene to phenol by dielectric barrier discharge plasma[J]. Russ J Phys Chem A, 2020, 93(13): 2812–2816.
DOI:10.1134/S003602441913020X?utm_medium=affiliate&utm_content=meta&utm_campaign=DDCN_1_GL01_metadata |
| [10] |
Luo Qian(罗茜), Dong Liang(董亮), Wang Jin-yue(王金月), et al. The catalytic performance of siliconsubstituted heteropolymolybdates and heteropolytungstates for the direct oxydation of benzene to phenol using hydrogen peroxide(硅钼钒和硅钨钒杂多酸催化过氧化氢直接氧化苯制苯酚的活性研究)[J]. J Mol Catal(China)(分子催化), 2007, 21(2): 128–131.
DOI:10.3969/j.issn.1001-3555.2007.02.007 |
| [11] |
Li Gui-xian(李贵贤), Tan Xue-ling(谭学苓), Wang Kong-zhao(汪孔照), et al. The catalytic oxidation of benzene to pphenol over molybdovanadophosphoric quaternary ammonium with keggin-type as catalyst keggin(型磷钼钒季铵盐催化氧化苯制苯酚反应研究)[J]. J Mol Catal(China)(分子催化), 2009, 23(2): 168–172.
|
| [12] |
Shijina A V, Renuka N K. Single step conversion of benzene to phenol using hydrogen peroxide over modified V2O5-Al2O3 systems[J]. React Kinet Catal Lett, 2009, 98(1): 139–147.
DOI:10.1007/s11144-009-0079-0 |
| [13] |
Zhao Xin-hong(赵新红), Yang Zhi-gang(杨志刚), Su Na(苏娜), et al. Phenol hydroxylation todihydroxybenzene over iron-based zeolitic catalysts(铁基沸石类催化剂催化苯酚羟基化制备苯二酚的研究)[J]. Ind Catal(China)(工业催化), 2021, 29(3): 16–26.
DOI:10.3969/j.issn.1008-1143.2021.03.003 |
| [14] |
Lin Dan(林丹), Sun Yu-ting(孙玉婷), Zhu Chuan-fang(朱传方). Introduction of direct catalytic oxidation of benzene to phenol(直接催化氧化苯制苯酚的研究简介)[J]. J Chem Edu(China)(化学教育), 2010, 31(3): 19–21.
DOI:10.3969/j.issn.1003-3807.2010.03.008 |
| [15] |
Liu Qing-qing(刘青青), Liu Bao-sheng(刘宝生), Huang Jun-zuo(黄军左), et al. Study on direct catalytic oxidation of benzene to phenol in different oxidants(不同氧化剂下苯直接催化氧化制苯酚的研究)[J]. Mod Chem Ind(China)(现代化工), 2011, 31(7): 27–31.
|
| [16] |
Zhang Xiong-fu(张雄福). Direct Hydroxylationof Benzene to Phenol(苯直接一步氧化合成苯酚)[J]. Prog Chem(China)(化学进展), 2008, 20(2/3): 386–395.
|
| [17] |
Li Zhong(李忠), Meng Fan-hui(孟凡会), Ren Jun(任军), et al. Surface structure and catalytic performance of CuCl/SiO2-Al2O3 catalysts for methanol oxidative carbonylation(CuCl/SiO2-Al2O3催化剂的表面结构及甲醇氧化羰基化催化性能)[J]. Chin J Catal(China)(催化学报), 2008, 29(7): 643–648.
DOI:10.3321/j.issn:0253-9837.2008.07.012 |
| [18] |
Gao Yuan(高远). Vanadium-based catalyst in the application of hydroxylation of benzene(钒基催化剂在苯羟基化反应中的应用)[D]. Dalian(大连): Liaoning Normal University(辽宁师范大学), 2015.
|
| [19] |
Xu J, Chen Y, Hong Y, et al. Direct catalytic hydroxylation of benzene to phenol catalyzed by vanadia supported on exfoliated graphitic carbon nitride[J]. Appl Catal A-Gen, 2018, 549: 31–39.
DOI:10.1016/j.apcata.2017.09.015 |
| [20] |
Shen B, Wang F, Zhao B, et al. The behaviors of V2O5-WO3/TiO2 loaded on ceramic surfaces for NH3-SCR[J]. J Ind Eng Chem, 2016, 33: 262–269.
|
| [21] |
Pei Su-peng(裴素朋). Studies on the synthesis and catalytic application of vanadum-based metal oxides in the selective oxidation of methane and propane(含钒氧化物和复合氧化物催化剂的制备及其在甲烷和丙烷选择氧化反应中的应用研究)[D]. Shanghai(上海): Fudan University(复旦大学), 2007.
|
| [22] |
Nemati Kharat A, Moosavikia S, Tamaddoni Jahromi B, et al. Liquid phase hydroxylation of benzene to phenol over vanadium substituted Keggin anion supported on amine functionalized SBA-15[J]. J Mol Catal A-Chem, 2011, 348(1/2): 14–19.
|
| [23] |
Wang C, Hu L, Wang M, et al. Vanadium supported on graphitic carbon nitride as a heterogeneous catalyst for the direct oxidation of benzene to phenol[J]. Chin J Catal(China), 2016, 37(11): 2003–2008.
|
| [24] |
Shi Lei-lei(石磊磊). Study on catalytic oxidation of benzene to phenol over vanadium based catalyst with molecular O2(含钒催化剂催化氧气氧化苯制备苯酚的研究)[D]. XiAn(西安): Shanxi University of Science and Technology (陕西科技大学), 2017.
|
| [25] |
Xu J, Hong Y, Cheng M J, et al. Vanadyl acetylacetonate grafted on ordered mesoporous silica KIT-6 and its enhanced catalytic performance for direct hydroxylation of benzene to phenol[J]. Micropor Mesopor Mat, 2019, 285: 223–230.
|
| [26] |
Shang X, Hu G, He C, et al. Regeneration of full-scale commercial honeycomb monolith catalyst (V2O5-WO3/TiO2) used in coal-fired power plant[J]. J Ind Eng Chem, 2012, 18(1): 513–519.
|
| [27] |
Li Meng-xi(李梦溪). The study on systhesis of zeolites ZSM-35 and theirscatalytic influences for butene skeletal isomerization(ZSM-35分子筛的合成及其催化正丁烯异构的研究)[D]. Xiamen (厦门): Xiamen University(厦门大学), 2017.
|
| [28] |
Guo Chao(郭超). Research on hydroxylation of benzene to phenol in supported Vspecies-O2-reducing agent systems(负载V-O2-还原剂体系中苯羟基化制苯酚的研究)[D]. Dalian(大连): Liaoning Normal University(辽宁师范大学), 2013.
|
| [29] |
Feng H, Li C, Shan H. In-situ synthesis and catalytic activity of ZSM-5 zeolite[J]. Appl Clay Sci, 2009, 42(3/4): 439–445.
|
| [30] |
Lv Zi-qi(吕子奇). Synthesis and adsorption properties of ZSM-35 molecular sieve(ZSM-35分子筛的合成及其吸附性能研究)[D]. Guilin(桂林): Guangxi Normal University(广西师范大学), 2020.
|
| [31] |
Anunziata O A, Pierella L B, Beltramone A R. Synthesis, characterization and catalytic activity of selective oxidation zeolites catalysts[J]. Stud Surf Sci Catal, 1999, 125: 523–530.
|
| [32] |
Makgwane P R, Ray S S. Development of a high-performance nanostructured V2O5/SnO2 catalyst for efficientbenzenehydroxylation[J]. Appl Catal A-Gen, 2015, 492: 10–22.
|
 2021, Vol. 35
2021, Vol. 35


