不可再生能源日渐枯竭, 人们致力于寻找环保、可持续、生态友好的能源来替代传统化石燃料[1]. 氢气是一种理想的清洁能源载体, 其燃烧热值高、燃烧产物无污染, 并且制备氢气的原料是地球储量极为丰富的水, 因此大力开发氢能源成为解决能源危机的重要策略. 在各种氢气生产方法中, 碱性水电解技术已被证明是最有前途的技术之一[2-3]. 目前, 电催化水分解制氢最高效的催化剂仍然是贵金属Pt, 但其高昂的价格使其难以满足实际生产要求[4-5], 因此设计合成廉价的非贵金属析氢催化剂势在必行.
目前, 过渡金属基材料由于其低廉的价格、丰富可调的元素组成和多维形貌结构, 使其成为未来替代Pt的最具前景的电催化材料. 众多的过渡金属基析氢电催化剂, 包括过渡金属合金[6]、碳化物[7]、磷化物[8]、氮化物[9]、硫化物[10]、硼化物[11]等被广泛研究报道. 其中, 合金, 尤其是Ni-Mo合金是一类优秀的析氢电催化剂. Ni-Mo合金具有类铂的电子结构和催化性能, 可以促进Hads在催化剂表面的快速吸脱附. 然而, 与酸性电解液不同的是, 在碱性电解液中H+浓度极低, 电催化析氢过程首先发生的是H2O在催化剂表面解离形成Hads, Hads进一步结合生产H2. 因此, 尽管Ni-Mo合金具有较好的Hads吸脱附能力, 但是H2O分子在其表面解离缓慢, 造成其析氢反应动力学缓慢、Tafel斜率较高, 其仍然无法完全替代贵金属Pt. 近期研究发现, 过渡金属氧化物(MxOy)在电催化析氢过程中可以有效加速H2O解离并释放Hads, 因此将MxOy与Ni-Mo合金复合将有望改善Ni-Mo合金的析氢性能[12]. 然而, 目前所报道的此类二元电催化材料通常只具有简单的一维结构, 例如纳米线、纳米棒等[13-14], 低维形貌不利于催化性能进一步提升. 二维纳米材料具有高比表面积、良好导电性、丰富的活性位点, 是目前广泛研究的电催化材料. 可以预见的是, 如果设计合成具有二维形貌结构的二元复合电催化剂有助于进一步改善析氢性能.
我们报道了一例新颖的二元过渡金属纳米片阵列自支撑电极(MoO3-x-MoNi4@NF), MoO3-x纳米片表面镶嵌着MoNi4合金纳米颗粒. 该自支撑电极催化剂具有高效的电催化析氢性能, 在碱性电解液中(1 mol/L KOH), MoO3-x-MoNi4@NF仅需要过电位30 mV就能达到10 mA·cm-2电流密度, 这个值甚至超过贵金属催化剂20% Pt/C(32 mV). 同时, MoO3-x-MoNi4@NF具有超低的Tafel斜率, 仅为31 mV dec-1, 如此低的Tafel斜率得益于Ni-Mo合金与MoO3-x之间的协同催化剂作用的发挥, MoO3-x可以有效促进H2O解离并释放Hads, MoNi4纳米颗粒作为Hads吸脱附位点可以促进H2生成, 这使得该催化剂有望替代贵金属铂用作碱性电催化析氢领域.
1 实验部分 1.1 电催化剂的制备 1.1.1 制备NiMoO4@NF首先, 在磁力搅拌下, 将2 mmol的NiSO4和2 mmol的(NH4)6Mo7O24·4H2O溶于80 mL蒸馏水, 搅拌30 min. 之后将溶液转移至反应釜中, 将泡沫镍竖直放入溶液中, 120 ℃水热反应6 h. 冷却至室温后, 将样品取出, 水洗, 在80 ℃干燥即获得NiMoO4@NF.
1.1.2 制备MoO3-x-MoNi4@NF将NiMoO4@NF置于管式炉中间位置, 通入H2/N2混合气体, 加热至350 ℃保持2 h, NiMoO4被还原生成MoO3-x-MoNi4@NF.
1.2 表征仪器用X射线粉末衍射仪(PXRD)在Cu-Kα辐射源(λ=0.154 056 nm)上测定了样品的结晶度和晶相组成. 利用JEOL-JSM-4800F扫描电镜对样品进行了能谱分析和表面形貌观察. 在JEOL-2100F型200 kV加速电压显微镜上研究了透射电子显微镜(TEM)、高分辨率图像(HRTEM). 用Al-Kα(1486.6 eV)作为X射线源, 在ESCALABMKII光谱仪上记录了X射线光电子能谱(XPS). 用康塔iQ吸附仪研究了Brunauer-Emmett-Teller N2吸附-脱附等温线.
1.3 电催化析氢性能测试自支撑电极催化剂的电解水制氢采用辰华电化学工作站测定. MoO3-x-MoNi4@NF自支撑催化剂作为工作电极, 碳棒作为对电极, 汞/氧化汞电极作为参比电极, 电解液为1 mol/L的KOH溶液(pH = 14). LSV曲线的扫速2 mV· s-1, 测定固定电位下自支撑电极在非法拉第区域的不同扫速下的循环伏安曲线, 比较电化学活性面积. 阻抗测定频率范围100 000~0.01 vHz.
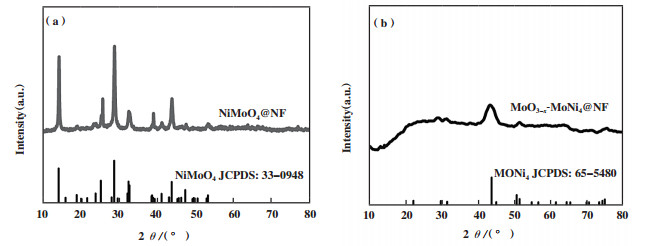
2 结果与讨论 2.1 催化剂的XRDNiMoO4@NF的XRD结果如图 1a所示, 14.2°, 19.0°, 23.8°, 25.4°, 28.9°, 32.6°, 39.1°, 41.1°, 43.8°, 47.3°和53.4°的衍射峰归属于NiMoO4(JCPDS No. 33-0948)的(110), (101), (-121), (-112), (220), (022), (-402), (400), (330), (-204)和(-510)晶面. 氢气气氛下还原后样品的XRD如图 1b所示, 其衍射峰与MoNi4(JCPDS No. 65-5480)一致, 表明NiMoO4被氢气还原生成合金MoNi4. 但是并没有观察到Mo-O物种相关XRD衍射峰, 暗示还原后的Mo-O物种是以无定型态形式存在.
|
图 1 (a)NiMoO4@NF的XRD图谱; (b)MoO3-x-MoNi4@NF的XRD图谱 Fig.1 (a) XRD patterns of NiMoO4@NF; (b) XRD patterns of MoO3-x-MoNi4@NF |
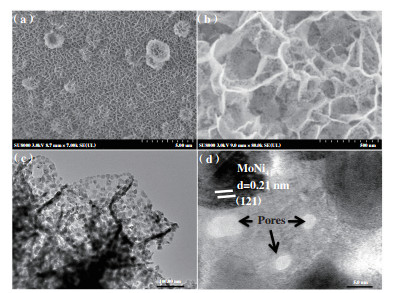
前驱体NiMoO4@NF形貌如图 2a所示, NiMoO4具有超薄的纳米片形貌, 纳米片表面平整光滑, 并且有序生长在泡沫镍基底上, 形成纳米片阵列结构, 纳米片阵列间距大约180 nm. NiMoO4@NF氢气还原后样品MoO3-x-MoNi4@NF的形貌如图 2b所示, 纳米片阵列结构得到很好的保持, 并且纳米片表面变得粗糙多孔, 这有利于增加材料比表面积. MoO3-x-MoNi4@NF的透射电镜结果如图 2c, 纳米颗粒均匀分布在纳米片表面, 颗粒尺寸大约10 nm. 高分辨透射电镜结果表明纳米颗粒的晶格衍射条纹为0.21 nm, 对应MoNi4的(121)晶面, 没有观察到其他晶格衍射条纹, 进一步证实Mo-O物种以无定型态存在, 这与XRD结果一致. 有趣的是, 氢气还原后纳米片表面出现大量孔洞, 这些孔洞可能是由于氢气还原过程中, Ni原子和部分Mo原子被还原并且聚集结合成MoNi4纳米颗粒所造成的, 丰富的孔洞有利于进一步增大比表面积(图 2d).
|
图 2 (a)NiMoO4@NF扫描电镜图片; (b)MoO3-x-MoNi4@NF扫描电镜图片; (c)MoO3-x-MoNi4@NF透射电镜图片; (d)MoO3-x-MoNi4@NF高分辨透射电镜图片 Fig.2 (a) SEM image of NiMoO4@NF; (b) TEM image of MoO3-x-MoNi4@NF; (c) TEM image of MoO3-x-MoNi4@NF; (d) HRTEM image of MoO3-x-MoNi4@NF |
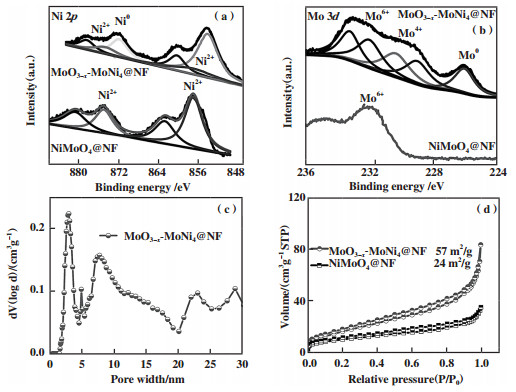
利用XPS光电子能谱研究MoO3-x-MoNi4@NF的元素组成和价态. Ni 2p HR-XPS光电子能谱如图 3a所示, 在前驱体NiMoO4@NF中, 只观察到Ni2+信号峰(857.2 eV), 氢气还原后, 在MoO3-x-MoNi4@NF中除了存在Ni2+信号峰, 还观察到强的Ni0信号峰(854.1 eV), 这说明氢气还原后, 几乎大多数Ni2+都被还原, 微弱的Ni2+信号峰可能是由于催化剂表面少量Ni被氧化造成的. 图 3b显示的是Mo 3d HR-XPS, 在前驱体NiMoO4@NF中, 只观察到Mo6+信号峰(232.1 eV), 氢气还原后, 在MoO3-x-MoNi4@NF中除了存在Mo6+信号峰, 还观察到强的Mo4+(230.4, 229.0 eV)和Mo0信号峰(226.0 eV), 这说明氢气还原后, 部分Mo6+被还原成金属并且与Ni结合形成MoNi4合金, 部分Mo6+被还原成低价Mo-O物种. 详细的XPS信息如表 1所示. 因此, 结合XRD和TEM结果, 氢气还原后纳米片的组成应当是MoO3-x, 纳米片表面镶嵌着MoNi4合金纳米颗粒. 孔尺寸分布曲线和氮气吸附-脱附等温曲线结果如图 3c-3d所示, 催化剂具有IV型吸附脱附曲线类型, 说明其具有介孔结构, MoO3-x-MoNi4@NF孔径大约在3~12 nm, 其比表面积为57 m2/g, 高于前驱体NiMoO4@NF的24 m2/g. 这说明MoO3-x-MoNi4@NF具有很高的比表面积和丰富的介孔结构.
|
图 3 (a)MoO3-x-MoNi4@NF的Ni 2p HR-XPS光电子能谱; (b)Mo 3d的HR-XPS谱图; (c)MoO3-x-MoNi4@NF氮气吸附-脱附等温曲线; (d)孔尺寸分布曲线 Fig.3 (a) Ni 2p HR-XPS spectrum of MoO3-x-MoNi4@NF; (b) HR-XPS of Mo 3d; (c) The N2 adsorption-desorption isotherms; (d) The pore-size distribution of MoO3-x-MoNi4@NF |
| 表 1 NiMoO4@NF和MoO3-x-MoNi4@NF的XPS对比 Table 1 The XPS comparison of NiMoO4@NF and MoO3-x-MoNi4@NF |
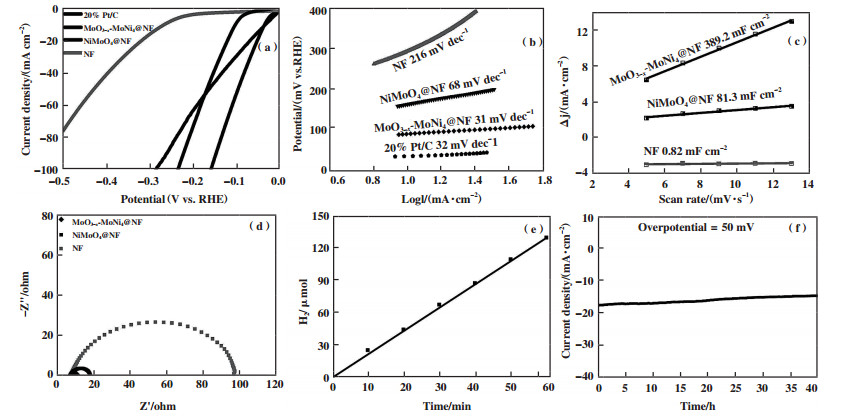
自支撑电极的电催化析氢结果如图 4所示, 以1 mol/L氢氧化钾溶液为电解液, 自支撑电极为工作电极, 碳棒为对电极, 汞/氧化汞电极为参比电极. 对比样品包括贵金属20% Pt/C、NiMoO4@NF和泡沫镍NF. LSV曲线如图 4a所示, MoO3-x-MoNi4@NF具有最高的催化活性, 其仅仅需要过电位30 mV即可达到电流密度10 mA·cm-2, 甚至超过贵金属20% Pt/C(32 mV). 而前驱体NiMoO4@NF和NF则分别需要较高的过电位140和290 mV才能达到同样的电流密度. MoO3-x-MoNi4@NF具有与贵金属20% Pt/C相当的塔菲尔斜率(图 4b), 分别是31和32 mVdec-1, 这说明MoO3-x-MoNi4@NF具有快速的电催化析氢反应动力学, 其析氢反应决速步骤是Tafel反应, 这应当得益于MoNi4合金纳米颗粒与MoO3-x纳米片之间协调催化作用的发挥, MoO3-x可以加速H-OH解离出Hads, 同时Hads在MoNi4表面迅速结合形成H2. NF和NiMoO4@NF的双电层电容(Cdl)分别是0.82和81.3 mF·cm-2. 氢气还原产物MoO3-x-MoNi4@NF具有极大的Cdl值, 389.2 mF·cm-2, 分别是NF和NiMoO4@NF的486倍和4.8倍. 这说明与其他对比样品相比, MoO3-x-MoNi4@NF具有最高的电化学活性面积(ECSA), 并且如此高的电化学活性面积有助于充分暴露活性位点、促进质子传递和电子传递(图 4c). 图 4d显示的是自支撑电极的电化学阻抗图, MoO3-x-MoNi4@NF、NiMoO4-NF和NF的电荷迁移电阻(Rct)分别是5、17和86 Ω, MoO3-x-MoNi4@NF具有最低的Rct值, 这得益于泡沫镍基底良好的导电性以及纳米片阵列开放多孔结构, 可以有效促进电荷传递, 降低电阻. 与其他对比样品相比, MoO3-x-MoNi4@NF具有最高的电化学活性面积(ECSA)和最低的电荷迁移电阻(Rct), 这得益于自支撑电极材料独特的纳米片阵列结构, 过渡金属纳米片原位生长在泡沫镍基底上, 纳米片阵列具有开放的孔道结构, 并且经过氢气还原处理后的纳米片进一步被刻蚀出现纳米级孔洞, 赋予催化剂更高的比表面积和孔道结构, 这有助于提高材料的电化学活性面积(ECSA), 并且开放多孔结构有助于加速电荷传递和质传递, 降低电阻. 图 4e是MoO3-x-MoNi4@NF电催化析氢法拉第效率, 接近100%, 说明电子利用率非常高, 没有其他副反应发生. 图 4f显示的是电流密度-时间曲线, 经过40 h电解后, 电流密度几乎没有改变, 说明MoO3-x-MoNi4@NF具有长期催化稳定性.
|
图 4 (a)1 mol/L氢氧化钾中各催化剂析氢LSV曲线; (b)塔菲尔斜率; (c)电流密度差值-扫速曲线(d)电化学阻抗; (e)法拉第效率; (f)电流密度-时间曲线 Fig.4 (a) LSV curves of catalysts for HER in 1 mol/L KOH; (b) Tafel slopes; (c) The difference in the current density (j) between the anodic and cathodic sweeps (Dj) versus the scan rate; (d) Electrochemical impedance spectra (EIS); (e) Faraday efficiency; (f) I-T curve |
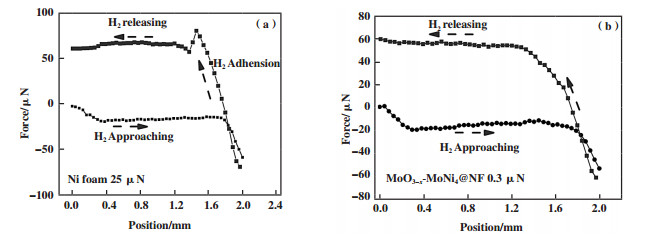
自支撑电极表面的气泡粘附力大小对于电催化产生的氢气气体的快速脱附具有重要影响, 当气泡在电极表面粘附力较小时, 有利于促进气体快速脱附, 促进析氢反应发生. 如图 5a所示, 氢气气泡在NF表面的粘附力为25 μN, 图 5b显示, 氢气气泡在MoO3-x-MoNi4@NF表面的粘附力为0.3 μN. 气泡在MoO3-x-MoNi4@NF表面的粘附力远小于在NF表面, 这是由于MoO3-x-MoNi4@NF表面覆盖着纳米片阵列, 阵列结构降低了电极表面三相线(气-液-固)的连续性, 使得气泡在MoO3-x-MoNi4@NF表面接触面积减小, 粘附力降低. 因此, 电催化析氢过程中所产生的氢气在其表面粘附力小, 可以迅速脱附, 促进析氢反应进行.
|
图 5 (a)氢气气泡在NF表面粘附力测试; (b)氢气气泡在MoO3-x-MoNi4@NF表面粘附力测试 Fig.5 (a) The H2 bubble adhesion force on the surface of NF; (b) The H2 bubble adhesion force on the surface of MoO3-x-MoNi4@NF |
我们报道了一例结构组成新颖的纳米片自支撑电极析氢催化剂MoO3-x-MoNi4@NF, 纳米片是由镶嵌了MoNi4合金纳米颗粒的无定型态的MoO3-x构成, 这个自支撑电极催化剂具有高效的电催化析氢性能, 甚至超过贵金属Pt/C. 其之所以具有高效析氢性能, 可归因于以下原因: (1)独特的纳米片阵列结构, 过渡金属纳米片原位生长在泡沫镍基底上, 纳米片阵列具有开放的孔道结构, 并且经过氢气还原处理后的纳米片进一步被刻蚀出现纳米级孔洞, 赋予催化剂更高的比表面积和孔道结构; (2)合金纳米颗粒与过渡金属氧化物之间的协同催化作用, MoO3-x可以加速H2O分子解离产生Hads, Hads在MoNi4表面迅速结合产生H2; (3)较小的表面气泡粘附力, 泡沫镍表面生长的纳米片阵列可以有效降低氢气气泡粘附力, 促进气体脱附, 加速析氢反应. 总之, 我们在文中为设计合成高效稳定的碱性电催化水裂解析氢电极材料提供了理论和实验指导, 对于解决当前能源危机具有积极意义.
| [1] |
a. Merki D, Hu X L. Recent developments of molybdenum and tungsten sulfides as hydrogen evolution catalysts[J]. Energ Environ Sci, 2011, 4(10): 3878-3888. b. Liu Hong-xia(刘洪霞), Lu Gong-xuan(吕功煊). Research progress for hydrogen evolution from formaldehyde(甲醛催化制氢的研究进展)[J]. J Mol Catal(China)(分子催化), 2020, 34(3): 210-226. c. Feng Chen-chen(冯晨晨), Zhang Ya-jun(张亚军), Bi Ying-pu(毕迎普). Research progress and challenges of α-Fe2O3 photoanode for photoelectrochemical water splitting(α-Fe2O3光阳极光电化学分解水的研究进展与挑战)[J]. J Mol Catal(China)(分子催化), 2020, 34(3): 227-241. d. Wang Meng(王蒙), Ma Jian-tai(马建泰), Lu Gong-xuan(吕功煊). The inhibition of hydrogen and oxygen recombination reverse reaction on cocatalyst surface in photocatalytic overall water splitting for hydrogen evolution(光催化全分解水制氢中助催化剂表面氢氧复合反应的抑制)[J]. J Mol Catal(China)(分子催化), 2019, 33(5): 461-485. |
| [2] |
Wang Guan-ning, Chen Ting-ting, C J Gómez-García , et al. A High-Capacity negative electrode for-asymmetric supercapacitors based on a PMo12 coordination polymer with novel water-assisted proton channels[J]. Small, 2020, 16(29): 2001626.
DOI:10.1002/smll.202001626 |
| [3] |
Subbaraman R, Tripkovic D, Strmcnik D, et al. Enhancing hydrogen evolution activity in water splitting by tailoring Li-Ni(OH)-Pt interfaces[J]. Science, 2011, 334(6060): 1256–1260.
DOI:10.1126/science.1211934 |
| [4] |
Zou Xiao-xin, Zhang Yu. Noble metal-free hydrogen evolution catalysts for water splitting[J]. Chem Soc Rev, 2015, 44(15): 5148–5180.
DOI:10.1039/C4CS00448E |
| [5] |
Shi Yan-mei, Zhang Bin. Recent advances in transition metal phosphide nanomaterials: Synthesis and applications in hydrogen evolution reaction[J]. Chem Soc Rev, 2016, 45(6): 1529–1541.
DOI:10.1039/C5CS00434A |
| [6] |
Fu Lu-hong, Li Yun-bo, Yao Na, et al. IrMo nanocatalysts for efficient alkaline hydrogen electrocatalysis[J]. ACS Catal, 2020, 10(13): 7322–7327.
DOI:10.1021/acscatal.0c02254 |
| [7] |
Hu Yang, Jensen J O, Zhang Wei, et al. Hollow spheres of iron carbide nanoparticles encased in graphitic layers as oxygen reduction catalysts[J]. Angew Chem Int Ed, 2014, 126(14): 3749–3753.
DOI:10.1002/ange.201400358 |
| [8] |
Popczun E J, Read C G, Roske C W, et al. Highly active electrocatalysis of the hydrogen evolution reaction by cobalt phosphide nanoparticles[J]. Angew Chem Int Ed, 2014, 126(21): 5531–5534.
DOI:10.1002/ange.201402646 |
| [9] |
Xie Jun-feng, Li Shuang, Zhang Xiao-dong, et al. Atomically-thin molybdenum nitride nanosheets with exposed active surface sites for efficient hydrogen evolution[J]. Chem Sci, 2014, 5(12): 4615–4620.
DOI:10.1039/C4SC02019G |
| [10] |
Peng Sheng-jie, Li Lin-lin, Han Xiao-peng, et al. Cobalt sulfide nanosheet/graphene/carbon nanotube nanocomposites as flexible electrodes for hydrogen evolution[J]. Angew Chem Int Ed, 2014, 126(46): 12802–12807.
DOI:10.1002/ange.201408876 |
| [11] |
Kadrekar R, Patel N, Arya A. Understanding the role of boron and stoichiometric ratio in the catalytic performance of amorphous Co-B catalyst[J]. Appl Surf Sci, 2020, 518: 146199.
DOI:10.1016/j.apsusc.2020.146199 |
| [12] |
Xu Kun, Cheng Han, Lv Hai-feng, et al. Controllable surface reorganization engineering on cobalt phosphide nanowire arrays for efficient alkaline hydrogen evolution reaction[J]. Adv Mater, 2018, 30(1): 1703322.
DOI:10.1002/adma.201703322 |
| [13] |
Chen Yu-yun, Zhang Yun, Zhang Xing, et al. Self-templated fabrication of MoNi4/MoO3-x nanorod arrays with dual active components for highly efficient hydrogen evolution[J]. Adv Mater, 2017, 29(39): 1703311.
DOI:10.1002/adma.201703311 |
| [14] |
Meng Ling-shen, Li Li-ping, Wang Jiang-hao, et al. Valence-engineered MoNi4/MoOx@NF as a Bi-functional electrocatalyst compelling for urea-assisted water splitting reaction[J]. Electrochim Acta, 2020, 350: 136382.
DOI:10.1016/j.electacta.2020.136382 |
 2021, Vol. 35
2021, Vol. 35


