丙烯是重要的化工原料, 可以制备聚丙烯, 丙烯腈、丙烯酸及其酯类等化工产品[1]. 近年来随着丙烯需求的日益增长, 丙烷催化脱氢制丙烯作为一条有竞争力的油气清洁转化技术路线发展迅速[2]. 目前工业上丙烷脱氢催化剂主要包括两大类: 贵金属Pt催化剂和铬氧化物催化剂, 其分别面临价格昂贵和对环境存在污染的问题, 石油化工行业绿色低碳发展已经成为全球共识, 通过改进催化剂减少污染是绿色化工和环保技术的重要趋势. 科学界和工业界都迫切需要开发新型环保型非贵金属PDH催化剂[3-5]. 目前已经有多种金属及其氧化物催化剂, 如VOx[6]、CoOx[7]、Ga2O3[8]、MoOx[9]、ZnO[10]、InOx等已被报道存在一定的PDH活性, 但相较Pt、CrOx基催化剂性能仍有较大差距. 二氧化碳作为氧化剂辅助脱氢(CO2-PDH)被认为是更有前途的生产低碳烯烃的策略, 该方法满足绿色化学, 也符合“双碳”要求.
近年来, 铟基催化剂逐渐在PDH领域受到关注. Tan等[11-12]报道了通过调控铟-镓及铟-镓-铝复合氧化物的组成优化其丙烷脱氢催化性能, 最优的In/Ga/Al=5∶15∶80催化剂表现出17%的丙烷转化率和86%的丙烯选择性, 是In2O3-Ga2O3或In2O3-Al2O3二元氧化物活性的3倍以上. 结构表征数据表明复合氧化物的不同元素组成影响了催化剂的还原性以及酸强度, 提高还原性以及酸量有助于提升催化性能; 此外, In2O3在丙烷脱氢气氛中逐渐还原成金属态是该催化体系的主要失活原因之一. Yuan等[13]报道了通过浸渍法合成的In/CHA体系中, 铟可以与CHA沸石孔道内的质子H置换形成孤立的In+活性位. 不同于常规In2O3/SiO2催化剂, In/CHA体系的铟物种在反应中能够保持不被还原为金属态, 从而表现出突出的催化稳定性优势. 针对类似的In2O3/Al2O3体系, Chen等[14]通过关联H2、CO2预处理后催化剂的XPS和活性数据得出高分散的In2O3颗粒在反应中会被还原为金属In(In0), 其作为主要的脱氢位点; 而In2O3晶粒则作为逆水煤气变换反应的活性中心. 真实反应条件下的In0和In2O3协同作用催化丙烷脱氢与逆水煤气变换串联反应, 表现出了约30%丙烷转化率和75%丙烯选择性的优异催化性能. 随后, 该课题组进一步研究了In2O3催化CO2-PDH反应中的载体效应[15], XRD和TPR实验证明Al2O3和ZrO2载体相比SiO2能够促进铟活性相的分散, 从而提高丙烯收率. 此外, ZrO2载体能够促进CO2的吸附和活化, 有利于逆水煤气变换反应的发生, 表现出了最优的催化性能. 以上结果说明了铟基催化剂在丙烷脱氢反应中的潜在催化性能, 但PDH反应中真实的活性中心结构(即金属In还是高分散的InOx物种)尚未有明确的定论[11-14], 厘清真实活性位与构效关系对开发高效的铟基催化剂至关重要. 载体调控对铟活性相的催化性能也起着至关重要的作用. 相比氧化物载体, 分子筛具有大比表面积和高孔道有序度的显著优势, 是担载金属活性相用于丙烷脱氢反应的理想平台. 如肖丰收课题组[16-17]报道了基于分子筛限域效应构筑单原子B-OH活性位在丙烷脱氢中表现出优异的催化性能, Liu等[18]报道了小孔SSZ-13沸石的限域效应能够有效促进CO2分子的吸附与活化, 从而在CO2氧化乙烷脱氢反应中具有优异性能.
通过文献调研, 以分子筛为载体有望能提高In分散度从而提高其活化丙烷C-H键性能, 同时分子筛的孔道限域效应也有望促进CO2的吸附与活化. 因此, 构筑分子筛担载铟活性相催化剂预期能够在CO2-PDH反应中表现出优异的催化性能. 在乙烷氧化脱氢领域有较好效果的CHA沸石由于其较小的孔径(~0.38 nm[19])会限制丙烷分子(动力学直径~0.47 nm[20])的吸附与扩散. 相比之下, 中孔的silicalite-1分子筛具有高孔道连通度的十元环交叉孔道, 其孔径(0.56 × 0.51 nm)略大于丙烷的动力学直径, 能够为丙烷分子的吸附提供便利, 其孔道限域效应也能够对丙烷、CO2分子的活化起到一定的促进作用[18, 20]. 结合以上讨论, 推测silicalite-1担载In催化剂有望在CO2-PDH反应中表现出优异的催化性能. 因此, 通过不同的方法制备系列不同负载量和不同载体的掺杂铟的silicalite-1分子筛催化剂, 研究系列合成催化剂的结构、In含量、制备方法和载体对催化剂在PDH中活性的影响.
1 实验部分 1.1 实验原料CO2(99.999%)、CO(99.999%)、N2(99.999%)、H2(99.999%)、C3H8(5%, N2稀释), 北京华通精科气体化工有限公司生产. 硝酸铟五水合物(99.99%)、乙二胺(98%)、无水乙醇(99.7%)、四丙基氢氧化铵(25%水溶液)、正硅酸四乙酯(98%)均购自安耐吉化学有限公司; 商业Al-Beta分子筛(Si/Al比为40)购自南开催化剂厂; 去离子水为实验室自制.
1.2 催化剂的制备 1.2.1 Silicalite-1(S1)分子筛的合成将3 g TPAOH与15 g去离子水混合, 待溶解完全后加入8.32 g正硅酸乙酯, 连续搅拌6 h. 将所得混合物转移到高压釜中并在170 ℃条件下恒温72 h. 将产物冷却至室温后离心、洗涤, 之后在80 ℃下干燥12 h.最终, 在马弗炉中以2 ℃/min的加热速率加热至550 ℃, 并以此温度焙烧6 h, 最终产物记为S1.
1.2.2 浸渍法In/S1催化剂的合成称取一定质量的硝酸铟五水合物, 根据载体的饱和吸水量配置溶液. 称取1 g待浸渍S1载体, 将铟盐溶液缓慢滴加入载体中. 同时不断进行快速搅拌, 待浸渍液滴加完毕后将其置于80 ℃烘箱中干燥12 h. 将干燥后的样品放入马弗炉中, 在空气氛围下以2 ℃/min升温速度升至550 ℃并保持6 h. 焙烧结束后, 待样品冷却至室温回收样品, 得到浸渍质量分数分别为1%、3%、5%、7%、10%和20% 的系列In/S1样品.
1.2.3 水热法5In-S1催化剂的合成将0.33 g五水硝酸铟、0.1 g乙二胺与15 g去离子水混合, 搅拌至形成澄清溶液后依次加入8.32 g正硅酸乙酯、13 g四丙基氢氧化铵, 连续搅拌6 h. 将所得混合物转移至高压釜中, 随后水热、洗涤、焙烧过程与制备S1载体一致.
1.2.4 浸渍法5In/Si-Beta催化剂的合成称取1 g商业Si/Al为40的Beta分子筛放入烧杯中, 量取浓硝酸20 mL倒入装有分子筛的烧杯, 在80 ℃, 400 r/min搅拌6 h. 待混合液降至室温后, 分离、洗涤、焙烧样品, 即为Si-Beta分子筛. 随后采用浸渍法合成5In/Si-Beta催化剂, 合成方法与In/S1催化剂一致.
1.3 催化剂的表征利用荷兰纳科PANalytical B. V.公司生产的Empyrean型X-射线粉末衍射仪对样品进行晶相结构表征, 2θ扫描范围为5°~90 °, 扫描速度为5(°)/min. 利用FEI Tecnai G2 F20型透射电镜对样品进行形貌表征. Raman表征是在Renishaw inVa仪器上进行, 激发光源为325 nm. H2-TPR及CO2-TPD实验在湖南华思仪器上进行, 检测器为热导检测器(TCD), 升温速率为10 ℃/min, N2及H2/N2气体流量均为30 mL/min.
1.4 常压固定床反应器丙烷脱氢反应活性评价催化剂丙烷脱氢性能评价在微型固定床常压反应器上进行, 系统内压力为0.1 MPa. 称取0.3 g催化剂颗粒(粒径0.450~0.280 mm), 用石英棉固定在石英管中间, 反应管上下剩余部分用石英砂填充. 在氮气氛围下, 以20 ℃/min升温速度将催化剂从室温加热至反应温度(600 ℃), 并恒温处理30 min. 待温度稳定后, 通入反应气C3H8(5%(体积分数)余N2), 控制流量为20 mL/min, 催化剂与反应气进行反应. 二氧化碳氧化脱氢所用原料气为(5%(体积分数)C3H8, 1%~20%(体积分数)CO2余N2), 流量为20 mL/min. 为保证数据是在稳态下进行, 反应进行10 min后, 打开自动进样器取第1个数据点, 并用色谱(GC 9890B)对产物进行在线分析. 为了探究CO2的引入对催化性能的影响, 还对典型催化剂进行了CO2加氢活性的评价, 实验在600 ℃下进行, 催化剂用量为0.3 g, 反应气为10%(体积分数)CO2, 30%(体积分数)H2, 余N2, 总流速为20 mL/min.
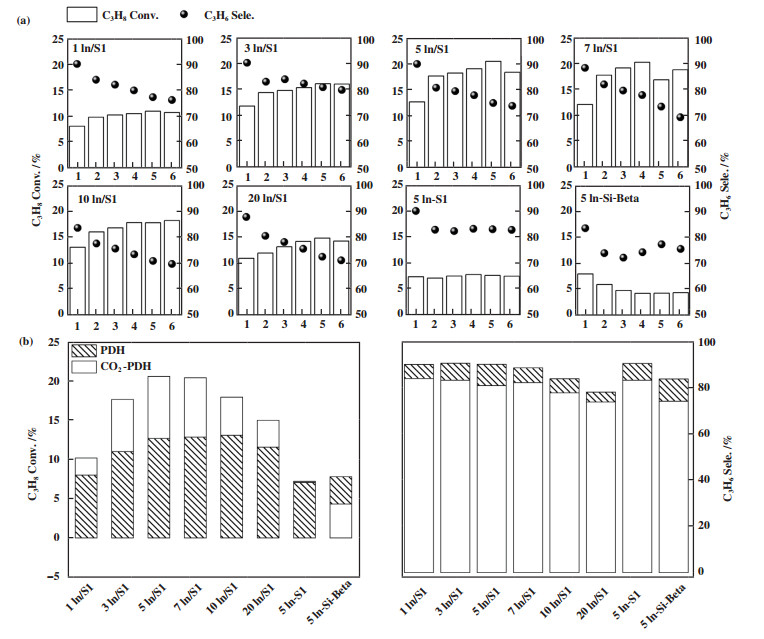
2 结果与讨论 2.1 铟基催化剂的丙烷脱氢反应性能 2.1.1 不同C3H8/CO2比例对催化丙烷脱氢活性的影响由图 1(a)可以看出, 各浸渍法制得的x In/S1催化剂中引入CO2对丙烷转化率均有较为明显的促进作用, 当C3H8∶CO2体积比为1∶1 ~ 1∶2时促进效果最为明显. 而水热法制得的5In-S1样品引入CO2对丙烷转化率无明显影响, 浸渍法制得的5In/Si-Beta样品引入CO2反而对丙烷转化率表现出了抑制效果. 以上各催化剂中引入CO2均造成了丙烯选择性有不同程度的降低. 我们将各催化剂在无CO2时的PDH数据与最佳C3H8/CO2比例时的CO2-PDH活性数据汇总得到图 1(b)进行分析如下.
|
图 1 (a)系列催化剂在不同C3H8/CO2原料气配比下的CO2-PDH催化活性; (b)各催化剂在无CO2及最优C3H8/CO2配比条件下的活性对比结果 Fig.1 (a) The catalytic activity over series catalysts under different C3H8/CO2 ratios, operating at 600 ℃, using 0.3 g catalysts; (1) 5%(volume fraction) C3H8, (2) 5%(volume fraction) C3H8-1%(volume fraction) CO2, (3) 5%(volume fraction) C3H8-2.5%(volume fraction) CO2, (4) 5%(volume fraction) C3H8-5%(volume fraction) CO2, 5%(volume fraction) C3H8-10%(volume fraction) CO2, 6 mL C3H8-20%(volume fraction) CO2; (b) The activity results under no CO2 co-feed and optimized C3H8/CO2 ratios |
如图 1(b)所示, 对于以S1为载体的系列浸渍法合成催化剂, 无论是否通入CO2, 铟负载量的改变对PDH反应的丙烷转化率的影响趋势是一致的. 随着铟负载量由1%增加至5%(质量分数), PDH反应的丙烷转化率逐渐增加, 由约7%增至约13%, 这证明In是系列In/S1催化剂的活性相; 但当In负载量由5%进一步增加至7%(质量分数)时, PDH反应的丙烷转化率波动很小, 基本保持在13%左右, 随着In负载量由7%进一步增加至20%(质量分数)时, PDH反应的丙烷转化率甚至开始下降, 这说明高于5%(质量分数)的In负载量对丙烷转化率无明显贡献甚至表现出抑制作用. 因此对于PDH反应而言, 5%(质量分数)是最佳的In负载量.
2.1.3 不同制备方法对丙烷脱氢反应性能的影响通过一锅水热法合成的5In-S1催化剂(In投料量为5%(质量分数), 与5In/S1相同), 其在无CO2条件下的丙烷转化率约为7%, 低于通过浸渍法合成的5In/S1催化剂(转化率约为12%). 特别的是, CO2的引入并未对一锅水热法合成的5In-S1催化的PDH反应的丙烷转化率起到促进作用. 此外, 通过浸渍法合成的5In/Si-Beta催化剂上CO2的引入也未起到促进作用.
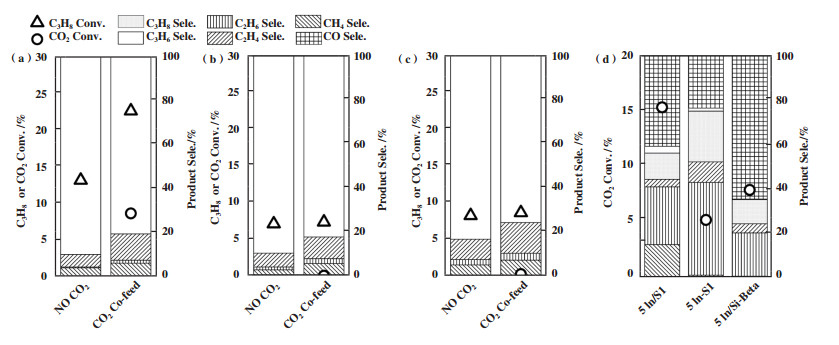
2.2 不同载体和制备方法对铟基催化剂的活性影响根据上述活性数据, 选取Silicalite-1(S1)为载体的一锅水热法5In-S1催化剂和浸渍法合成的5In/S1催化剂, 以及Si-Beta为载体的浸渍法5In/Si-Beta为代表催化剂, 研究它们对丙烷和二氧化碳分子活化能力的影响. 如图 2(a)-(c)所示, 5In/S1催化剂上CO2转化率约为8%, 而其它两个催化剂并无CO2活化能力(CO2转化率接近0), 上述结果说明了5In/S1能够活化CO2分子, 从而在CO2分子引入后提高丙烷转化率. 此外, 这3种催化剂催化PDH及CO2-PDH反应的产物中甲烷选择性均约为乙烷+乙烯选择性的30%~50%, 类似的产物分布情况也在PtSn-Beta、Na-Cr2O3/Al2O3、ZnO/AlN、Co-MCM-41、In2O3-Ga2O3-Al2O3体系中有报道[2, 12, 20-22]. 结合先前工作报道的丙烷脱氢各基元反应的活化能[23-24], 我们推测该工作中副反应的路径主要为丙烷在催化剂上生成丙基、丙烯中间体, 后可能发生C-C键裂解反应生成乙烯、乙基中间体, 同时伴随生成甲基中间体, 这些甲基中间体既有可能加氢生成CH4, 也有可能发生C-C偶联反应生成乙烷或乙烯, 因此导致甲烷的选择性低于乙烷和乙烯选择性之和.
|
图 2 (a)5In/S1;(b)5In-S1;(c)5In/Si-Beta 3种典型催化剂的纯PDH及CO2-PDH活性对比; (d)三者的二氧化碳加氢活性对比 Fig.2 The activity comparison of (a) 5In/S1; (b) 5In-S1; (c) 5In/Beta under PDH and CO2-PDH; (d) The CO2 hydrogenation activity and product distribution |
我们进一步对这上述3种典型催化剂的CO2加氢活性进行了评价, 如图 2(d)所示, 3种催化剂上CO2的转化率遵循5In/S1 > 5In/Si-Beta > 5In-S1, 3种催化剂上产物分布则以乙烷和CO为主. 其中, 5In/S1和5In-S1两个催化剂上乙烷选择性高于5In/Si-Beta样品, 这可能是由于MFI拓扑结构的S1具有更小的十元环孔道, 产生一定的限域效应能促进多碳产物的生成.
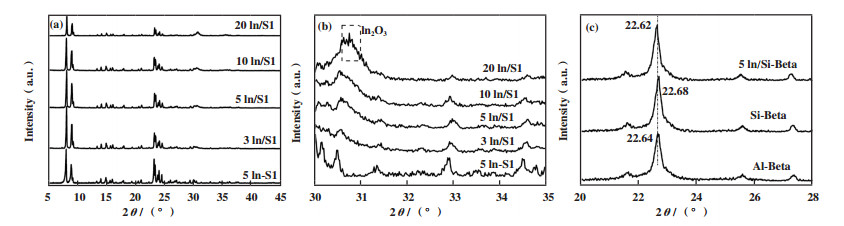
2.3 催化剂的物化性质表征 2.3.1 X射线衍射(XRD)表征从图 3(a)-(b)不同In含量及不同合成方法合成的系列5In/S1及5In-S1催化剂的广角XRD谱图中可以看出, 在2θ角位于7.96°、8.82°、23.12°、23.99°和24.47°处均表现出特征衍射峰, 证明其具有良好的MFI分子筛晶体结构[25]. 对30°~35°范围内的XRD谱图进行放大发现, 仅在20In/S1样品中观察到位于30.6 °附近归属于In2O3晶体的衍射峰, 证明当In浸渍量达到20%(质量分数)时才会生成大颗粒的In2O3晶粒, 低于该负载量时In2O3尺寸较小[26]. 从图 3(c)的Al-Beta、Si-Beta及5In/Si-Beta的小角谱图可以看出, 商业Al-Beta载体经过硝酸脱铝处理后, 其2θ角在22.64 °处的特征峰略微向高角度方向偏移, 归因于骨架Al的脱除导致分子筛晶胞收缩, 而再浸渍In后5In/Si-Beta催化剂的特征峰则又相比Si-Beta载体向低角度偏移至22.62 °, 可以归因于In部分进入Si-Beta分子筛的骨架, 导致晶胞出现一定程度的膨胀[27].
|
图 3 催化剂的XRD谱图 Fig.3 The XRD patterns of various catalysts |
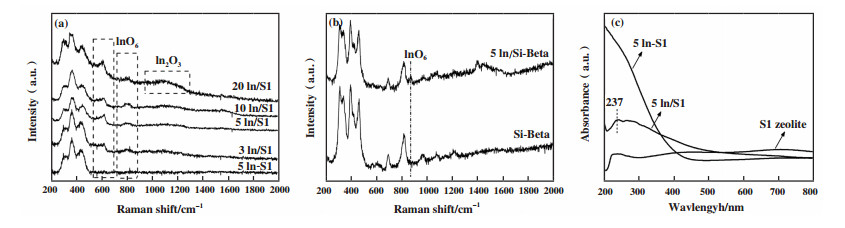
通过拉曼光谱对所合成系列催化剂的精细结构进行了表征, 对于系列以S1为载体的催化剂, 从图 4可以看出, 200~450 cm-1范围内存在3个特征峰, 可归因为MFI沸石中的Si-O-Si物种[28], 在各个样品中均可观察到. 在600及800 cm-1处的特征峰, 可归因为高分散In2O3中的InO6物种, 而位于1100 cm-1附近的特征峰则归属于In2O3晶粒[29], 上述3种特征峰中前两者仅在浸渍法合成的催化剂中存在, 而In2O3物种的特征峰则仅出现于20In/S1催化剂. 结果表明浸渍法合成的系列催化剂中存在In2O3颗粒. 而水热合成的5In-S1催化剂中不含上述特征峰, 证明In可能以单位点形式存在, 不存在颗粒或团簇. 为了进一步探究5In-S1以及5In/S1催化剂中的铟物种状态, 我们对该两种催化剂进行了UV-vis DRS表征. 相比纯S1载体无明显吸收峰, 5In/S1催化剂在中心位于波长237 nm处出现了较宽的吸收峰, 可以归属为该催化剂中的In2O3颗粒或团簇[30]. 水热的5In-S1催化剂中可以观察到 < 200 nm处存在特征吸收峰, 该特征峰常被归属为分子筛骨架中的孤立四配位金属杂原子[28], 因此我们推测5In-S1催化剂中In成功嵌入到了S1分子筛骨架中. 此外, 5In/Si-Beta样品相比Si-Beta载体也出现了位于820 cm-1处的特征峰, 可以归属于InO6物种. 以上结果说明浸渍法合成的In/S1及In/Si-Beta催化剂中存在In2O3颗粒, 而水热合成的5In-S1催化剂则无此结构, 推测其中In可能以单位点形式存在.
|
图 4 催化剂的(a)-(b)Raman以及(c)紫外可见漫反射吸收光谱图 Fig.4 The (a)-(b) Raman and (c) UV-vis DR spectra of various catalysts |
通过扫描及透射电镜探究了代表型5In-S1及5In/S1催化剂的微观形貌. 图 5(a)-(b)的扫描电镜图像说明两者均表现出典型S1分子筛的六棱柱形貌, 尺寸均约为200 nm. 右侧的SEM-EDX图像说明了两个样品中均含有Si, In元素, 且两者均匀分散. 通过积分得知5In-S1, 5In/S1催化剂中In元素含量分别为3.90%以及4.77%(质量分数). 为进一步探究In的分布及存在形式, 补充了两者的TEM图像. 5In-S1催化剂(图 5(c))中未观察到明显的In颗粒或团簇, 而对比的5In/S1催化剂中则观察到了明显的尺寸约为3~5 nm的颗粒(图 5(d)中黄色圈区域). 结合上述Raman、UV-vis表征推测其为担载的In2O3活性相, 而水热法5In-S1样品未观察到明显的金属颗粒或团簇, 这也与Raman表征中其不含InO6特征峰的结果相一致, 结合图 5(a)的元素扫描中In活性相的均匀分布推测其In活性相主要以单位点形式存在.

|
图 5 (a), (c)5In-S1及(b), (d)5In/S1催化剂的扫描电镜及透射电镜表征 Fig.5 The FESEM, SEM-EDX and TEM images of (a), (c) 5In-S1 and (b), (d) 5In/S1 |
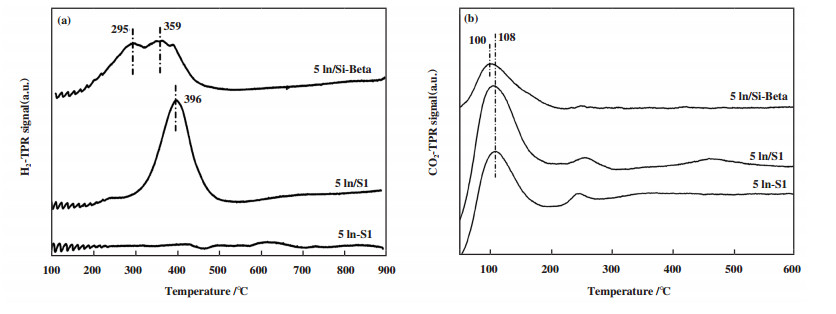
图 6为5In-S1、5In/S1及5In/Si-Beta催化剂的H2-TPR谱图和CO2-TPD谱图, 从H2-TPR谱图中可以看出, 每个催化剂有不同的还原性能, 浸渍合成的5In/S1及5In/Si-Beta样品中出现了位于600 ℃以前的还原峰, 表明活性评价所用的600 ℃条件下, 以上两个催化剂中的In位点能够发生氧化还原循环. 而水热合成的5In-S1则到900 ℃均无可见的还原峰, 证明该催化剂中的In不可被H2还原[12-13]. 结合活性评价及XRD、Raman表征结果可以推断, 浸渍合成的5In/S1催化剂含有In2O3颗粒, 其可以发生氧化还原循环, 因此可以活化CO2分子. 催化剂的孔道大小可以显著影响催化剂的吸附能力, 图 6中的CO2-TPD谱图表明, 具有十元环孔道的5In/S1及5In-S1中具有位于108和250 ℃的两个脱附峰, 而十二元环孔道的5In/Si-Beta催化剂则仅具有位于100 ℃的脱附峰, 其结果表明, 具有更小孔道的S1载体对于CO2具有更强的吸附能力, 也可以一定程度上促进CO2的吸附与活化.
|
图 6 (a)H2-TPR和(b)CO2-TPD谱图 Fig.6 The (a) H2-TPR and (b) CO2-TPD spectra of catalysts |
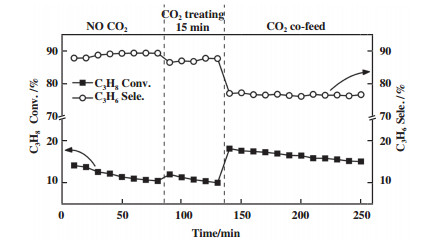
为了进一步探究反应构效关系, 选取了具有最高活性的5In/S1催化剂进行了不同反应气氛下的活性评价. 从图 7可以发现, 当无CO2通入时, 其丙烷转化率逐渐由14%降低至10%. 随后用CO2处理催化剂15 min, 发现丙烷转化率升高至13%, 随后随着反应进行丙烷转化率又逐渐降低至9%. 当采取CO2共进料时, 丙烷转化率明显升高至19%. 根据以上结果作者推测, In2O3能够发生氧化还原循环, 即被H2还原的同时被CO2氧化, 在该氧化还原循环中可以活化丙烷分子C-H键与CO2分子C=O键, 因此表现出了CO2氧化丙烷脱氢催化性能, 相比Beta分子筛, S1分子筛具有合适的孔道大小, 一定程度上能够促进反应物分子特别是CO2的吸附与活化, 因此5In/S1相比5In/Si-Beta表现出了更优的CO2氧化丙烷脱氢性能.
|
图 7 不同反应气氛下5In/S1催化剂的催化性能 Fig.7 The catalytic activity of optimized 5In/S1 under different reaction conditions |
扫描电镜和Raman表征表明, In/S1催化剂(浸渍法合成)中含有In2O3物种, 该活性物种是In基催化剂具备CO2氧化丙烷脱氢活性的关键. In-S1催化剂(水热法合成)中In主要以单位点形式存在, 不具备CO2氧化丙烷脱氢能力.
3.2用浸渍法合成的铟负载量1%~20%的系列In/S1催化剂中, 当负载量由1%提高至10%时, 其丙烷初始转化率升高, 引入二氧化碳的提升效果也增大, 负载量为5%~7%时达到峰值, 进一步增加负载量会导致活性降低.
3.3CO2-TPD表明, 5In/S1催化剂(浸渍法合成)比5In/Si-Beta催化剂(浸渍法合成)表现出了更优的丙烷转化率及CO2促进效果, 说明孔道尺寸越小的S1载体限域作用越强, 越能促进丙烷分子、CO2分子的吸附和活化.
3.4H2-TPR和CO2-TPD结合活性评价及XRD、Raman表征表明In2O3物种在600 ℃下可以发生氧化还原循环, 在循环过程中完成了对丙烷分子及CO2分子的活化.
| [1] |
Liu Meng-yang (刘梦洋), Rong Xin (荣欣), Gu Bin (顾彬), et al. Propane dehydrogenation of Pt-Sn metal loadedon aluminum-boron composite oxide(铝硼复合氧化物负载Pt-Sn催化剂的丙烷脱氢性能研究)[J]. J Mol Catal(China) (分子催化), 2019, 33(5): 412-419.
|
| [2] |
Zhang Jin-he (张金赫), Zhang Chang-wu (张昌武), WangXin-ge (王新鸽), et al. Self-hydrolysis-driven synthesis of nanocrystalline aluminum nitride supported platinum-zinc catalyst for propane dehydrogenation(自水解驱动PtZn/纳米AlN催化剂的合成及其丙烷脱氢性能研究)[J]. J Mol Catal (China) (分子催化), 2021, 35(5): 395-403.
|
| [3] |
Hu Z P, Yang D, Wang Z, et al. State-of-the-art catalysts for direct dehydrogenation of propane to propylene[J]. Chin J Catal, 2019, 40(9): 1233–1254.
DOI:10.1016/S1872-2067(19)63360-7 |
| [4] |
Sattler J J H B, Ruiz-Martinez J, Santillan-Jimenez E, et al. Catalytic dehydrogenation of light alkanes on metals and metal oxides[J]. Chem Rev, 2014, 114(20): 10613–10653.
DOI:10.1021/cr5002436 |
| [5] |
Zhang Suo-jiang (张锁江), Zhang Xiang-ping (张香平), Ge Wei (葛蔚), et al. Carbon neutral transformative technol-ogies for industrial process(工业过程绿色低碳技术)[J]. Bull Chin Academy Sci(China)(中国科学院院刊), 2022, 37(4): 511-521.
|
| [6] |
Chen C, Sun M, Hu Z, et al. Nature of active phase of VOx catalysts supported on SiBeta for direct dehydroge-nation of propane to propylene[J]. Chin J Catal, 2020, 41(2): 276–285.
DOI:10.1016/S1872-2067(19)63444-3 |
| [7] |
Hu B, Schweitzer N M, Das U, et al. Selective propane dehydrogenation with single-site Co(Ⅱ) on SiO2 by a non-redox mechanism[J]. J Catal, 2015, 322: 24–37.
DOI:10.1016/j.jcat.2014.10.018 |
| [8] |
Liu Y, Zhang G, Wang J, et al. Promoting propane dehydrogenation with CO2 over Ga2O3/SiO2 by eliminating Ga-hydrides[J]. Chin J Catal, 2021, 42(12): 2225–2233.
DOI:10.1016/S1872-2067(21)63900-1 |
| [9] |
Shao Huai-qi (邵怀启), Zhong Shun-he (钟顺和). MoO3-V2O5/SiO2 catalyst for oxidative dehydrogenation of propane with CO2(CO2氧化丙烷脱氢MoO3-V2O5/SiO2催化剂研究)[J]. J Mol Catal (China) (分子催化), 2004, 18(2): 87-92.
|
| [10] |
Liu G, Zeng L, Zhao Z J, et al. Platinum-modified ZnO/Al2O3 for propane dehydrogenation: Minimized platinum usage and improved catalytic stability[J]. ACS Catal, 2016, 6(4): 2158–2162.
DOI:10.1021/acscatal.5b02878 |
| [11] |
Tan S, Gil L B, Subramanian N, et al. Catalytic propane dehydrogenation over In2O3-Ga2O3 mixed oxides[J]. Appl Catal, A, 2015, 498: 167-175.
|
| [12] |
Tan S, Kim S J, Moore J S, et al. Propane dehydroge-nation over In2O3-Ga2O3-Al2O3 mixed oxides[J]. ChemCatChem, 2016, 8(1): 214–221.
DOI:10.1002/cctc.201500916 |
| [13] |
Yuan Y, Lobo R F. Propane dehydrogenation over extra-framework In(Ⅰ) in chabazite zeolites[J]. Chem Sci, 2022, 13(10): 2954–2964.
DOI:10.1039/D1SC05866E |
| [14] |
Chen M, Xu J, Cao Y, et al. Dehydrogenation of propane over In2O3-Al2O3 mixed oxide in the presence of carbon dioxide[J]. J Catal, 2010, 272(1): 101–108.
DOI:10.1016/j.jcat.2010.03.007 |
| [15] |
Chen M, Wu J L, Liu Y M, et al. Study in support effect of In2O3/MOx (M= Al, Si, Zr) catalysts for dehydrogenation of propane in the presence of CO2[J]. Appl Catal, A, 2011, 407(1/2): 20-28.
|
| [16] |
Zhou H, Yi X, Hui Y, et al. Isolated boron in zeolite for oxidative dehydrogenation of propane[J]. Science, 2021, 372(6537): 76–80.
DOI:10.1126/science.abe7935 |
| [17] |
Wang H, Wang L, Xiao F S. Metal@ zeolite hybrid materials for catalysis[J]. ACS Cent Sci, 2020, 6(10): 1685–1697.
DOI:10.1021/acscentsci.0c01130 |
| [18] |
Liu J, He N, Zhang Z, et al. Highly-dispersed zinc species on zeolites for the continuous and selective dehydrogenation of ethane with CO2 as a Soft Oxidant[J]. ACS Catal, 2021, 11(5): 2819–2830.
DOI:10.1021/acscatal.1c00126 |
| [19] |
Kalipcilar H, Bowen T C, Noble R D, et al. Synthesis and separation performance of SSZ-13 zeolite membranes on tubular supports[J]. Chem Mater, 2002, 14(8): 3458–3464.
DOI:10.1021/cm020248i |
| [20] |
Ingale P, Knemeyer K, Preikschas P, et al. Design of PtZn nanoalloy catalysts for propane dehydrogenation through interface tailoring via atomic layer deposition[J]. Catal Sci Technol, 2021, 11(2): 484–493.
DOI:10.1039/D0CY01528H |
| [21] |
Gao Y, Peng L, Long J, et al. Hydrogen pre-reduction determined Co-silica interaction and performance of cobalt catalysts for propane dehydrogenation[J]. Micro Mes Mater, 2021, 323: 111187.
DOI:10.1016/j.micromeso.2021.111187 |
| [22] |
Ma Y, Chen X, Guan Y, et al. Skeleton-Sn anchoring isolated Pt site to confine subnanometric clusters within *BEA topology[J]. J Catal, 2021, 397: 44–57.
DOI:10.1016/j.jcat.2021.03.022 |
| [23] |
Sun S, Sun G, Pei C, et al. Origin of performances of Pt/Cu single-atom alloy catalysts for propane dehydrogen-ation[J]. J Phys Chem C, 2021, 125(34): 18708–18716.
DOI:10.1021/acs.jpcc.1c04295 |
| [24] |
Yang M L, Zhu Y A, Fan C, et al. DFT study of propane dehydrogenation on Pt catalyst: Effects of step sites[J]. Phys Chem Chem Phys, 2011, 13(8): 3257–3267.
DOI:10.1039/c0cp00341g |
| [25] |
Wang Y, Hu Z P, Lu X, et al. Ultrasmall PtZn bimetallic nanoclusters encapsulated in silicalite-1 zeolite with superior performance for propane dehydrogenation[J]. J Catal, 2020, 385: 61–69.
DOI:10.1016/j.jcat.2020.02.019 |
| [26] |
O'Connell K, Regalbuto J R. High sensitivity silicon slit detectors for 1 nm powder XRD size detection limit[J]. Catal Lett, 2015, 145(3): 777–783.
DOI:10.1007/s10562-015-1479-6 |
| [27] |
Chen C, Zhang S, Wang Z, et al. Ultrasmall Co confined in the silanols of dealuminated beta zeolite: A highly active and selective catalyst for direct dehydrogenation of propane to propylene[J]. J Catal, 2020, 383: 77–87.
DOI:10.1016/j.jcat.2019.12.037 |
| [28] |
Fan F, Feng Z, Li C. UV Raman spectroscopic studies on active sites and synthesis mechanisms of transition metal-containing microporous and mesoporous materials[J]. Acc Chem Res, 2010, 43(3): 378–387.
DOI:10.1021/ar900210g |
| [29] |
Shao M, Chen H, Shen M, et al. Synthesis and photocat-alytic properties of In2O3 micro/nanostructures with different morphologies[J]. Coll Surf, A, 2017, 529: 503-507.
|
| [30] |
Serykh A I. Low-dimensional indium oxo-species on the surface of In2O3/Al2O3 catalytic material: the sites of dissociative adsorption of hydrogen[J]. J Phys Chem C, 2016, 120(38): 21436–21440.
DOI:10.1021/acs.jpcc.6b05681 |
 2022, Vol. 36
2022, Vol. 36

