2. 兰州理工大学 石油化工学院, 甘肃 兰州 730050
2. School of Petroleum and Chemical, Lanzhou University of Technology, Lanzhou 730050, China
近年来, 经由各类污染源排放的挥发性有机化合物(VOCs)受到了人们的广泛关注, 这类污染物种类繁多, 能直接导致PM2.5、光化学烟雾等细颗粒物的形成[1−2], 对环境造成了严重危害. 同时, 大多数VOCs都具有毒性, 容易对人体健康产生危害[3]. 当前VOCs的降解手段主要是针对废气排放的末端治理[2], 其中常用的降解技术便是催化氧化法, 能够在较低的温度下将VOCs分解为无毒无害的CO2和H2O[4]. 催化氧化法的核心在于催化剂, 其催化性能的优劣会直接影响污染物的降解效率. VOCs催化燃烧催化剂根据活性组分的不同主要分为两大类: 以能够高效活化反应物的贵金属(Pt、Pd、Au、Ru等)为活性物种的贵金属催化剂和以储量较大的非贵金属为活性中心的非贵金属催化剂. 由于非贵金属具有价态多变, 易形成多种类型氧化物且较为经济等特点[5], 因而目前的研究以贵金属掺杂非贵金属、多种非贵金属共掺杂等途径为主. 相比于只含单一金属元素的催化剂, 这些复合催化剂能将各类金属的优点结合起来, 更好地提升活性、稳定性及抗硫性等重要性能, 同时也能在一定程度上降低催化剂的成本[6].
然而在实际生产生活中, 污染源排放的废气成分往往比较复杂, 由燃料燃烧等途径产生的SO2不仅自身就是一类污染物, 而且还会对用于降解废气的催化剂造成严重的影响: 一方面, SO2易与反应物分子竞争吸附在催化剂的活性位点上, 降低催化氧化反应的效率, 造成催化剂的暂时失活; 另一方面, 若SO2分子与催化剂的活性位点或载体发生化学反应, 生成的硫酸盐物种沉积在催化剂上时, 则会造成催化剂的永久中毒失活. 因此设计与制备出具有良好耐SO2中毒性能的VOCs氧化催化剂是非常有必要的. 本综述归纳了催化剂的SO2中毒机理, 根据不同的中毒原因重点总结了贵金属及非贵金属催化剂针对性的抗SO2中毒策略, 并提出了目前VOCs催化燃烧领域中催化剂抗SO2中毒需要改进的方向, 对未来催化剂的发展进行了展望.
1 催化剂SO2中毒机理一般来说, 反应气氛中SO2的存在带来的负面影响主要是硫物种在催化剂表面的吸附及硫酸盐物种的形成, 这可能导致活性位点的团聚与损失或载体的中毒硫酸化等, 从而造成催化剂的可逆失活或不可逆失活.
1.1 活性位点上SO2与反应物的竞争吸附SO2通常会吸附在催化剂的活性位点上, 这种竞争行为阻碍了反应物分子与催化剂的接触, 直接影响了催化氧化反应的效率. 以应用广泛且具有优异性能的Pt基催化剂为例[7], SO2的强电负性可以通过诱导电子转移从而降低Pt d轨道的电子云密度, 进而抑制VOCs的吸附[8]. 有研究认为, 贵金属Pt对SO2具有较强的物理吸附作用, 在含SO2气氛的甲苯催化燃烧过程中, SO2不与贵金属Pt反应形成硫酸铂物种, 只是强吸附覆盖了Pt活性位点, 但催化活性依然会受到严重影响[9], 但若催化剂与吸附硫物种的相互作用不强, 或载体的结构与性能较好, 也能促使覆盖在催化剂表面的硫物种出现解吸行为, 这就形成了催化剂的可逆失活.
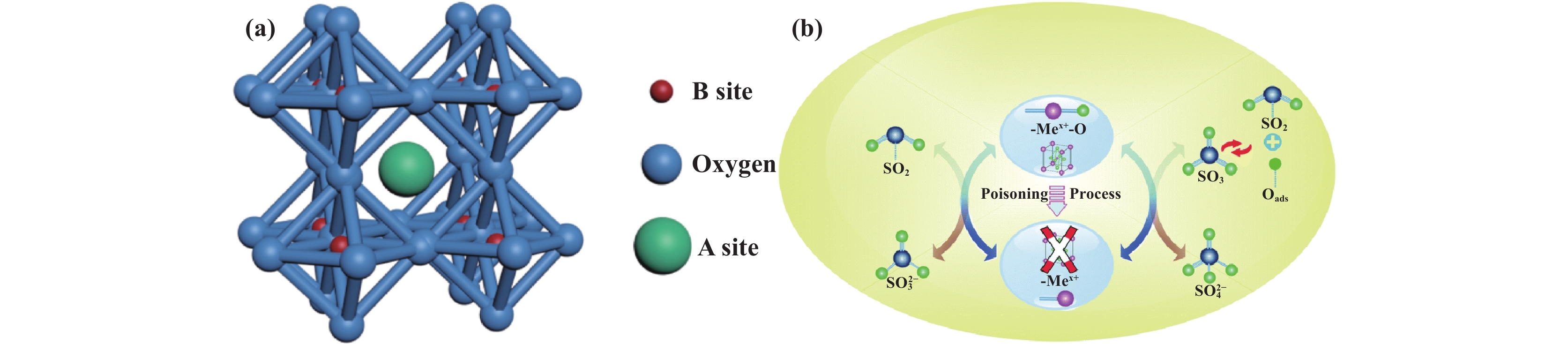
1.2 活性位点上硫酸盐或亚硫酸盐物种的生成催化剂的活性位点较易受到外部环境的干扰, 强吸附的SO2可以与活性金属物种发生反应生成硫酸盐或亚硫酸盐, 致使活性位点中毒. 如Pd系催化剂, 虽具有良好的耐热性和耐烧结性[7], 但对硫物种的敏感性却很高[10], 废气中的SO2在Pd基催化剂上会强烈抑制VOCs的氧化[11]. 这是由于贵金属Pd物种的活性组分不仅容易吸附SO2, 还能与SO2反应生成稳定的硫酸钯物种, 使催化剂产生不可逆的中毒失活[9]. 有研究发现, SO2的抑制作用表现为PdO-SO3配合物的形成从而使甲烷氧化反应活化能增加[12]. 尽管硫酸盐配合物对甲烷仍有一定的氧化性, 但其活性明显低于PdO, Pd基催化剂依然会很快失活. 而类似的结果在VOCs的催化氧化中也得到了体现[13−14]. 此类催化剂活性物种如果对SO2比较敏感, 不仅易吸附SO2, 更易与其反应生成硫酸盐物种将活性位点覆盖, 若吸附的硫物种与催化剂相互作用较强, 则很难在停止SO2通入后使其解吸, 从而造成催化剂不可逆失活. 在非贵金属催化剂中, 有一类具有结构稳定性高、热稳定好等优点的钙钛矿型催化剂(图1(a))[15], 该类催化剂的SO2中毒行为主要是通过生成硫酸盐从而破坏钙钛矿结构使其性能变差. 气态SO2会首先吸附在其表面的阴离子空位上, 随着SO2的持续氧化进而反应生成亚硫酸盐和硫酸盐. 以LaCoO3钙钛矿为例(图1(b))[16], 在初始阶段, SO2会扩散到催化剂中, 可能会反应生成La2(SO4)3、La2(SO3)3、La2O2SO4、CoO等物质, 导致催化剂的比表面积、孔容等物理性质发生轻微变化. 但此时钙钛矿结构未破坏, 大部分活性组分也未失活. 而当SO42−与钙钛矿相互作用进一步形成大量的硫酸镧物种时, 则会破坏钙钛矿的结构, 导致不可逆中毒, 严重影响催化剂的性能.
|
图 1 (a)钙钛矿结构示意图[15]; (b) ABO3钙钛矿的SO2中毒机理[16] Fig.1 (a) Schematic diagram of perovskite structure[15]; (b) Poisoning mechanism of SO2 on ABO3 perovskite[16] |
催化剂所选用的不同载体对SO2具有不一样的敏感性, 如果使用一些性质稳定的惰性材料如SiO2等作为载体时, SO2便很难与这类酸性载体进行反应. 相反, CeO2这种具有较强的氧化还原能力且易与气态SO2结合生成硫酸盐的物质被用作载体时, 则非常容易出现SO2中毒的现象. 如沉积在CeO2上的Pt基催化剂虽通常具有较高的氧化活性, 但由于CeO2易在SO2的存在下转化为硫酸铈, 因而也能导致催化剂活性的明显下降[17].
另外, 使催化剂产生硫中毒行为的常见硫物种除了SO2, 还有H2S、硫醇、噻吩等物质, 这些硫物种的沉积也会导致催化剂的中毒失活[18−19]. 例如, H2S会吸附在Ni基催化剂的活性位点上致使其失活, 但通常情况下人们会选择添加另一种化合物或贵金属以此来稳定含硫气氛中的Ni物种[20]; 甲硫醇能附着在CeO2的高活性氧上, 随后会生成H2S继续与氧反应, 最后生成Ce2S3组分令催化剂失活. 有研究通过降低Ce周围的氧配位数从而减少了催化剂表面的高活性氧, 避免了其从甲硫醇或H2S中捕获大量的硫物种[21]. 由此可见, 提升催化剂的抗硫中毒性能是非常重要的.
相对来说, SO2在VOCs中是较为普遍存在的有害硫物种, 且SO2对于催化剂的毒化与侵蚀是严重且深远的. 根据前人研究[8,22]中描述的硫物种对催化剂的影响机制来看, 无论是SO2存在导致的电子效应、SO2在催化剂上的竞争吸附, 还是催化剂表面或载体上硫酸盐的形成等行为所产生的中毒, 均与催化剂的结构组成、性质及载体的选择等有关. 因此, 提升催化剂抗SO2中毒能力的措施也是多样化的, 对其进行活性组分、载体和结构上抑制SO2的竞争吸附和反应的针对性改性是非常必要的.
2 催化剂抗SO2中毒策略 2.1 贵金属催化剂贵金属元素具有较多参与配位的d轨道电子, 容易与反应物形成配位键, 从而高效地活化反应物质. 在VOCs的催化燃烧领域中, 应用较多的贵金属催化剂为Pt系和Pd系. Pt系催化剂往往具有较高的活性和选择性, 近年来人们也常通过减小Pt金属颗粒尺寸的方式来更好地提升催化剂的性能. 但SO2往往很容易强吸附到Pt活性位点上, 严重阻碍了Pt对VOCs的吸附活化. Pd系催化剂相较于Pt系催化剂表现出了更好的耐热性和耐烧结性, 且价格更为低廉[7]. 一般情况下, 负载型Pd基催化剂上PdO的活性作用要优于金属Pd[23], 但SO2的氧化行为能消耗PdO相表面的晶格氧, 使Pd类活性组分易与SO2反应形成稳定的硫酸盐, 致使催化剂产生不可逆的中毒失活.
2.1.1 构建双金属体系双金属体系一般是将两种不同的贵金属共同负载或沉积在同一载体上, 使二者之间产生协同效应, 有助于提升催化剂的催化燃烧活性和抗SO2中毒能力. 由于Pt物种对SO2的敏感度没有Pd物种那么高, 因此关于Pt-Pd双金属体系的构建较多[24]. 适量贵金属Pt的添加不仅有助于减少硫酸盐在Pd物种上的富集, 还能提高Pd基催化剂的活性[25]. 研究发现, Pt-Pd之间的电子传递效应可以有效缓解Pd基催化剂的SO2中毒现象. Yang等[9]采用初湿浸渍法制备的Pd-Pt/γ-Al2O3双金属催化剂在甲苯的催化氧化反应中展现出了优异的活性和抗SO2中毒能力. XPS结果证明加入少量Pt可以提高Pd基催化剂中的Pd2+/Pd0比, 这可能是Pt和Pd之间的电子调制效应促使了部分Pd0相向PdO相的转变, 增加了催化剂中PdO的数量. 当反应气氛中有SO2存在时, 活性组分对SO2的吸附性能会减弱, 从而有效阻止了Pd物种与SO2发生反应, 使催化剂具有良好的抗SO2中毒性能. 同时, SO2-TPD结果发现, Pd-Pt/γ-Al2O3催化剂在290 ℃左右时硫酸钯的热分解峰面积明显小于Pd/γ-Al2O3, 再次验证了Pt和Pd之间的电子调制减少了Pd类活性组分与SO2反应产生硫酸盐的数量. 此外, 作者的另一项研究[26]也使用了贵金属Pt来调节Pd的电子结构以改善Pd基催化剂的性能. 硫化后的Pd-Pt/γ-Al2O3催化剂在甲苯催化燃烧过程中表现出了明显的抗中毒效果, SO2-TPD与XPS测试结果证实Pd-Pt/γ-Al2O3催化剂中Pt将电子转移给Pd, 使得Pd很难得到电子与SO2反应. 而Pd较好的供氧性能会使更多的SO2被氧化成SO3, 更容易与载体γ-Al2O3反应形成硫酸铝, 而非与贵金属Pd活性位点形成硫酸钯.
由此可见, Pt物种的加入能显著影响到Pd基催化剂的性能, 两种金属之间的电子调制效应不仅提升了催化剂的氧化活性, 还缓解了由活性Pd物种与SO2的反应导致的中毒失活. 而由这两种金属共同添加形成的双金属体系中的Pt∶Pd含量之比也是影响催化剂性能的一个重要变量. Huang等[10]通过调整不同的Pt∶Pd摩尔比, 发现高比例的Pt0.2Pd0.8/CeO2催化剂具有最佳的活性和抗SO2中毒性能: 其在丙烯催化燃烧中的T50仅有170 ℃, 催化剂起燃温度的降低是由于Pt与Pd之间良好的协同效应. 当在反应气氛中通入SO2时, 抗性测试和活性受SO2影响程度的定量分析结果均表明Pt0.2Pd0.8/CeO2催化剂拥有更好的抗中毒性能. 两种金属的不同含量能影响到催化剂的表面活性氧数量. 当SO2的强吸附阻碍了催化剂对气相氧的利用并使催化剂活性变差时, 高比例的Pt-Pd催化剂因含有更丰富的表面活性氧从而显著减弱了SO2带来的影响.
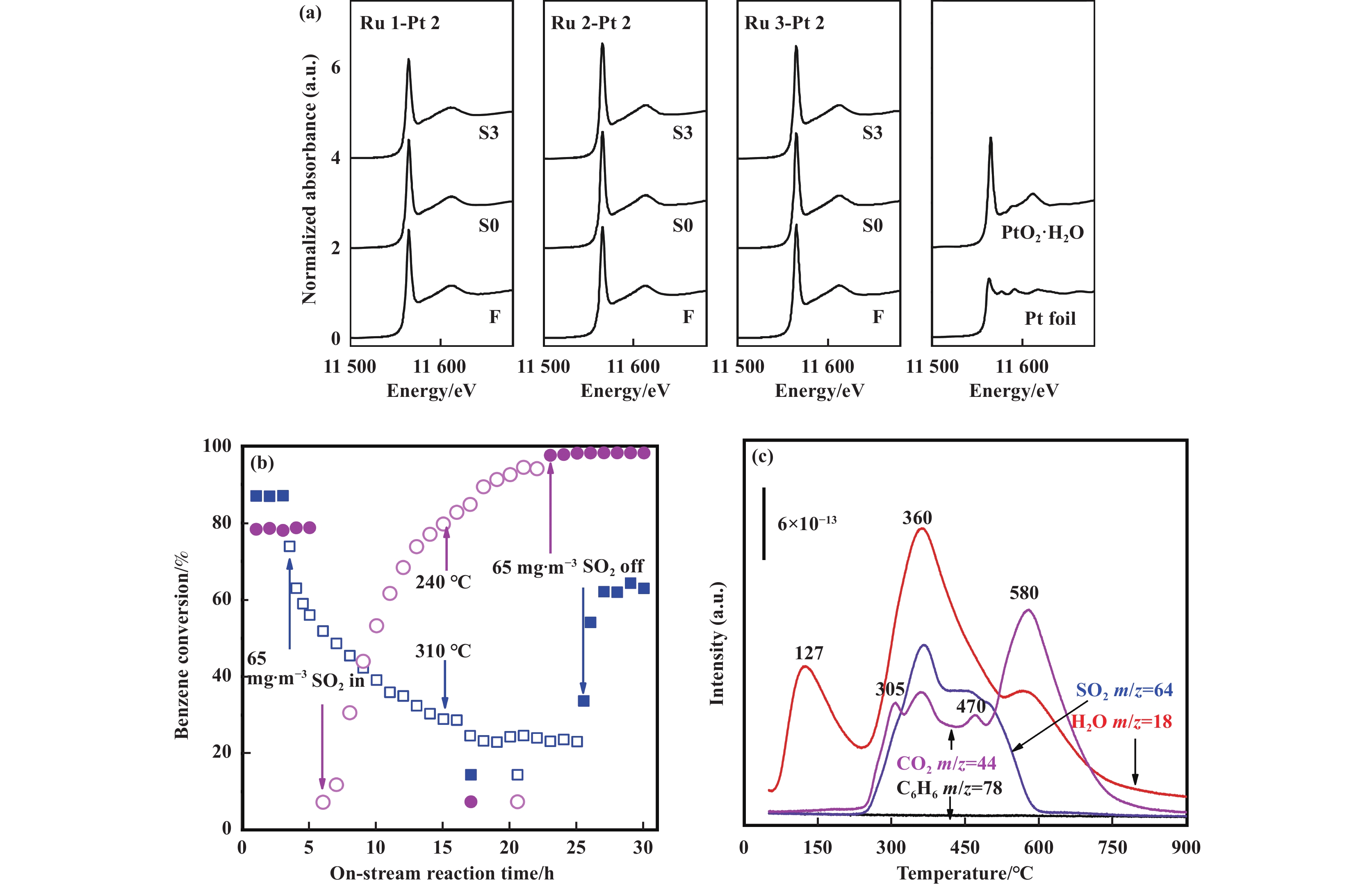
除了常见的Pt-Pd体系, 近些年来也有关于其他双贵金属或者贵金属与非贵金属组合的研究. 如Ohtsuka等[27]采用湿浸渍法构建了Ru-Pt/ZrO2双贵金属催化剂, 发现Ru的加入能显著抑制催化剂在SO2条件下的失活. 反应前后催化剂的Pt L3 XANES光谱证明(图2(a)), Ru的加入能有效地维持Pt的高氧化态且不会被SO2还原. 当Ru的添加量为2%(质量分数)或者更高时, 含SO2条件下反应前后催化剂的Pt氧化态变化很小, 表明负载的Pt物种始终处于高氧化状态从而表现出较高的氧化活性. Hou等[12]制备了双金属单原子Pd1Co1/Al2O3催化剂, 发现Pd-Co体系的构筑大幅提升了Pd/Al2O3催化剂的燃烧活性, T90由295降低到了250 ℃; 并且具有了逐步增强的抗SO2性能(图2(b)). Pd和CoO的双活性位点效应导致了苯氧化性能的增强, 活性位点较好的再生能力提升了催化剂的抗SO2中毒能力. 在SO2的存在下, Pd1Co1/Al2O3催化剂表面的PdO能转化为PdOS-O3配合物, 可以与Al2O3相互作用从而分解为PdO、活性氧和亚硫酸铝. 生成的活性氧和PdO活性位点之间可以继续反应, 有助于催化剂活性的逐渐恢复. Ben-TPD结果(图2(c))发现该样品上硫酸盐分解的同时能产生CO2和H2O, 这证明了苯在硫酸盐分解后可以与活性位点的活性氧再次发生反应. 这种由贵金属与非贵金属构建的双金属体系结合了单原子催化剂高度分散和利用率高的特点, 使得双活性位点效应得以实现. 高效的活性位点再生行为也为催化剂抗SO2中毒能力的提升提供了新的思路, 为双金属体系中添加的金属的选择和活性物种分散状态的利用提供了参考价值.
|
图 2 (a) Ru-Pt/ZrO2的Pt L3 XANES光谱[27]; (b)两种催化剂在苯氧化过程中的耐SO2性能测试; (c) SO2处理后Pd1Co1/Al2O3的Ben-TPD曲线 [12] Fig.2 (a) Pt L3 XANES spectra of Ru-Pt/ZrO2[27], (b) Test of SO2 resistance of two catalysts in benzene oxidation process, and (c) Ben-TPD profiles of the Pd1Co1/Al2O3 after SO2 treatment[12] |
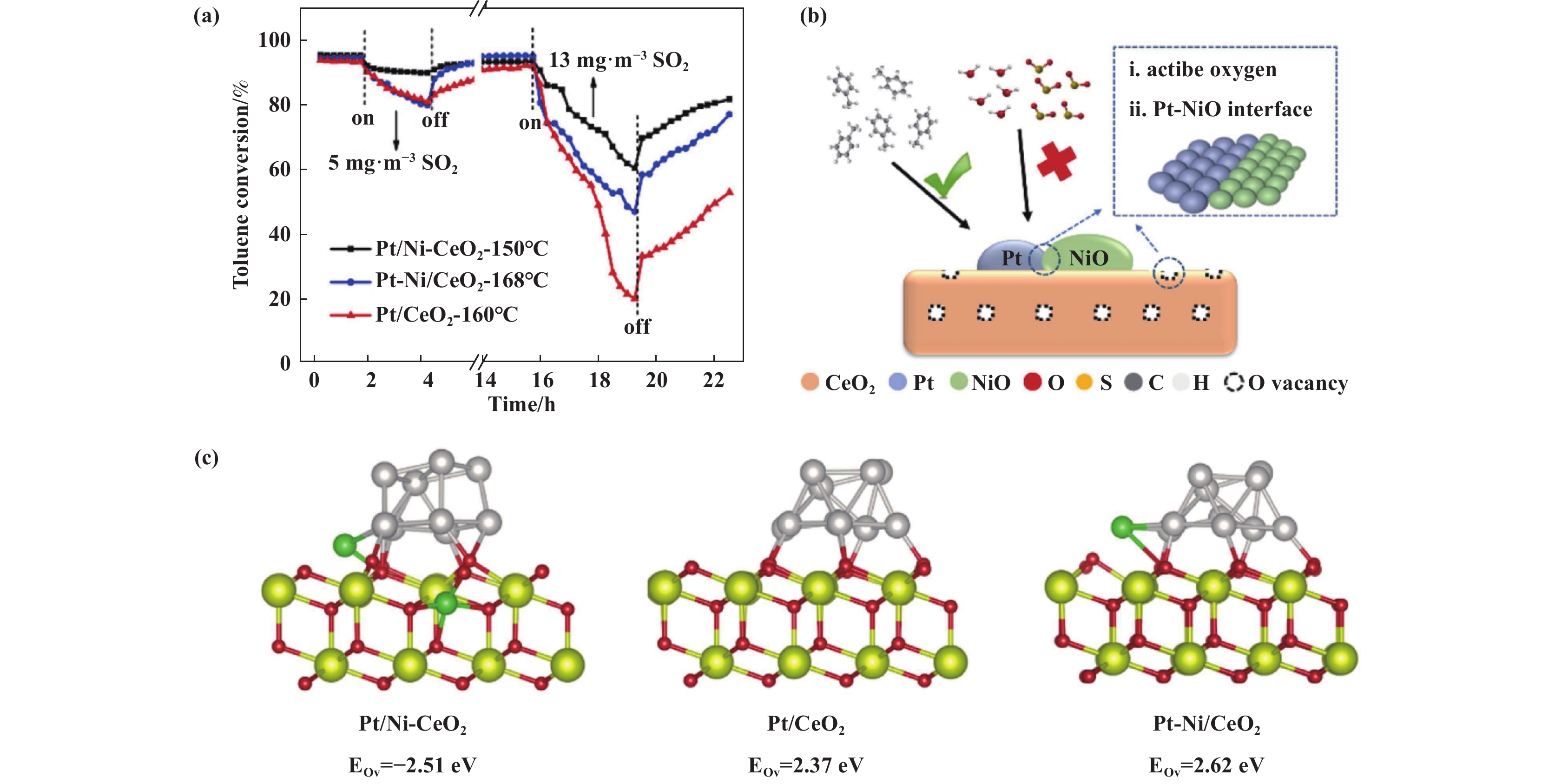
贵金属催化剂因其较为高昂的价格限制了它的大规模使用, 因此在减少贵金属含量的同时保证其活性和抗SO2性能, 成为了目前贵金属催化剂研发的一大热点. 通过掺杂金属氧化物助剂能对催化剂的酸性位点和界面结构等进行改性, 有助于改善低负载量的贵金属催化剂的性能, 还能有效抑制SO2的吸附以提高其抗中毒能力. Wang等[28]将Ce、V、W掺杂进了超低负载的0.05Pt/TiO2催化剂中, 得到了0.57CeO2-0.05Pt/TiO2、0.54V2O5-0.05Pt/TiO2和0.55WO3-0.05Pt/TiO2 3个样品, 并将它们应用于丙酮的催化燃烧. XPS结果证明3种助剂的掺杂增多了催化剂的表面吸附氧和Pt2+含量, 使得氧空位浓度增大, 有利于反应物分子的吸附和活化, 从而增强了氧化活性. 当反应气氛中引入SO2时, Ce、V或W的添加会增加原本催化剂表面酸性位点的数量, 能有效抑制酸性SO2的吸附. 同时CeO2极易与气态SO2结合形成Ce(SO4)2从而避免了SO2与Pt活性位点的结合. V物种的掺杂也会生成VOSO4来消耗SO2分子以减少其在Pt上的吸附; W的掺杂改性则能有效抑制SO2的氧化, 减缓硫酸盐的生成. Xiao等[29]以3种方式分别制备了Pt/Ni-CeO2(Ni掺杂)、Pt-Ni/CeO2(Ni表面修饰)和Pt/CeO2(浸渍法)催化剂, 将其用于甲苯的催化燃烧反应, 并考察了它们的抗SO2中毒效果. 如图3(a)所示, 采用Ni掺杂法构建的Pt/Ni-CeO2催化剂展现出了最优的抗SO2性能. 在Pt基催化剂中掺杂Ni后, Ni与Pt能通过热驱动形成Pt-NiO界面结构来对Pt的电子和化学性质进行修饰, 从而达到抑制SO2分子吸附的效果(图3(b)). 同时, 电子能损失谱、密度泛函理论计算(图3(c))等表征也证实了Pt/Ni-CeO2中掺杂的Ni物质会诱导催化剂从本体到表面产生丰富的氧空位, 从而在SO2的通入过程结束后, 也能保证有足够的活性氧在一定程度上帮助排出催化剂表面的硫物种, 使催化剂活性逐渐恢复. Ni物种的掺杂虽未以自身作为牺牲位点与SO2反应, 但仍通过与Pt活性物种形成界面结构从而对其电子和化学性质进行了改性, 促使Pt基催化剂达到了有效抗SO2中毒的目的.
|
图 3 (a)所制备的催化剂在甲苯氧化中的抗SO2性能; (b)Pt/Ni-CeO2催化剂抗中毒机理; (c)制备催化剂上氧空位形成能的DFT计算[29] Fig.3 (a) The SO2 resistance of the prepared catalyst in the oxidation of toluene; (b) Anti-poisoning mechanism of Pt/Ni-CeO2 catalyst; (c) DFT calculation of oxygen vacancy formation energy on as-prepared catalysts[29] |
负载型贵金属催化剂的载体一般为SiO2、Al2O3、TiO2等具有较大比表面积的材料. 良好的载体不仅有助于提高贵金属的分散度, 还可以增强活性组分与载体之间的相互作用, 有效提升催化剂的低温氧化性能. 但当催化剂在反应中受到SO2的攻击时, 载体与活性物种在一定情况下均能与SO2进行反应. 因此若要抑制酸性SO2分子在催化剂上的吸附, 提升载体的抗中毒能力也是必要的. Yang等[30]采取了在载体上引入金属氧化物的方式, 通过浸渍法用不同含量的SiO2对载体Al2O3进行改性, 制备了一系列Pt/SiO2-Al2O3催化剂. 含SO2条件下的丙烯催化氧化反应表明, 适量SiO2(18%, 体积分数)的引入有效提高了Pt/Al2O3的抗硫性能. 作者认为, Al2O3易与SO2反应生成硫酸铝, 而SiO2属于惰性的酸性材料不易硫酸化, 且N2吸附-脱附实验证明SiO2的引入没有改变Pt/Al2O3的织构性质. 研究发现该SiO2层均匀地沉积在了Al2O3载体上, 有效覆盖了其表面的SO2吸附位, 因而阻断了硫酸盐的沉积, 达到了抑制硫物种在Pt/Al2O3上生成与累积的效果. 该载体改性方法简单且抗SO2中毒能力显著, 适量SiO2的添加有效维持了催化剂原有的活性水平, 还展现出了最优的耐久性. Sun等[31]选择了直接合成耐SO2中毒载体以提升催化剂的抗中毒能力. 当反应气氛中存在SO2时, 甲苯转化率在V2O5-TiO2上仅略有变化, 并且0.46PdPt2.10/V2O5-TiO2催化剂的活性也几乎不受SO2的影响, 这充分展现了耐SO2的V2O5-TiO2载体的良好性能. XPS和(C7H8 + SO2)-TPD表征结果证明, 对于0.46PdPt2.10/ V2O5-TiO2样品, SO2主要吸附在载体的V物种上并生成硫酸盐从而有效保护了Pt活性位点不受SO2的毒害.
将载体进行硫酸化预处理以提高催化剂酸度也是一种非常有效的改性手段. Gu等[32]通过用不同质量百分比的硫酸水溶液进行湿浸渍对Ce-Zr载体进行了预处理, 制备了Pt/CZ和一系列Pt/CZ‐S催化剂. 丙烯的催化燃烧实验证明载体硫酸化预处理的措施极大提升了催化剂的抗SO2性能: 通入SO2反应长达20 h, Pt/CZ‐10S样品的丙烯转化率始终保持在95%不变. SO42−的加入显著增加了催化剂的总酸度且产生了新的Brönsted酸位, 有效抑制了SO2的吸附. 由此可见, 贵金属催化剂载体改性的手段巧妙且抗硫效果显著, 具有较好的应用潜力.
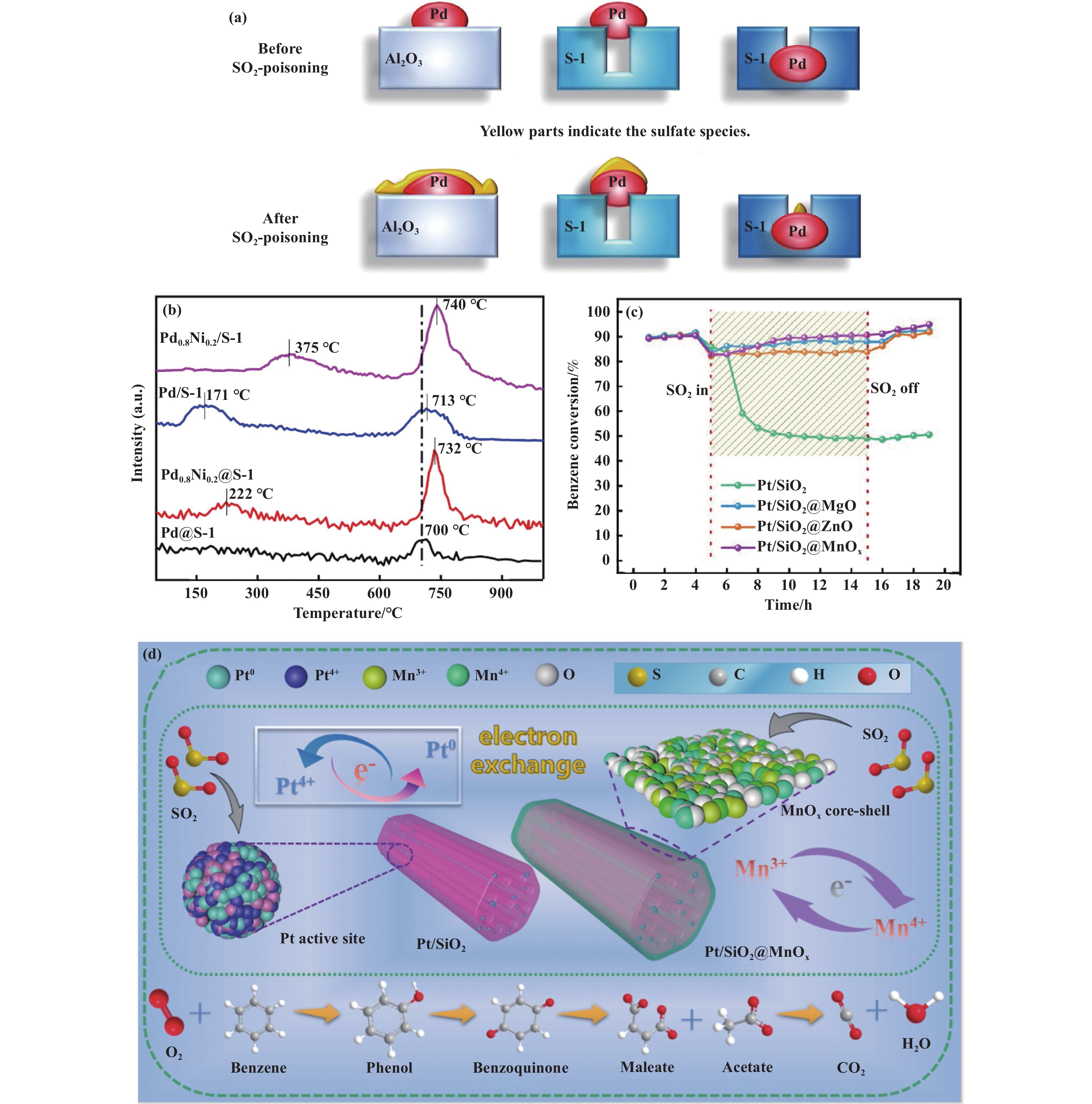
2.1.4 设计壳层保护结构目前对催化剂进行防止SO2吸附的保护设计较多的是通过构建核壳结构, 该形貌结构一般是由两种或两种以上材料组成, 使得内层被外层完全或部分包裹, 同时组成材料之间有明显边界. 当催化剂的活性物种置于核壳结构的内部时, SO2便会率先吸附到外部壳层上, 从而保护核内的活性物种不被SO2毒化. 并且核壳结构可在催化剂体系中产生协同效应[33−34], 有助于各类性能的提升, 如活性、抗SO2中毒能力等. Zhang等[35]将Pd纳米颗粒直接封装到沸石中, 得到了具有核壳结构的Pd@silicalite-1催化剂. 如图4(a)所示, 作者指出S-1壳层对SO2有屏蔽作用, 且壳层的微孔限制作用能阻止大尺寸PdSO4簇的形成, 导致SO2易在催化剂表面解吸从而降低了Pd@S-1催化剂的再生温度. 这是由于硫酸盐物种与SiO2的相互作用较弱, 所以硫物种不会在沸石的孔隙中积累, 使SO2的解吸相对容易. SO2-TPD(图4(b))结果表明Pd@S-1样品的PdSO4分解峰温度与峰面积远小于其他样品, 说明该催化剂对SO2的吸附量比其他样品都少且弱. 同时发现具有核壳结构的样品的峰都更窄, 解吸温度也更低, 意味着SO2更容易在壳层表面解吸, 这也证明了S-1壳层对SO2具有阻隔作用, 有助于提高催化剂的抗SO2性能. Yang等[36]通过一步水热法制备了具有有序介孔结构的Pt/SiO2催化剂, 并将其作为核包裹在了金属氧化物MOx (M = Mg, Zn, Mn)壳层里面. 外部的壳层能优先与SO2接触并反应, 从而避免了SO2对活性Pt位点的吸附毒化, 有效保护了核内物质(图4(d)). 如图4(c)所示, 在SO2的存在下, 3种核壳结构复合催化剂的苯转化率始终保持在80%以上, 相比于Pt/SiO2催化剂, 它们的抗SO2中毒效果十分显著. 特别是MnOx壳层不仅可以吸附SO2, 还能通过介孔孔道与活性Pt物种接触, 使Mnδ+与Ptδ+之间产生快速的电荷传递, 有助于Pt0活性物种的生成, 因此其抗硫性能最好. 这种保护结构的设计在物理抵御SO2对活性位点的吸附上具有非常显著的优势, 性能良好的壳层不仅有助于表面吸附硫酸盐物种的解吸, 还能促进氧化反应的进行, 是一种简单且高效的贵金属催化剂抗SO2中毒的措施. 综上, 一些代表性的贵金属催化剂采取的抗SO2中毒策略及效果如表1所示.
|
图 4 (a), (b)Pd/Al2O3、Pd/S-1和Pd@S-1上的硫化模式示意图、催化剂的SO2-TPD[35]; (c),(d) 所制备催化剂在苯氧化中的抗SO2性能和Pt/SiO2@MnOx的抗硫机理图[36] Fig.4 (a), (b) Schematic diagram of the sulfidation patterns on Pd/Al2O3, Pd/S-1 and Pd@S-1, SO2-TPD of catalysts[35]; (c), (d) SO2 resistance of the prepared catalysts in benzene oxidation and sulfur resistance mechanism diagram of Pt/SiO2@MnOx[36] |
| 表 1 代表性贵金属催化剂的抗SO2策略及效果 Table 1 Anti-SO2 strategies and effects of representative noble metal catalysts |
非贵金属储量大且较为经济, 多为过渡金属, 通常含有不饱和的d轨道, 容易吸附反应物分子并活化[5], 如Mn、Co、Fe、Cr等. 它们一般价态多变, 易形成多种氧化物, 可由调节形貌、暴露晶面等方式来调控催化剂的性能, 也可通过预处理在催化剂表面产生缺陷位点进而增强其对VOCs的吸附活化能力[37−38]. 但是当一些非贵金属如Cu、Mn等作为活性位点时, 则易与SO2反应生成硫酸盐或亚硫酸盐物种, 从而导致催化剂的中毒失活.
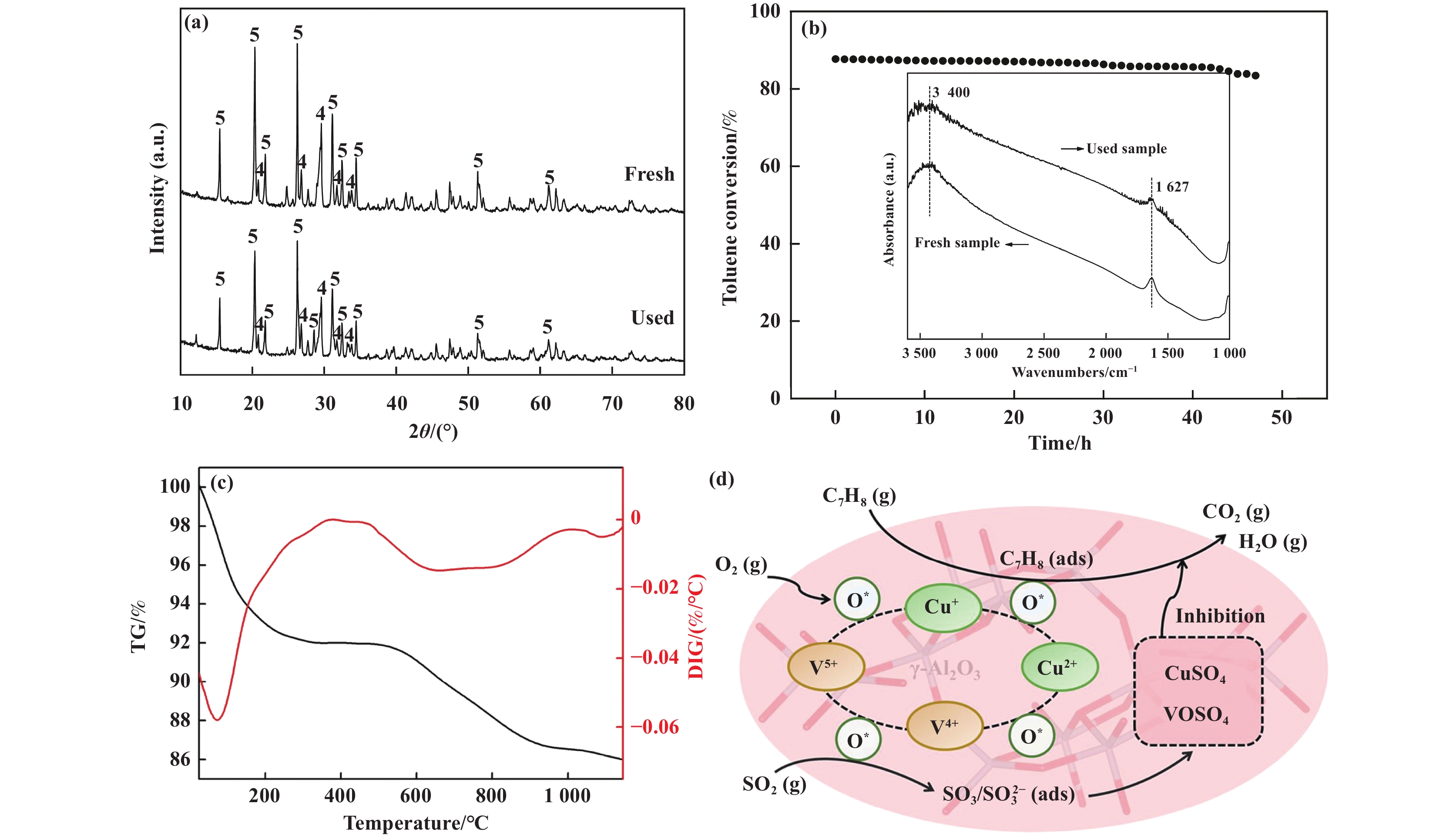
2.2.1 多组分金属元素掺杂助剂掺杂: 提升非贵金属催化剂的抗SO2中毒能力, 一般都是通过掺杂具有较好SO2耐受性的助剂来抑制SO2的侵蚀, 达到保护活性物种的目的. 一些研究表明, 掺杂V不仅能有效抑制SO2的吸附[39], 还能在一定程度上保护其他活性金属不被硫酸盐化, 这是由于V对SO2有较高的亲和力[40−41]. 例如, Zhang等[42]将耐SO2性能良好的V物种与氧化活性优异的Cu物种结合起来, 采用溶胶-凝胶法制备了一系列Cu-V混合氧化物催化剂用于含SO2气氛下的甲苯催化氧化反应, 找到了抗SO2中毒能力最好的Cu1V6样品. 作者认为, 这是由于该催化剂拥有最大的比表面积和良好的还原性, 以及形成了能抑制硫酸盐物质生成的CuV2O6相, 才使其在长期暴露于SO2气氛中时仍然表现出了良好的抗性. 图5(a), (b)中XRD和FT-IR表征结果证明, Cu1V6催化剂在通SO2反应后依然保留了原来的物相组成, 没有形成硫酸盐, 抗SO2中毒效果显著. 尽管该研究中不同掺杂比例的催化剂抗硫能力有差异, 但相比于原始的CuOx样品, 助剂的掺杂对催化剂耐硫性的提升始终有着一定效果. 另外, 助剂的添加不仅能抑制SO2的侵蚀, 还能与活性金属产生相互作用, 促进其分散. Lyu等[43]研究发现V的掺杂有效提高了13Cu/γ-Al2O3在甲苯氧化过程中的抗SO2中毒能力, 并找到了性能最好的10Cu-3V/γ-Al2O3催化剂. V的加入不仅使得CuO具有了更好的分散性和均匀的元素分布, 有利于产生更多的活性中心, 而且构成了V5+ + Cu+↔V4+ + Cu2+的氧化还原循环, 能引起更多的表面化学氧, 有助于活性的提升. 如图5(c)所示, TG表征结果证明了硫化后10Cu-3V/γ-Al2O3表面的硫酸盐主要以VOSO4和CuSO4的形式存在, SO2会优先与V反应. 同时图5(d)的机理图也清楚表示了与SO2更亲和的V物种的添加延缓了催化剂上硫酸盐的生成, 显著提高了13Cu/γ-Al2O3的抗SO2性能.
|
图 5 (a)新鲜和使用过的Cu1V6样品的XRD谱图; (b)Cu1V6样品的耐久性测试和新鲜与使用过的样品的傅里叶变换红外光谱图[42]; (c) S-10Cu-3V/γ-Al2O3的TG和DTG谱; (d)SO2对10Cu-3V/γ-Al2O3的抑制机理[43] Fig.5 (a) XRD patterns of fresh and used Cu1V6 samples; (b) Durability testing of Cu1V6 samples and FT-IR spectra of fresh and used samples[42]; (c) TG and DTG profiles of S-10Cu-3V/γ-Al2O3; (d) The inhibition mechanism of SO2 over 10Cu-3V/γ-Al2O3[43]. |
A位或B位金属阳离子的引入: 钙钛矿催化剂作为一类重要的VOCs催化燃烧非贵金属催化剂, 其催化性能主要由AB位点的阳离子性质和价态决定, 它们可以被相同或不同价态的阳离子部分取代. 目前对钙钛矿催化剂抗SO2中毒的研究主要集中在A/B位阳离子的引入上, 酸度的增加和钙钛矿晶格稳定性的提升均有助于减少SO2对其结构的破坏. Shi等[44]通过在A或/和B位点引入Sr/Mn制备了一系列钙钛矿型催化剂, 并通过苯的催化燃烧反应发现AB位共掺杂的La0.9Sr0.1Co0.9Mn0.1O3具有最好的活性和抗SO2性能. Sr和Mn的掺杂提高了Co3+和Oads的浓度, 也促进了活性Co物质的分散. B位掺杂Mn和A/B位共掺杂Sr/Mn这两种途径均可以改善催化剂的酸度, 并且SO2-TPD等表征证实了Sr和Mn的掺杂有助于催化剂表面吸附硫物种的解吸, 有效提高了LaCoO3钙钛矿催化剂的抗SO2性能. Lv等[16]采用溶胶-凝胶法制备了在同等条件下不同B位金属掺杂的LaCo1−xMxO3 (M = Fe, Cr, Cu)钙钛矿型催化剂, 其中LaCo0.6Fe0.4O3在甲苯氧化中展现出了最优的抗SO2中毒能力. 钙钛矿B位金属阳离子掺杂能通过改变还原性、氧空位含量、B位氧化态等提升催化剂活性和减弱SO2中毒的影响. 该研究中Fe掺杂剂的效果要优于Cr和Cu. 这是由于Fe的加入提高了钙钛矿的结晶度, 使其保持了原有的稳定性因而未被破坏. 且Fe掺杂剂能稳定高度分散的Co颗粒, 尽可能保持Co离子的还原性, 对催化活性和抗SO2性能有较大的促进作用. 原位漂移光谱的半定量分析和XPS等表征证明了Fe的掺杂更有利于抑制硫酸盐的沉积. 钙钛矿晶格的高稳定性和Fe离子掺杂导致的对SO2的不敏感, 使得该催化剂在中毒过程中形成的硫酸盐最少, 并且原有的钙钛矿结构保持完好, 因而获得了良好的抗SO2性能.
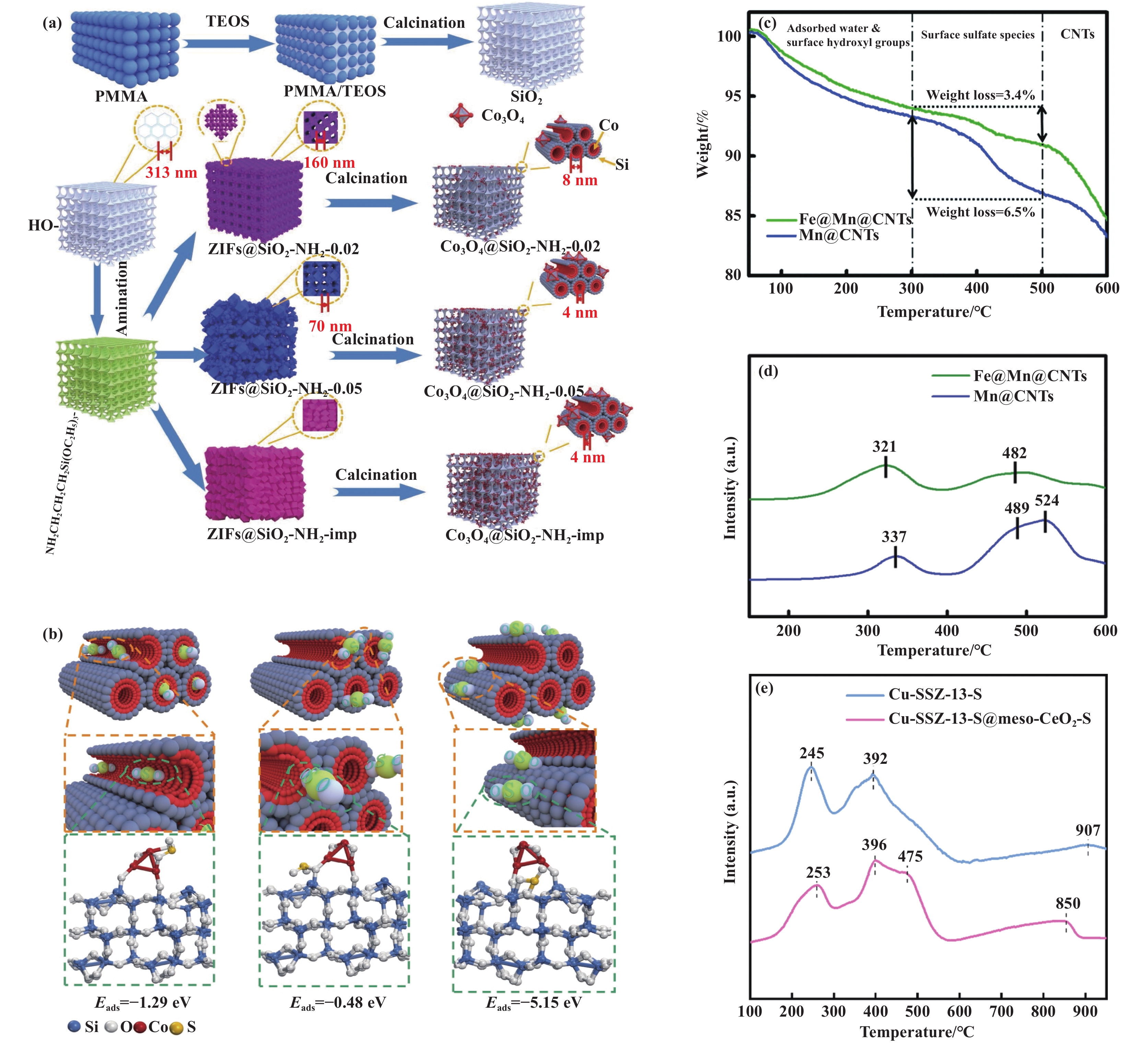
2.2.2 构建核壳结构通过构建保护壳层来减弱SO2对活性物种的吸附毒化, 对于非贵金属催化剂依然是适用的. 例如, Han等[45]以三维有序大孔-介孔(3DOM)SiO2作为纳米反应器, 通过原位生长的方式将Co3O4纳米粒子限域封装到了孔道中, 制备了一系列不同孔径的Co3O4@SiO2-NH2催化剂用于苯的催化燃烧(图6(a)). 实验结果表明, 与纯的Co3O4相比, Co3O4@SiO2-NH2-imp催化剂具有更好的抗SO2中毒性能. 作者通过如图6(b)所示的理论计算证明, SO2会率先吸附在SiO2上, 而不易吸附在Co—O—Si键上. 因此SiO2纳米反应器起到了保护壳的作用, 保护内部的活性位点免受SO2的侵蚀. Cai等[46]通过化学浴沉积和电置换反应合成了具有多壳层的Fe2O3@ MnOx@CNTs催化剂. 作者指出, 硫酸锰的积累是Mn@CNTs失活的主要原因, 当其外部包裹Fe2O3壳层后可以提升催化剂表面的碱性从而抑制硫酸盐物质的形成, 这是Fe2O3@MnOx@CNTs催化剂具有高SO2抗性的一个重要因素. 如图6(c),(d)所示, TGA测试证明了Fe@Mn@CNT催化剂表面形成的硫酸盐的数量远少于Mn@CNTs, (SO2+O2)-TPD结果也显示Fe@Mn@CNT催化剂在高温范围内对SO2的吸附量明显低于Mn@CNT催化剂. 具有抗硫酸酸化能力的Fe2O3壳层有效保护了Mn活性物种, 提高了催化剂的抗SO2中毒能力. Xu等[47]采用自组装技术合成了具有核壳结构的Cu-SSZ-13@ meso-CeO2催化剂, H2-TPR结果(图6(e))表明CeO2壳层与SO2反应生成了硫酸铈, 以保护活性Cu物种不受SO2的攻击, 从而达到了提升催化剂抗SO2性能的目的. 以牺牲壳层物质使其与SO2反应生成硫酸盐物种的保护手段, 对提高催化剂抗SO2中毒能力是非常有用的. 此类方法不仅具有物理抵御SO2的效果, 还能够与核内物质产生协同效应, 有助于催化剂各类性能的提升, 这也为催化剂的形貌设计提供了一定的参考价值. 上述论述中一些代表性的非贵金属催化剂采取的抗SO2中毒策略及效果如表2所示.
|
图 6 (a)催化剂合成示意图; (b)SO2在Co—O—Co, Co—O—Si和Si—O—Si键上的吸附能[45]; (c)耐SO2试验后催化剂的TGA曲线; (d)催化剂(SO2+O2)-TPD谱图[46]; (e)硫化样品H2-TPR结果[47] Fig.6 (a) Schematic diagram of the synthesis of catalysts; (b)The Eads of SO2 on Co—O—Co, Co—O—Si and Si—O—Si bond[45]; (c) TGA curves of the catalysts after the SO2 tolerance test; (d)SO2 +O2-TPD profiles of the catalysts[46]; (e) H2-TPR results of sulfided samples[47] |
| 表 2 代表性非贵金属催化剂的抗SO2策略及效果 Table 2 Anti-SO2 strategies and effects of representative non-noble metal catalysts |
通过分析催化剂的活性物种和载体性质, 采取合理的掺杂、预处理等改性手段, 对催化剂进行结构保护、增加酸性位点、稳固催化剂结构和增强SO2在催化剂上的解吸等, VOCs催化燃烧催化剂的抗SO2性能得到了很好的改进. 这些抗中毒的措施从不同方面有效抑制了SO2在催化剂表面的吸附, 阻止了其与活性物种或载体发生反应形成硫酸盐等物质. 然而, 尽管前人已经做了相当丰富的研究, 但随着工业化的发展, 目前应用在VOCs催化燃烧领域的抗SO2中毒催化剂仍有着一定的局限性.
3.1 尽管已经有不少工作进行了催化剂在SO2存在条件下的耐久性测试, 但实验室模拟的反应过程中SO2的通入浓度还是相对较低, 且测试时间较短. 若考虑到催化剂在实际工业生产中的应用场景, 应尽量保证催化剂在上百小时及以上的长寿命稳定性, 并且应逐步增大SO2的浓度进行性能测试, 确保催化剂在高浓度SO2和长时间的高温反应中依然具有良好的稳定性和抗中毒能力.
3.2 实际VOCs废气往往会含有多种污染物. 如当苯、甲苯、氯苯、烷烃等污染物共存时, 同一种催化剂对其的氧化活性应相差不大, 且在含SO2的工况下, 应保证催化剂始终具有良好的抗中毒能力. 甚至要考虑到废气中不仅含有VOCs, 还有CO、NOx等不同种类的污染物, 此时催化剂能否同样拥有对VOCs良好的降解能力和耐SO2性能.
3.3 在呼吁高效且经济化降解VOCs废气的大环境下, 制备出方法简单、材料用量少且具有优异催化性能的催化剂是研究的首要目标. 目前关于抗SO2中毒催化剂研究的大部分工作, 虽取得了不错的效果, 但催化剂制备过程仍然繁冗复杂, 并不适合实际的工业应用. 因此, 必须要对催化剂的制备方法进行改进, 使其既具有优异的活性和抗SO2中毒能力, 又能实现制备过程简便且材料用量少, 这样才能使抗SO2中毒催化剂的应用前景不断扩大, 更好地满足大规模的工业应用.
| [1] |
Promoting effect of acid sites in hierarchical porous Pt/ZSM-5 catalysts for low-temperature removal of VOCs[J]. Appl Surf Sci, 2022, 606: 154888.
DOI:10.1016/j.apsusc.2022.154888 |
| [2] |
Simple thermocatalytic oxidation degradation of VOCs[J]. Catal Lett, 2021, 152(6): 1801–1818.
DOI:10.1007/s10562-021-03770-x |
| [3] |
Studies on the activity and deactivation of novel optimized TiO2 nano- particles for the abatement of VOCs[J]. Chem Eng J, 2011, 175: 330–340.
DOI:10.1016/j.cej.2011.09.115 |
| [4] |
Investigation into the enhanced catalytic oxidation of o-Xylene over MOF-derived Co3O4 with different shapes: The role of surface twofold-coordinate lattice oxygen (O2f)[J]. ACS Catal, 2021, 11(11): 6614–6625.
DOI:10.1021/acscatal.1c01116 |
| [5] | |
| [6] | |
| [7] | |
| [8] |
On the mechanism of sulfur poisoning of platinum catalysts[J]. J Catal, 1972, 27(3): 453–456.
DOI:10.1016/0021-9517(72)90183-2 |
| [9] |
Study on anti-sulfur dioxide poisoning of palladium-based catalyst for toluene catalytic combustion[J]. Int J Hydrog Energy, 2021, 46(9): 6329–6340.
DOI:10.1016/j.ijhydene.2020.11.126 |
| [10] | |
| [11] | |
| [12] |
Highly efficient and enhanced sulfur resistance supported bimetallic single-atom palladium-cobalt catalysts for benzene oxida-tion[J]. Appl Catal B: Environ, 2021, 285: 119844.
DOI:10.1016/j.apcatb.2020.119844 |
| [13] |
Three-dimensionally ordered mesoporous Co3O4-supported Au-Pd alloy nanoparticles: High-performance catalysts for methane combustion[J]. J Catal, 2015, 332: 13–24.
DOI:10.1016/j.jcat.2015.09.008 |
| [14] |
Confined ultrathin Pd‐Ce nanowires with outstanding moisture and SO2 tolerance in methane combustion[J]. Angew Chem Int Ed, 2018, 57(29): 8953–8957.
DOI:10.1002/anie.201803393 |
| [15] |
Catalytic oxidation of volatile organic compounds by non-noble metal catalyst: Current advancement and future prospec-tives[J]. J Clean Prod, 2022, 363: 132523.
DOI:10.1016/j.jclepro.2022.132523 |
| [16] |
Dopant-driven tuning of toluene oxidation and sulfur resistance at the B-site of LaCo1-xMxO3 (M = Fe, Cr, Cu) perovskites[J]. Catal Sci Technol, 2022, 12(11): 3670–3684.
DOI:10.1039/D2CY00476C |
| [17] |
Surface restructuring of supported nano-ceria for improving sulfur resistance[J]. ACS Catal, 2021, 11(12): 7154–7159.
DOI:10.1021/acscatal.1c02209 |
| [18] |
Microwave-assisted rapid synthesis of CeO2 nanoparticles and its desulfurization processes for CH3SH catalytic decomposi-tion[J]. Chem Eng J, 2016, 289: 161–169.
DOI:10.1016/j.cej.2015.12.103 |
| [19] |
Deactivation and regeneration method for Ni catalysts by H2S poisoning in CO2 methanation reaction[J]. Catalysts, 2021, 11(11): 1292.
DOI:10.3390/catal11111292 |
| [20] |
H2S poisoning of NiAl2O4/Al2O3-YSZ catalyst during methane dry reforming[J]. Can J Chem Eng, 2016, 94(4): 650–654.
DOI:10.1002/cjce.22438 |
| [21] |
Regulation of the reaction pathway to design the high sulfur/coke-tolerant Ce-based catalysts for decomposing sulfur-containing VOCs[J]. Chem Eng J, 2022, 429: 132473.
DOI:10.1016/j.cej.2021.132473 |
| [22] |
Kinetics, operando FTIR, and controlled atmosphere EXAFS study of the effect of sulfur on Pt-supported catalysts during CO oxidation[J]. J Catal, 2005, 233: 372–387.
DOI:10.1016/j.jcat.2005.04.016 |
| [23] |
A study of Pt-Pd/γ-Al2O3 catalysts for methane oxidation resistant to deactivation by sulfur poisoning[J]. J Mol Catal A: Chem, 2010, 315(1): 35–42.
DOI:10.1016/j.molcata.2009.08.023 |
| [24] | |
| [25] |
Deceleration of SO2 poisoning on PtPd/Al2O3 catalyst during complete methane oxidation[J]. Appl Catal B: Environ, 2018, 236: 384–395.
DOI:10.1016/j.apcatb.2018.05.018 |
| [26] |
Pt modulates the electronic structure of Pd toimprove the performance of Pd-based catalytic combustion catalyst[J]. Int J Hydrog Energy, 2021, 46(35): 18391–18400.
DOI:10.1016/j.ijhydene.2021.03.028 |
| [27] |
Effects of Ru or Rh addition on the activity and sulfur tolerance of Pt/ZrO2 for the oxidation of methane at low temperatures[J]. Catal Lett, 2013, 143(10): 1043–1050.
DOI:10.1007/s10562-013-1056-9 |
| [28] |
Supported ultralow loading Pt catalysts with high H2O-, CO2-, and SO2-resistance for acetone removal[J]. Appl Catal A: Gen, 2019, 579: 106–115.
DOI:10.1016/j.apcata.2019.04.018 |
| [29] |
Ni-doping-induced oxygen vacancy in Pt-CeO2 catalyst for toluene oxidation: Enhanced catalytic activity, water-resistance, and SO2-tolerance[J]. Appl Catal B: Environ, 2023, 323: 122173.
DOI:10.1016/j.apcatb.2022.122173 |
| [30] | |
| [31] |
PdPty/V2O5-TiO2: Highly active catalysts with good moisture- and sulfur dioxide-resistant performance in toluene oxidation[J]. Catalysts, 2022, 12(11): 1302.
DOI:10.3390/catal12111302 |
| [32] |
Propene and CO oxidation on Pt/Ce-Zr-SO42− diesel oxidation catalysts: Effect of sulfate on activity and stability[J]. Chinese J Catal, 2017, 38(3): 607–616.
DOI:10.1016/S1872-2067(17)62781-5 |
| [33] |
Core/shell nanoparticles: Classes, properties, synthesis mechanisms, characterization, and applications[J]. Chem Rev, 2011, 112(4): 2373–2433.
DOI:10.1021/cr100449n |
| [34] |
Core-shell structured catalysts for thermocatalytic, photocatalytic, and electrocatalytic conversion of CO2[J]. Chem Soc Rev, 2020, 49(10): 2937–3004.
DOI:10.1039/C9CS00713J |
| [35] |
Anti-sintering Pd@silicalite-1 for methane combustion: Effects of the moisture and SO2[J]. Appl Surf Sci, 2019, 494: 1044–1054.
DOI:10.1016/j.apsusc.2019.07.252 |
| [36] |
Significant enhanced SO2 resistance of Pt/SiO2 catalysts by building the ultrathin metal oxide shell for benzene catalytic combus-tion[J]. ACS Appl Mater Interfaces, 2023, 15(36): 42541–42556.
DOI:10.1021/acsami.3c07515 |
| [37] | |
| [38] | |
| [39] |
V2O5-modified Mn-Ce/AC catalyst with high SO2 tolerance for low-temperature NH3-SCR of NO[J]. Chem Eng J, 2019, 370: 810–821.
DOI:10.1016/j.cej.2019.03.225 |
| [40] |
Synergistic effect and mechanism of FeOx and CeOx co-doping on the superior catalytic performance and SO2 tolerance of Mn-Fe-Ce/ACN catalyst in low-temperature NH3-SCR of NO[J]. J Environ Chem Eng, 2021, 9(6): 106360.
DOI:10.1016/j.jece.2021.106360 |
| [41] |
SO2 poisoning mechanism of the multi-active center catalyst for chlorobenzene and NOx synergistic degradation at dry and humid environments[J]. Environ Sci Technol, 2021, 55(19): 13186–13197.
DOI:10.1021/acs.est.1c03617 |
| [42] |
A mechanistic study of the sulfur tolerance of Cu-V mixed oxides in toluene catalytic combustion[J]. Reac Kinet Mech Catal, 2015, 116(2): 467–478.
DOI:10.1007/s11144-015-0912-6 |
| [43] |
Highly efficient removal of toluene over Cu-V oxides modified γ-Al2O3 in the presence of SO2[J]. J Hazard Mater, 2022, 436: 129041.
DOI:10.1016/j.jhazmat.2022.129041 |
| [44] |
Design Sr, Mn-doped 3DOM LaCoO3 perovskite catalysts with excellent SO2 resistance for benzene catalytic combustion[J]. Chem Eng J, 2023, 473: 145476.
DOI:10.1016/j.cej.2023.145476 |
| [45] |
A confined growth strategy to construct 3DOM SiO2 nanoreactor in-situ embedded CO3O4 nanoparticles catalyst for the catalytic combustion of VOCs: Superior H2O and SO2 resistance[J]. Nano Res, 2024, 17(1): 207–220.
DOI:10.1007/s12274-023-5498-0 |
| [46] |
Design of multi-shell Fe2O3@MnOx@CNTs for the selective catalytic reduction of NO with NH3: Improvement of catalytic activity and SO2 tolerance[J]. Nanoscale, 2016, 8(6): 3588–3598.
DOI:10.1039/C5NR08701E |
| [47] |
Excellent NH3-SCR activity and significant sulfur resistance over novel core-shell Cu-SSZ-13@meso-CeO2 catalyst[J]. Fuel, 2023, 353: 129292.
DOI:10.1016/j.fuel.2023.129292 |
 2024, Vol. 38
2024, Vol. 38


