2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
乙烯是一种重要的化工原料[1], 是合成纤维、合成橡胶、合成塑料(聚乙烯及聚氯乙烯)、合成乙醇的基本化工原料, 也用于制造氯乙烯、苯乙烯、环氧乙烷、醋酸、乙醛和炸药等. 目前, 蒸汽裂解仍是全球乙烯供应的重要来源, 然而该过程能耗高, 导致释放大量CO2. 乙烷氧化脱氢制乙烯(ODHE)为放热反应, 反应条件温和, 能耗低, 发展前景可观. 然而该过程易发生副反应(深度氧化等), 因此如何在保持较高的乙烷转化率条件下提高乙烯选择性是关键挑战[2].
镍基金属氧化物催化剂因其在低温条件下表现出较高的C—H键断裂活性、低成本等优势, 被认为是性能最优异的ODHE催化剂之一[3−11]. 研究结果表明, O−物种是乙烷深度氧化的活性位点, 因此如何调控催化剂中Ni周围环境及活性氧物种成为设计高效Ni基催化剂的关键[11−12]. 关于镍基金属氧化物催化剂的研究主要集中在通过调控金属组分含量[3−4]、制备方法[5,10]、助剂添加[6−7]以及使用载体[8−9]对催化剂的氧化还原性质、氧物种、电子效应以及酸碱性等方面产生影响, 进而影响催化剂的反应性能. Ni-M/Al2O3 体系催化剂可以通过在载体中掺杂Si改变载体酸碱性或者改变焙烧温度对Ni的化学环境进行调控, 产生更多NiAl2O4 物种, 进而调控催化性能[13−14].
已有文献表明, 水蒸汽处理会对催化剂表面的活性位点及其周围的化学环境产生影响进而影响催化性能. 水蒸汽处理可以改变Co-CeO2催化剂表面的氧空位和氧物种的含量[15], 水解离形成的羟基在CeNiO催化剂表面的覆盖度不同会影响催化剂表面对反应物和产物的吸脱附[16], 水诱导也可以抑制Ni/h-BN催化剂上活性位点的烧结[17], 且水处理会影响γ-Al2O3载体与活性组分的相互作用[18]. 因此, 本文采用湿浸渍法制备Ni-Ga/γ-Al2O3催化剂, 通过调控水蒸汽处理温度来改变催化剂的物理化学性质, 进而探究水蒸汽处理温度对Ni-Ga/γ-Al2O3催化剂ODHE性能的影响.
1 实验部分 1.1 实验原料商业球形γ-Al2O3(中国日用化学工业研究院, 700 ℃煅烧2 h, 研磨至粉末后用作载体), Ni(NO3)2·6H2O(>98%, 国药集团化学试剂有限公司), Ga(NO3)3·xH2O(99.99%, 上海阿拉丁生化科技股份有限公司).
1.2 催化剂制备催化剂采用湿浸渍结合水蒸汽处理法制备. 常温下1.5 g Ni(NO3)2·6H2O和0.263 g Ga(NO3)3·xH2O溶于20 mL水中, 加入2.5 g γ-Al2O3 , 在红外灯照射下边搅拌边浸渍干燥成粉末. 然后将该粉末置于120 ℃烘箱中干燥24 h, 继而置于马弗炉中升温至550 ℃焙烧4 h获得催化剂, 记为NiGaAl. 其中NiO的负载量为12.5%, Ni/Ga的摩尔比为5.0. 将NiGaAl催化剂在不同温度(150、250、350、450及550 ℃)下通入水蒸汽处理1 h后, 继而干燥3 h, 获得不同温度水蒸汽处理的催化剂, 命名为NiGaAl-T (T代表水蒸汽处理温度(℃)).
1.3 催化剂表征室温下使用Cu Kα射线(λ=
催化剂的氧化还原性质在配备热导检测器(TCD)和质谱仪(MS)的ChemBET Pulsar TPR/TPD上测试. 首先是H2-程序升温还原反应(H2-TPR). 样品(0.05 g)在300 ℃的He流(35 mL∙min−1) 中预处理1 h, 去除物理吸附的杂质, 温度降至室温后将气体切换为10% H2/Ar流(35 mL∙min−1), 以20 ℃∙min−1 的升温速率从室温升至
催化性能评价在固定床石英反应器(内径 12 mm)中进行. 常压条件下, 催化剂(0.50 g, 粒径0.250~0.425 mm)通N2 升温至450 ℃后, 首先通入6% C2H6 + 94% N2, 5 min后通入6% O2 + 94% N2. 反应气体积比为6% C2H6 + 6% O2 + 88% N2(总流量为62.5 mL∙min−1), 接触时间(W/F)为0.48 g∙s∙cm−3. 反应稳定1 h后, 每隔2 h取样, 使用配备Al2O3色谱柱(分析CH4、C2H6和C2H4等)和TDX-01色谱柱(分析CH4和COx)的在线气相色谱仪(SHIMADZU GC-2014C)分析反应产物.
2 结果与讨论 2.1 催化剂组成与结构表征首先采用ICP测定催化剂的化学组成, 如表1所示. NiGaAl催化剂中NiO相对含量为12.7%, Ni/Ga摩尔比为7.6. 不同温度水蒸汽处理后的催化剂中NiO相对含量和Ni/Ga摩尔比基本保持不变, 表明水蒸汽处理温度对催化剂的组成影响不大.
| 表 1 催化剂的组成、织构信息及TEM表征数据 Table 1 Composition, N2 adsorption-desorption and TEM characterization data of different catalysts |
为了研究催化剂的织构信息, 对催化剂进行N2吸附-脱附测试, 如表1所示. NiGaAl催化剂的比表面积、孔体积和孔径分别为135 m2∙g−1、0.71 cm3·g−1和17.3 nm. 不同温度水蒸汽处理后的催化剂的比表面积和孔体积有所减小, 但孔径基本不变.
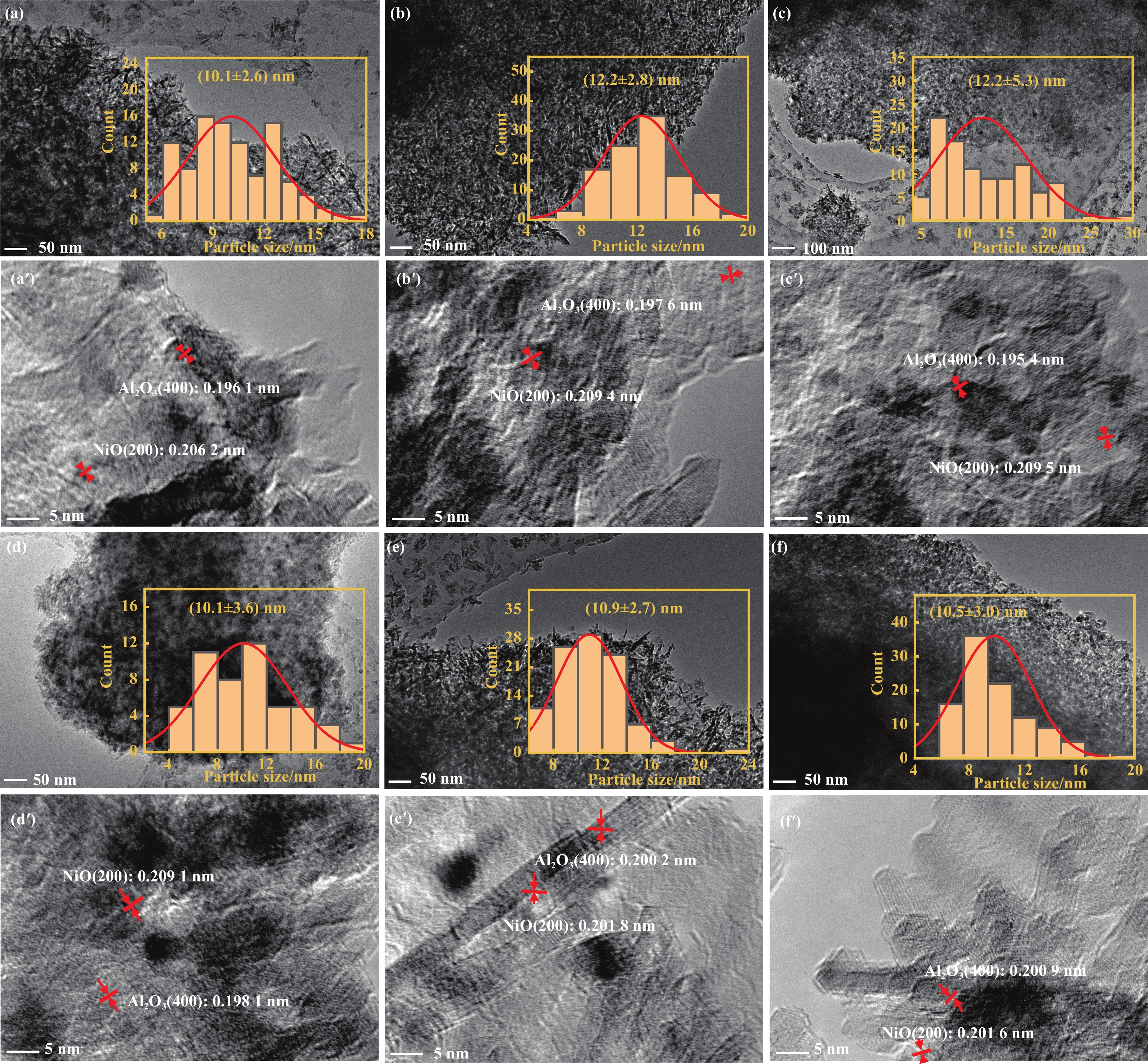
图1为催化剂的TEM图像. NiGaAl催化剂的NiO颗粒尺寸约为10.1 nm. 不同温度水蒸汽处理后的催化剂Ni颗粒粒径变化不大. 进一步对不同催化剂的NiO(200)晶面和Al2O3(400)晶面的晶面间距进行计算, 如图1(b)和表1所示. 水蒸汽处理温度≥450 ℃时, NiO(200)的晶面间距明显减小, Al2O3(400)的晶面间距明显增加. 其中, Al3+的离子半径为
|
图 1 反应前不同催化剂的TEM图 Fig.1 TEM of fresh catalysts (a−f) particle size and (a′−f′) crystal spacing for NiO(200) and Al2O3(400) of fresh catalysts: (a, a′) NiGaAl, (b, b′) NiGaAl-150, (c, c′) NiGaAl-250, (d, d′) NiGaAl-350, (e, e′) NiGaAl-450, and (f, f′) NiGaAl-550 |
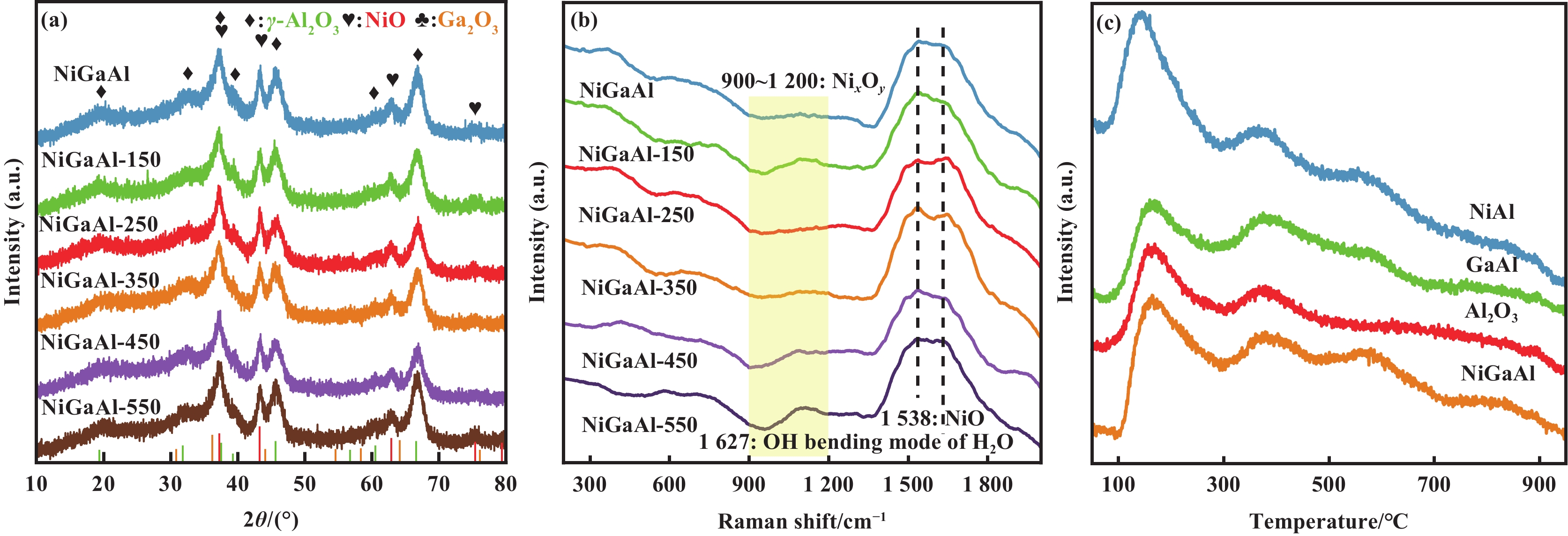
图2为催化剂的XRD和Raman谱图. XRD谱图中所有催化剂的物相结构基本相同, 包括γ-Al2O3 (JCPDS No: 50-0741)和NiO (JCPDS No: 47-1049), 表明水蒸汽处理温度对催化剂的物相结构无显著影响. 在Raman谱图中, 900~
|
图 2 不同催化剂的(a) XRD, (b) Raman 谱图与(c) O2-TPD-MS中O信号变化 (m/z=16) Fig.2 (a) XRD pattern, (b) Raman spectra, and (c) the variation of O signal (m/z=16) in O2-TPD-MS of different catalysts |
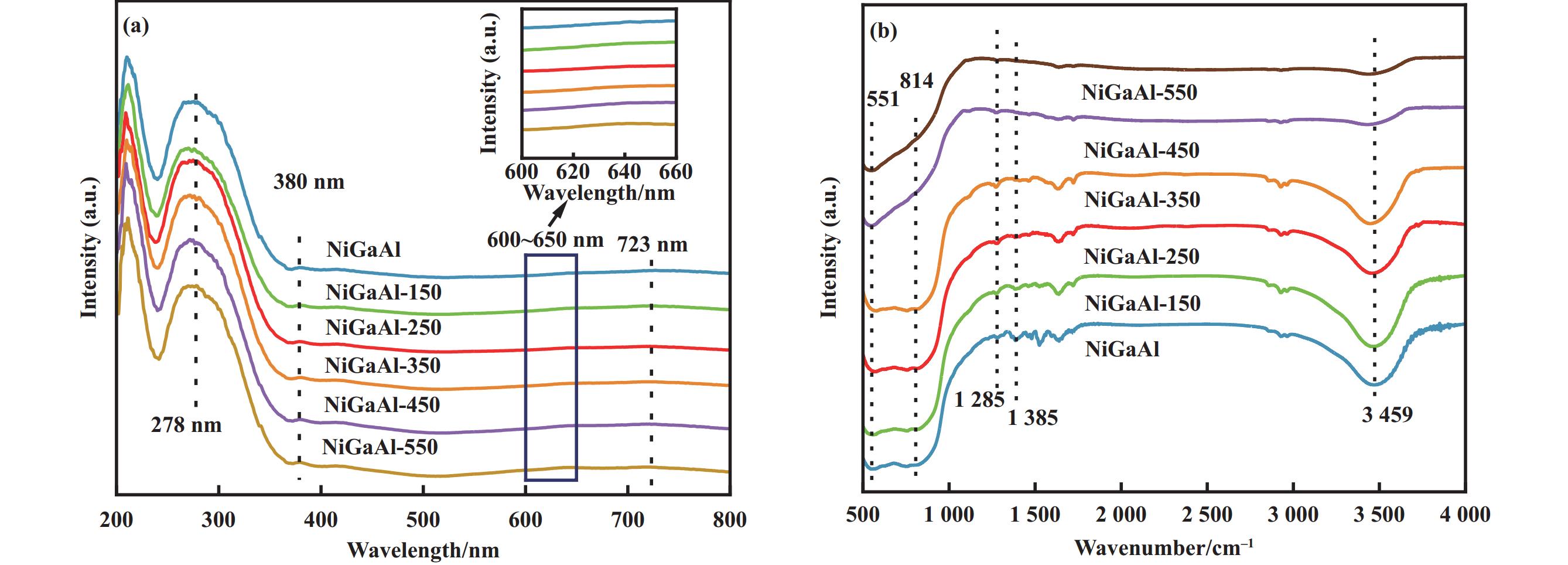
UV-Vis谱图和FTIR谱图为结构的分析进一步提供了有利信息, 如图3所示. 278 nm 处的特征峰归属于 Ni2+-O2− 之间的电荷转移[23], 380 nm和723 nm处的特征峰归属于八面体配位的NiO中Ni2+的3A2g→3T1g的d-d转移[24]. 600~650 nm范围内的信号与四面体对称的 Ni2+的存在有关[25]. 水蒸汽处理温度≥450 ℃时, 600~650 nm处的峰强度明显增强, 表明高温水蒸汽处理可以促进四面体对称的Ni2+生成, 这可能归属于NiAl2O4 尖晶石结构[25]. FTIR谱图显示, 551 cm−1 和 814 cm−1处的特征峰归属于 AlO6 八面体结构和 AlO4 四面体结构中 Al—O 键的晶格振动[26],
|
图 3 不同催化剂的(a) UV-Vis与(b) FTIR 谱图 Fig.3 (a) UV-Vis and (b) FTIR spectra of different catalysts |
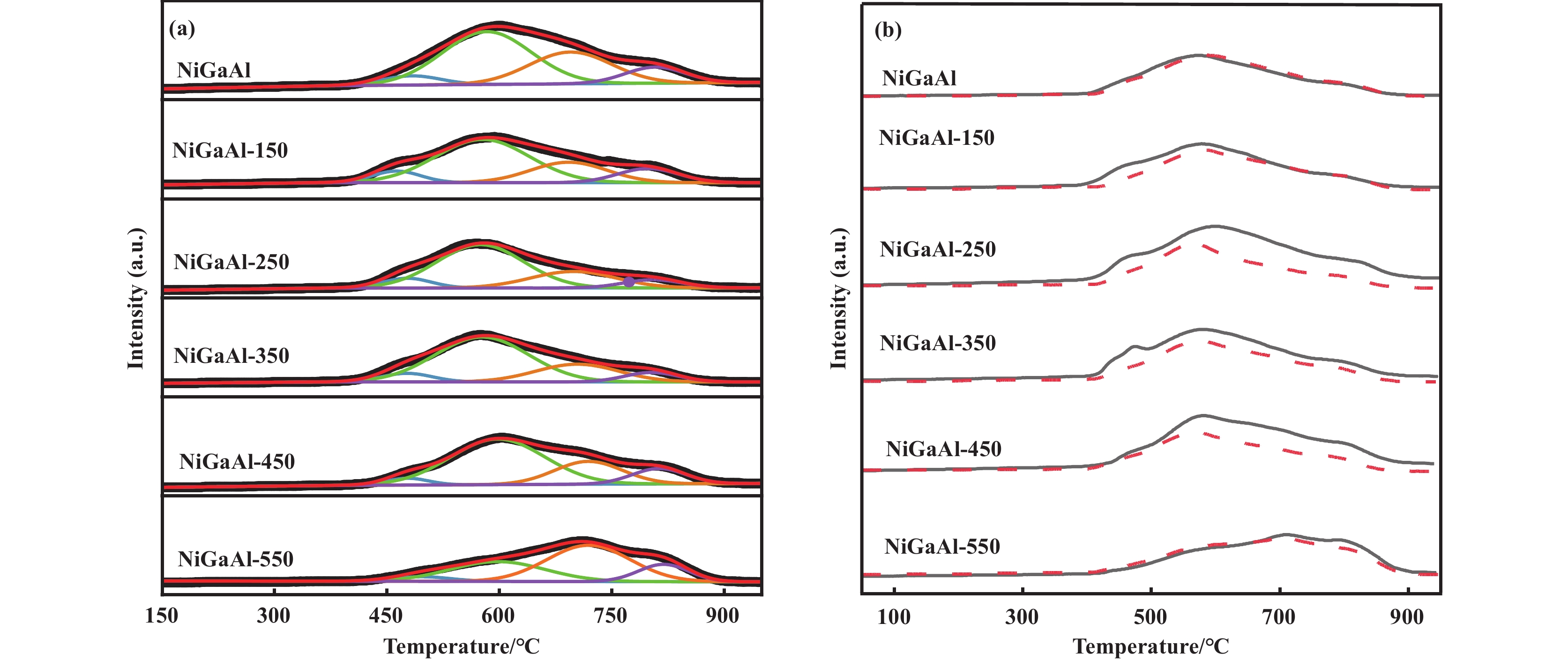
在氧化脱氢反应中, 催化剂的氧化还原性质对其催化性能有较大影响. 图4为催化剂的H2-TPR图. 对于NiGaAl催化剂, 483 ℃处的出峰(TF1)归属于与γ-Al2O3载体几乎无相互作用的NiO物种(游离NiO)还原, 583 ℃处的出峰(TF2)归属于与γ-Al2O3载体有较强相互作用的NiO物种还原, 694 ℃处的出峰(TF3)归属于Ni2+进入到Al2O3晶格当中形成的NiAl2-xO4物种的还原, 807 ℃处的出峰(TF4)归属于NiAl2O4物种的还原[30]. 对NiGaAl催化剂进行不同温度水蒸汽处理后, 不同Ni物种的出峰温度和峰面积发生变化. 如表2所示, NiGaAl-150催化剂中4种Ni物种的出峰温度均向低温方向位移, 特别是游离NiO的出峰温度降低了20 ℃, 表明150 ℃水蒸汽处理有利于NiO的还原. 除此之外, 游离NiO的氢消耗量以及在所有Ni物种中的占比增加, 表明150 ℃水蒸汽处理催化剂有利于游离NiO的生成. 一般认为与载体没有相互作用的NiO物种中的氧为O−, 与乙烷的非选择氧化有关, 该Ni物种的生成可以提高乙烷的转化率, 降低乙烯的选择性[12], NiGaAl-150催化剂的H2-TPR结果与其催化性能的结果一致. 当水蒸汽处理温度进一步升高, 游离NiO的出峰温度升高, 250~550 ℃水蒸汽处理后具有金属-载体强相互作用的NiO、NiAl2–xO4和NiAl2O4三种物种的出峰温度升高, 且三种Ni物种在所有Ni物种中的占比增加, 表明水蒸汽处理温度升高有利于增强金属-载体强相互作用.
|
图 4 不同催化剂的H2-TPR (a) 反应前与(b)反应前后对比: 灰实线-反应前, 红虚线-反应后 Fig.4 The H2-TPR of (a) fresh catalysts, and (b) the comparison of fresh and used catalysts: grey solid line-fresh catalysts, red dotted line-used catalysts |
| 表 2 反应前催化剂H2-TPR中不同镍物种的出峰位置TF及氢消耗量n Table 2 Peak positions TF and H2 consumption n of different nickel species in H2-TPR for fresh catalysts |
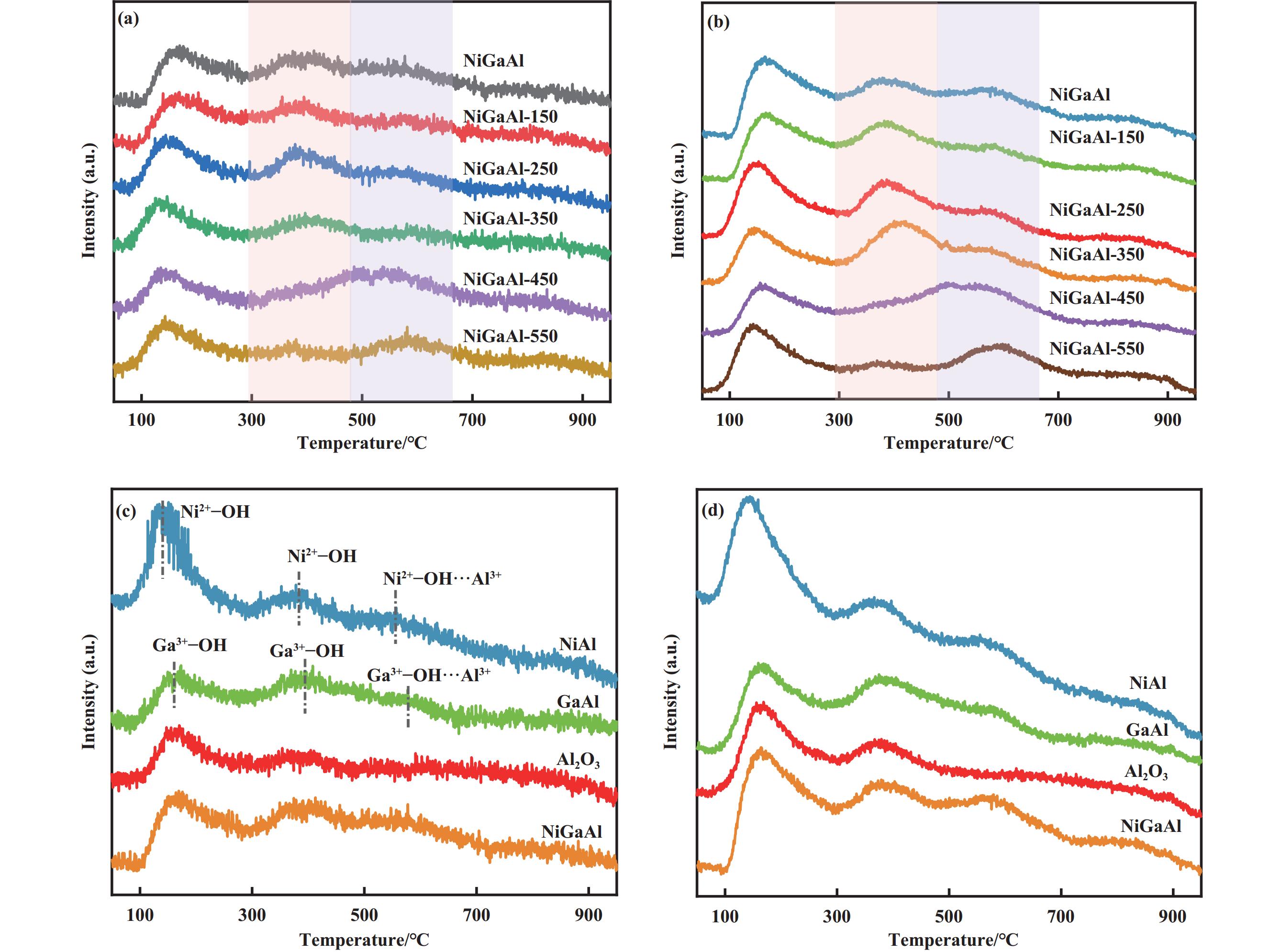
在O2-TPD测试过程中, MS中检测到OH信号和H2O信号发生变化. 如图5(a)和(b)所示, NiGaAl催化剂的OH信号和H2O信号主要分为三个峰, 分别为<300 ℃、300~500 ℃以及>500 ℃. 当水蒸汽处理温度≤350 ℃时, OH信号和H2O信号的出峰形状基本相似, 当水蒸汽处理温度升高至450 ℃和550 ℃后, >500 ℃处的峰强度明显增强, 表明高温水蒸汽处理催化剂会影响催化剂表面OH和H2O物种及其含量. 进一步探究催化剂表面不同的OH物种, 采用相同的湿浸渍法制备了只含Ni组分的负载型NiAl催化剂和只含Ga组分的负载型GaAl催化剂, 对NiAl和GaAl的催化剂进行O2-TPD测试, 如图5(c)所示,相比于Al2O3, NiAl和GaAl催化剂在300~500 ℃以及>500 ℃存在更明显的OH出峰, 表明300~500 ℃的出峰可以归属为化学吸附的Ni2+−OH或者Ga3+−OH, >500 ℃可以归属为化学吸附的且与载体有较强相互作用的Ni2+−OH∙∙∙Al3+或者Ga3+−OH∙∙∙Al3+. 除此之外, 对于NiAl催化剂, <300 ℃的出峰明显增强, 表明催化剂表面存在物理吸附的Ni2+−OH. 同时, H2O信号的峰变化与OH信号的变化相似, 结合不同温度水蒸汽处理后的NiGaAl催化剂的OH出峰变化情况, 高温水蒸汽处理(≥450 ℃)更容易形成与载体具有更强相互作用的Ni2+−OH∙∙∙Al3+或者Ga3+−OH∙∙∙Al3+.
|
图 5 不同催化剂的O2-TPD-MS信号 (a, c) OH信号 (m/z=17)与(b, d) H2O信号 (m/z=18) Fig.5 The signals of O2-TPD-MS for different catalysts (a, c) OH signal (m/z=17), (b, d) H2O signal (m/z=18) |
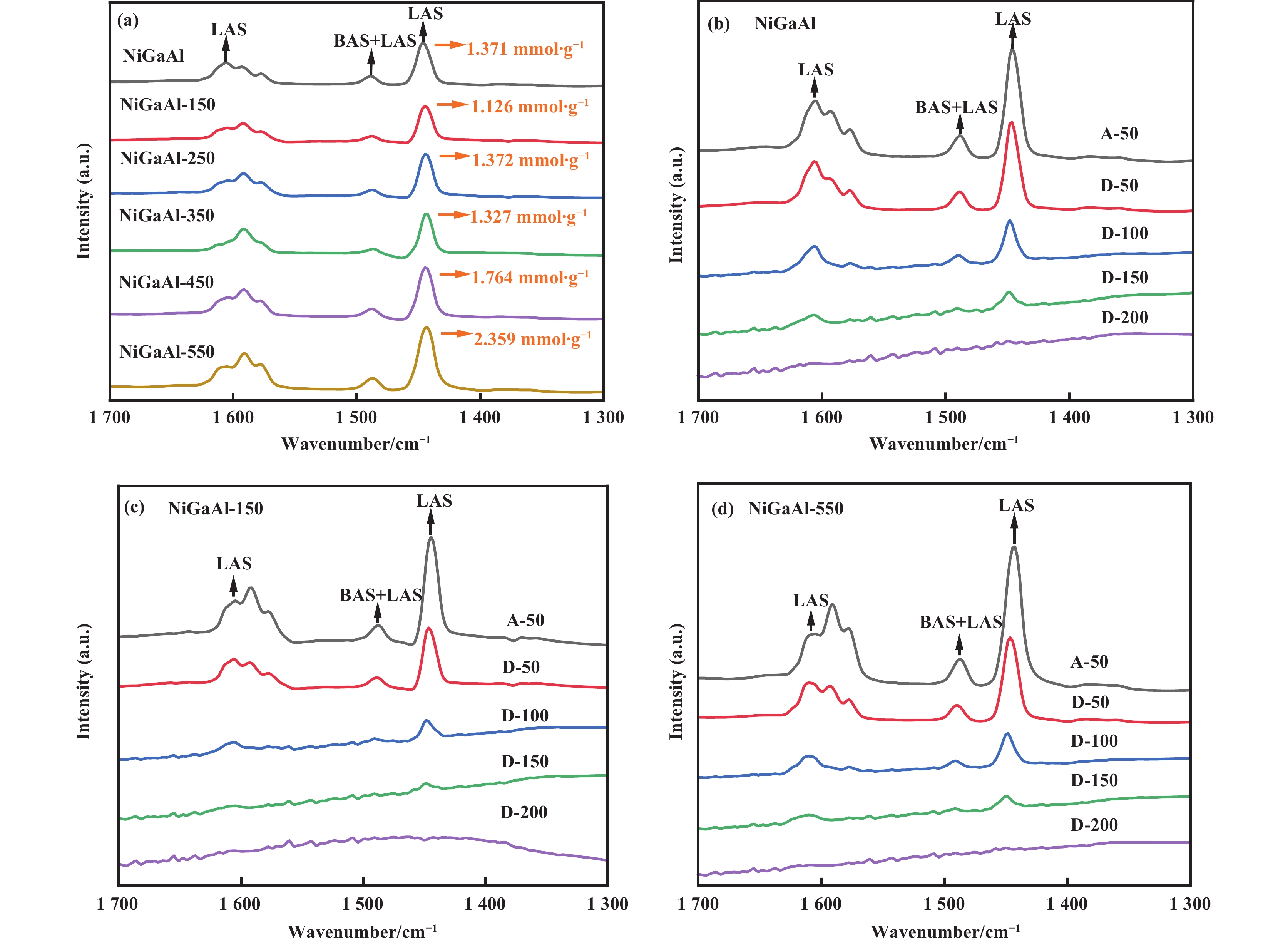
采用Py-IR观察催化剂表面酸性变化, 如图6所示. 不同催化剂的Py-IR出峰位置相似.
|
图 6 不同催化剂的Py-IR吸脱附谱图: (a) 不同催化剂吡啶吸附谱图及LAS酸浓度; (b) NiGaAl, (c) NiGaAl-150和(d) NiGaAl-550 催化剂的吡啶脱附温度, 其中A-T对应吡啶吸附温度, D-T对应吡啶脱附温度 Fig.6 Py-IR adsorption and desorption spectra of different catalysts: (a) Pyridine adsorption spectra and LAS concentration for different catalysts, pyridine desorption temperatures of (b) NiGaAl, (c) NiGaAl-150, and (d) NiGaAl-550, A-T corresponded to the temperature of pyridine adsorption and D-T corresponded to the temperature of pyridine desorption |
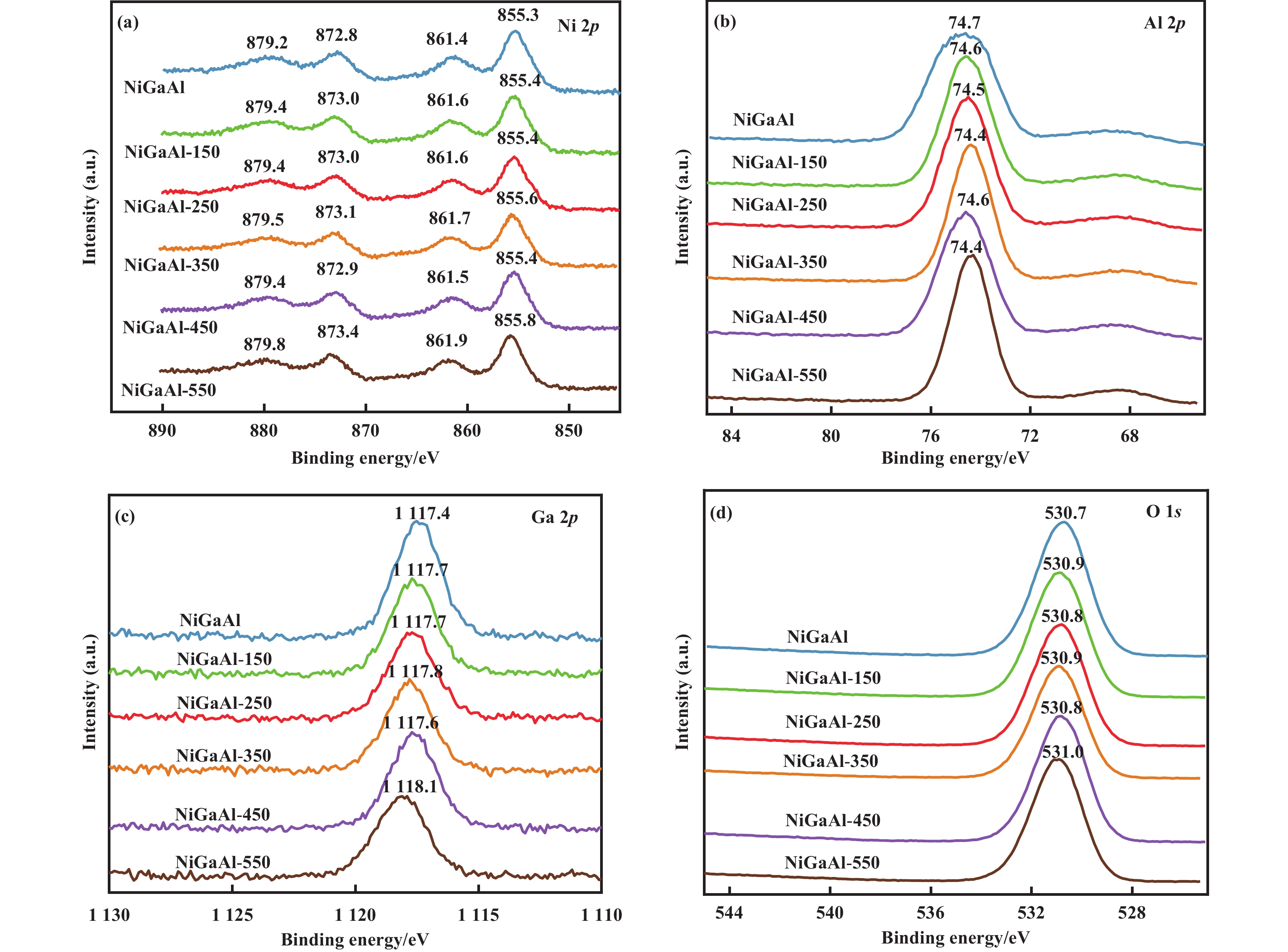
图7为不同催化剂的Ni 2p、Al 2p、Ga 2p以及O 1s谱图的出峰结合能变化, NiGaAl的XPS谱图Ni 2p、Al 2p、Ga 2p以及O 1s分别在855.3、74.7、
|
图 7 不同催化剂的XPS谱图 (a) Ni 2p, (b) Al 2p, (c) Ga 2p与(d) O 1s Fig.7 The XPS spectra for (a) Ni 2p, (b) Al 2p, (c) Ga 2p and (d) O 1s of different catalysts |
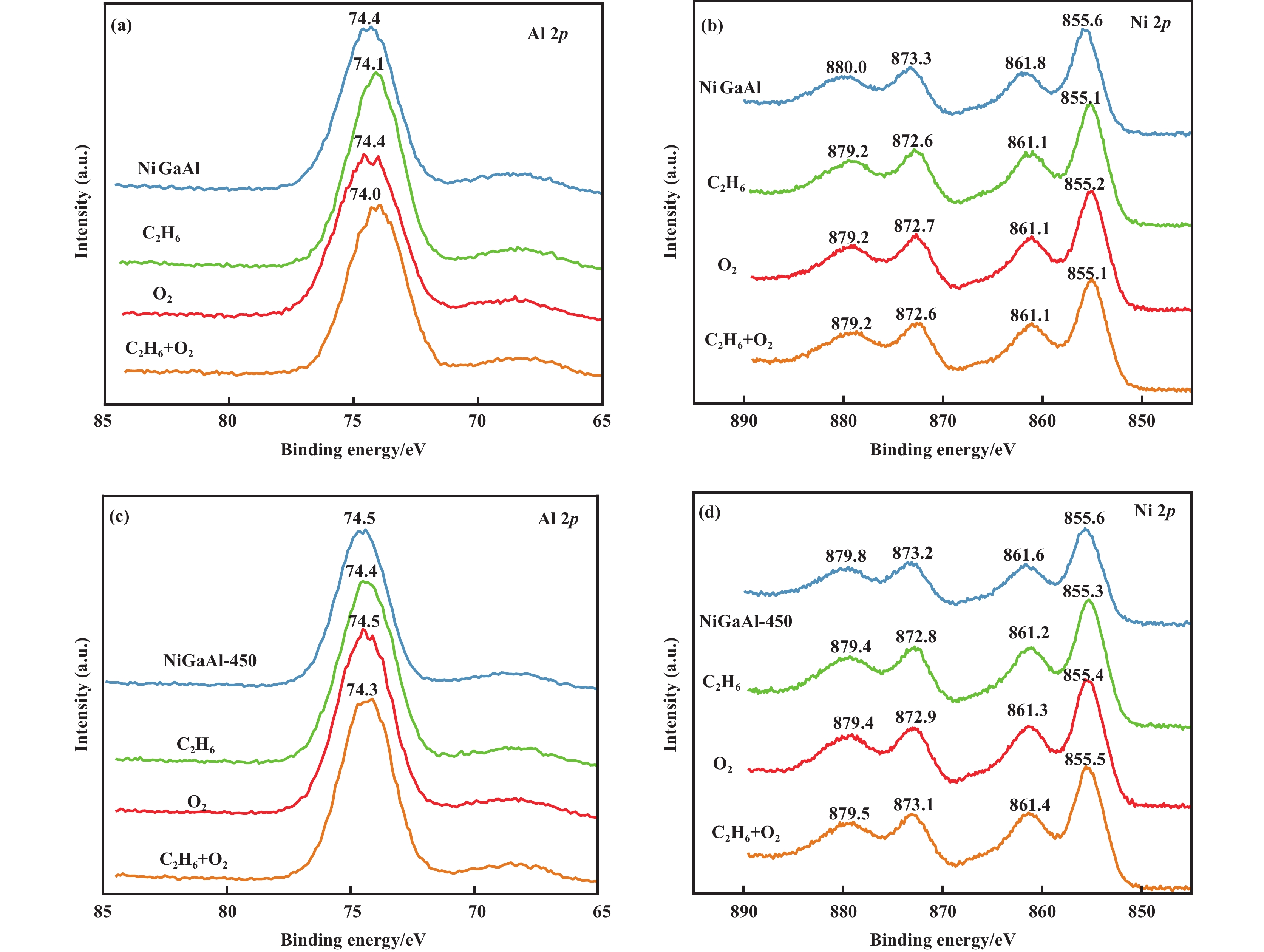
为进一步探究催化剂中不同物种在反应气中的变化, 对NiGaAl催化剂和NiGaAl-450催化剂进行quasi in-situ XPS测试. 如图8(a)和8(b)所示, 对于NiGaAl催化剂, 通入6% C2H6 + 94% N2后, Ni 2p和Al 2p均向低结合能方向位移, 最后通入6% C2H6 + 6% O2 + 88% N2后, Ni 2p和Al 2p均向低结合能方向位移, 表明在反应气氛围下存在电子转移. 对于NiGaAl-450催化剂, 如图8(c)和(d)所示, 在反应气氛围下也存在电子转移. 在不同的反应气氛围下, 两种催化剂的位移方向一致, 但通入反应气体后的位移程度存在差异, NiGaAl-450催化剂的Ni 2p和Al 2p的结合能位移程度小于NiGaAl催化剂的Ni 2p和Al 2p的结合能位移程度, 表明高温水蒸汽处理有利于活性组分和载体的稳定.
|
图 8 准原位XPS谱图 (a) NiGaAl: Al 2p, (b) NiGaAl: Ni 2p, (c) NiGaAl-450: Al 2p与(d) NiGaAl-450: Ni 2p Fig.8 The quasi in-situ XPS spectra (a) NiGaAl: Al 2p, (b) NiGaAl: Ni 2p, (c) NiGaAl-450: Al 2p, and (d) NiGaAl-450: Ni 2p |
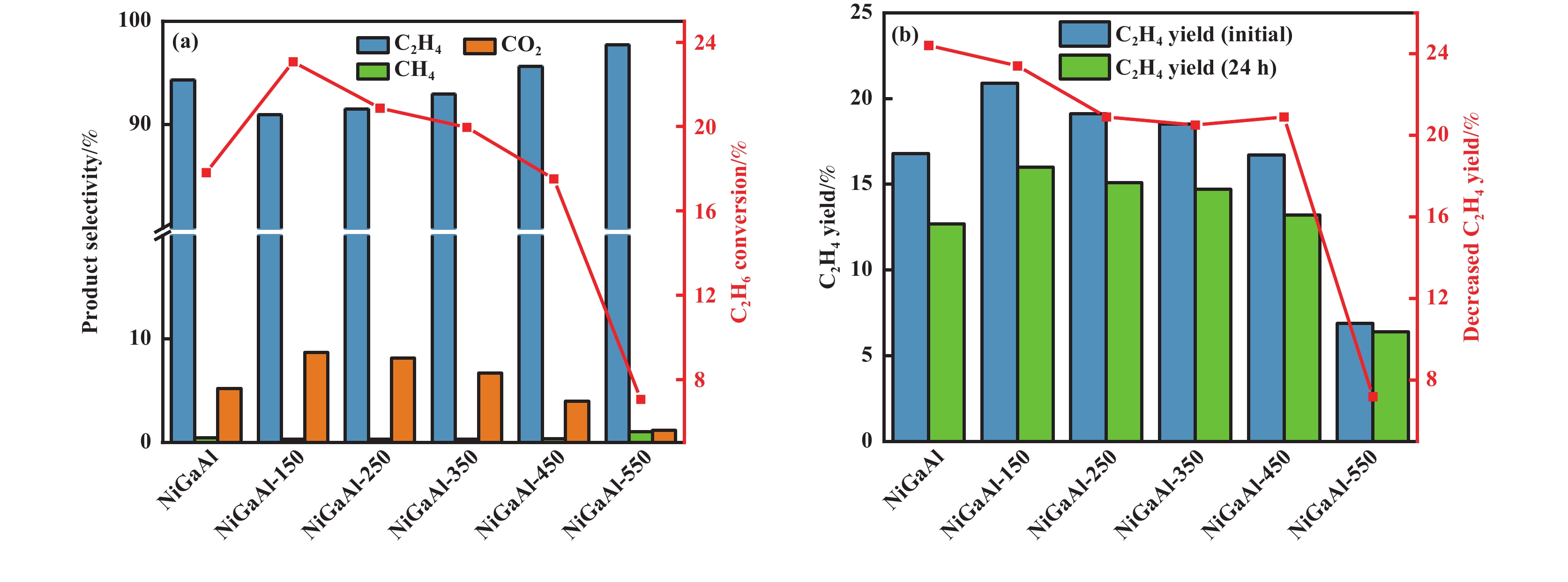
图9为催化剂ODHE反应评价结果. NiGaAl催化剂乙烷转化率为17.8%, 乙烯选择性为94.3%. 当水蒸汽处理温度≤350 ℃时, 催化剂乙烷转化率增加, 并且随着水蒸汽处理温度的升高, 乙烷转化率逐渐降低, 分别为23.1% (150 ℃)、20.9% (250 ℃)和19.9% (350 ℃), 同时乙烯选择性比未水蒸汽处理的NiGaAl有所降低, 分别为91.0%、91.5%和93.0%. 当水蒸汽处理温度进一步升高到450和550 ℃时, 相比于NiGaAl, 乙烷转化率分别降低为17.5%和7.1%, 而乙烯的选择性(95.6%和97.7%)提高, 表明不同水蒸汽处理温度对催化剂性能产生的影响不同. 水蒸汽处理温度较低(≤350 ℃)有利于提高乙烷转化率, 但会降低乙烯选择性. 随着水蒸汽处理催化剂温度的升高(≥450 ℃), 乙烷转化率下降, 乙烯选择性提高. 且随着水蒸汽处理温度的升高, 反应24 h后乙烯收率下降比例减小, 如图9(b)所示, 150 ℃水蒸汽处理后乙烯收率下降比例为23.4%, 而高温550 ℃水蒸汽处理后乙烯收率下降比例仅有7.2%, 表明高温水蒸汽处理会提高催化剂的反应稳定性.
|
图 9 不同催化剂的(a) 催化性能 和 (b) 反应24 h后乙烯收率下降比例 Fig.9 (a) Catalytic performance, and (b) the decreased percentage of C2H4 yield after 24 h reaction of different catalysts |
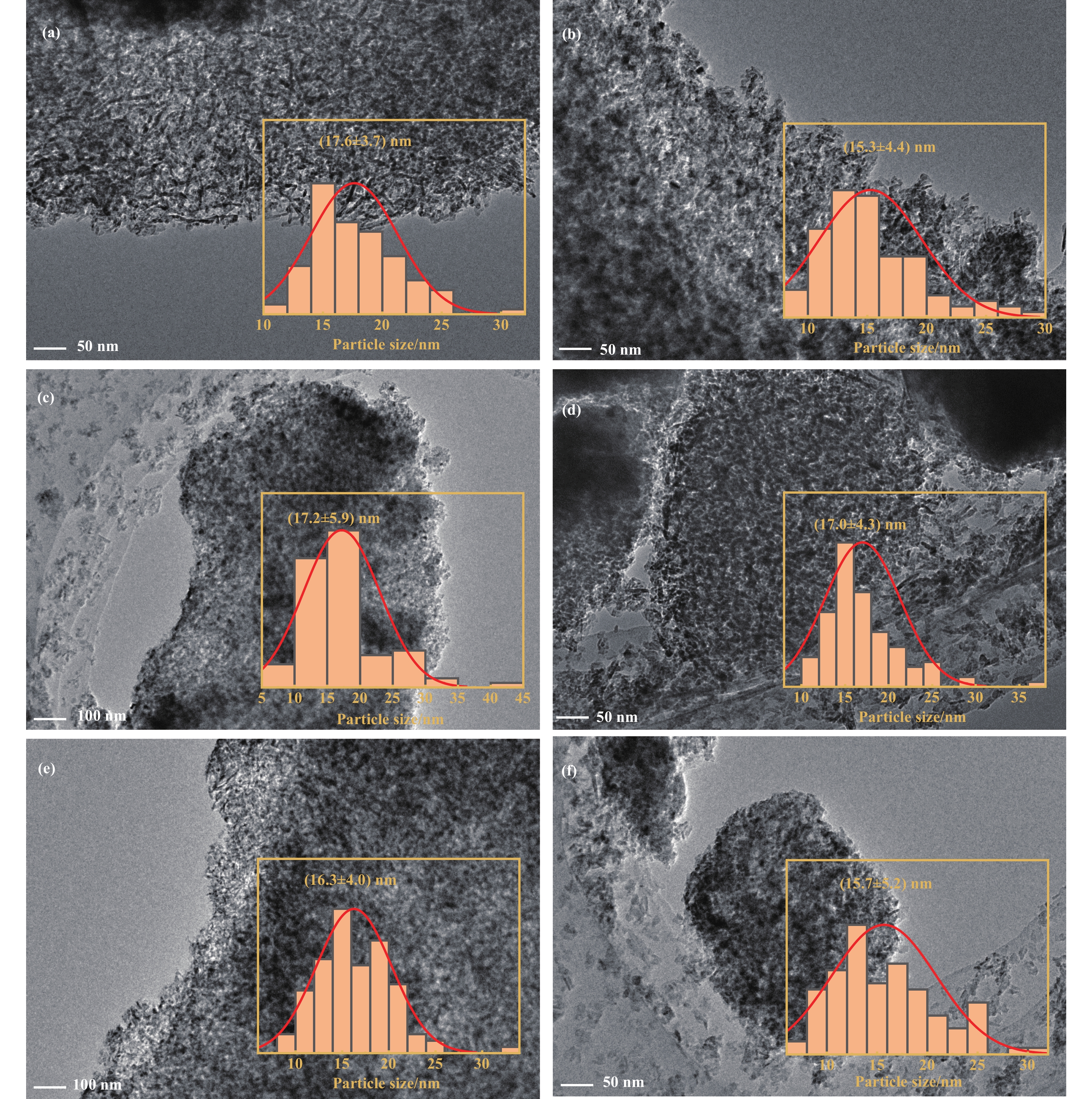
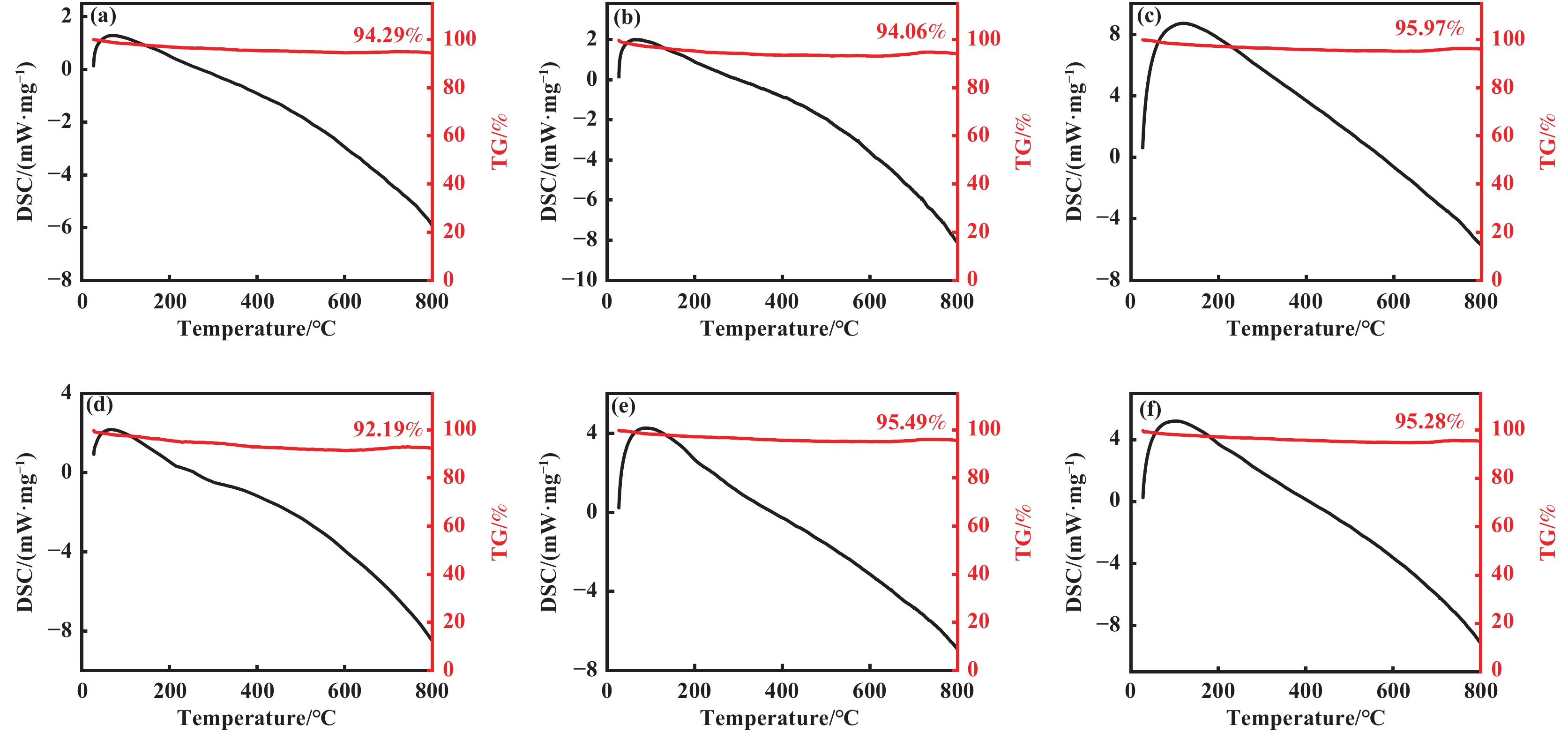
图10为反应24 h后催化剂的TEM图像. 反应24 h后催化剂的NiO粒径均增大, 表明在反应过程中存在活性组分的团聚导致颗粒尺寸增大. 进一步对反应24 h后催化剂进行TG-DSC分析, 如图11所示. 乙烷脱氢制乙烯产生的积碳通常在TG中的失重温度范围为400~700 ℃[32]. TG测试中400~700 ℃的失重率为5%左右, 但在该温度范围中, DSC曲线上并没有表现出积碳燃烧反应的放热信号. 由于催化剂采用大比表面积γ-Al2O3做载体, 因此推测400~700℃的失重是由于催化剂表面的强化学吸附的H2O或OH在高温下的脱附. 除此之外, 催化剂的TG-DSC在700~800 ℃表现出轻微的增重现象, 这可能是由于表面配位不饱和的Ni被空气氧化或者形成了NiAl2O4相所致[33−34].
|
图 10 反应后不同催化剂的颗粒大小 Fig.10 Particle size of the used catalysts (a) NiGaAl, (b) NiGaAl-150, (c) NiGaAl-250, (d) NiGaAl-350, (e) NiGaAl-450 and (f) NiGaAl-550 |
|
图 11 反应后催化剂的热重-差示扫描量热图 Fig.11 The TG-DSC of the used catalysts (a) NiGaAl, (b) NiGaAl-150, (c) NiGaAl-250, (d) NiGaAl-350, (e) NiGaAl-450 and (f) NiGaAl-550 |
将反应前和反应24 h后催化剂的H2-TPR进行对比, 如图4(b)所示. 对H2-TPR谱图中出现的最高峰温度位移进行分析发现, 反应后NiGaAl的H2-TPR峰位置向高温方向移动, 由此说明反应条件下有利于增强金属-载体相互作用. 而NiGaAl-150催化剂反应前后的峰位移现象不明显, 随着水蒸汽处理温度升高, 反应后催化剂的H2-TPR出峰向低温方向移动, 且该低温位移现象逐渐减弱, 表明在水蒸汽处理的催化剂上存在反应过程中活性组分颗粒尺寸变大的现象.
综上所述, 考察了不同水蒸汽处理温度对NiGaAl催化剂物理化学性质和ODHE反应性能的影响. XRD和UV-Vis证明水蒸汽处理温度的升高, 形成了金属-载体间的强相互作用. H2-TPR进一步证明了低温水蒸汽处理(≤350 ℃)更有利于游离NiO的生成, 进而有利于提高乙烷的转化率, 与低温水蒸汽处理(≤350 ℃)催化剂的催化性能表现一致. 进一步提高水蒸汽处理的温度(≥ 450 ℃), 催化剂中金属-载体相互作用增强, LAS酸浓度增加, 有利于提高乙烯的选择性. XPS和quasi in-situ XPS表明水蒸汽处理催化剂可以促进催化剂中Ni、Ga和Al间电子转移, 且高温水蒸汽处理有利于活性组分和载体的稳定, 使得乙烯收率下降比例减小.
3 结论采用不同温度水蒸汽处理NiGaAl催化剂, 不同水蒸汽处理温度对催化剂性能产生的影响不同, 且水蒸汽处理可以提高催化剂的稳定性. 不同温度水蒸汽处理的影响主要体现在低温水蒸汽处理(≤350 ℃)催化剂更有利于游离NiO的生成, 进而提高乙烷转化率; 高温水蒸汽处理(≥450 ℃)有利于增强NiGaAl催化剂中金属-载体相互作用, LAS酸浓度增加, 进而提高乙烯选择性. 同时不同水蒸汽处理温度还会影响催化剂中的电子转移, 高温水蒸汽处理有利于活性组分和载体的稳定. 该水蒸汽处理催化剂的方法为后续构筑高效乙烷氧化脱氢制乙烯催化剂提供了重要参考价值.
| [1] |
h-BN-doped Na2WO4-Mn/SiO2 catalysts for oxida-tive dehydrogenation of ethane to ethylene(h-BN掺杂Na2WO4-Mn/SiO2催化剂用于乙烷氧化脱氢制乙烯)[J]. J Mol Catal (China)(分子催化), 2020, 34(6): 495–504.
DOI:10.16084/j.cnki.issn1001-3555.2020.06.001 |
| [2] |
Oxidative dehydrogenation of ethane: Catalytic and mechanistic aspects and future trends[J]. Chem Soc Rev, 2021, 50(7): 4564–4605.
DOI:10.1039/D0CS01518K |
| [3] |
Unraveling the contribution of structural phases in Ni-Nb-O mixed oxides in ethane oxidative dehydrogenation[J]. Catal Today, 2012, 192(1): 169–176.
DOI:10.1016/j.cattod.2011.12.022 |
| [4] |
Oxidative dehydrogenation of ethane over NiO-CeO2 mixed oxides catalysts[J]. Catal Today, 2012, 180(1): 51–58.
DOI:10.1016/j.cattod.2011.03.056 |
| [5] |
Template-induced mesoporous Ni-Al oxide catalysts with tuned physico-chemical properties for the oxidative dehydrogenation of ethane[J]. Chem Eng J, 2023, 452(1): 139247.
DOI:10.1016/j.cej.2022.139247 |
| [6] |
Ni-Me-O mixed metal oxides for the effective oxidative dehydrogenation of ethane to ethylene-Effect of promoting metal Me[J]. J Catal, 2010, 270(1): 67–75.
DOI:10.1016/j.jcat.2009.12.004 |
| [7] |
Promoted NiO catalysts for the oxidative dehydrogenation of ethane[J]. Top Catal, 2014, 57: 1248–1255.
DOI:10.1007/s11244-014-0288-2 |
| [8] |
Precursors of active Ni species in Ni/Al2O3 catalysts for oxidative dehydrogenation of ethane[J]. Chin J Catal, 2013, 34(10): 1905–1913.
DOI:10.1016/S1872-2067(12)60672-X |
| [9] |
Catalysts based on Ni-Fe oxides supported on γ-Al2O3 for the oxidative dehydrogenation of ethane[J]. Catal Today, 2020, 356(1): 312–321.
DOI:10.1016/j.cattod.2019.05.044 |
| [10] |
Influence of preparation methods and CeO2 promoter on oxidative dehydrogenation of ethane to ethylene over Ni based catalysts(乙烷氧化脱氢制乙烯反应中制备方法及助剂对镍基催化剂性能的影响)[J]. J Mol Catal (China)(分子催化), 2007, 21(3): 209–214.
DOI:10.16084/j.cnki.issn1001-3555.2007.03.004 |
| [11] |
Study of oxygen species on CeO2-NiO/A2O3 for oxidative dehydrogenation of ethane to ethylene(乙烷氧化脱氢制乙烯CeO2-NiO/A2O3催化剂上氧物种的研究)[J]. J Mol Catal (China)(分子催化), 2007, 21(4): 344–350.
DOI:10.16084/j.cnki.issn1001-3555.2007.04.005 |
| [12] |
On ethane ODH mechanism and nature of active sites over NiO-based catalysts via isotopic labeling and methanol sorption studies[J]. J Catal, 2015, 322: 118–129.
DOI:10.1016/j.jcat.2014.11.014 |
| [13] |
The effects of doping alumina with silica in alumina-supported NiO catalysts for oxidative dehydrogenation of ethane[J]. Microporous Mesoporous Mater, 2020, 293: 109799.
DOI:10.1016/j.micromeso.2019.109799 |
| [14] |
Effect of calcination temperature on the structure and catalytic performance of the Ni/Al2O3 and Ni-Ce/Al2O3 catalysts in oxidative dehydrogenation of ethane[J]. Ind Eng Chem Res, 2015, 54(51): 12730–12740.
DOI:10.1021/acs.iecr.5b03425 |
| [15] |
Co-CeO2 interaction induces the Mars-van Krevelen mechanism in dehydrogenation of ethane[J]. J Phys Chem C, 2021, 125(21): 11411–11418.
DOI:10.1021/acs.jpcc.1c02855 |
| [16] |
Impact of surface-active site heterogeneity and surface hydroxylation in Ni doped ceria catalysts on oxidative dehydrogenation of propane[J]. J Catal, 2022, 413: 681–691.
DOI:10.1016/j.jcat.2022.07.019 |
| [17] |
Reaction-induced strong metal-support interactions between metals and inert boron nitride nanosheets[J]. J Am Chem Soc, 2020, 142(40): 17167–17174.
DOI:10.1021/jacs.0c08139 |
| [18] |
Promoting Ag/Al2O3 performance in low-temperature H2-C3H6-SCR by thermal pretreatment of γ-alumina in water[J]. Catal Lett, 2016, 146(12): 2622–2629.
DOI:10.1007/s10562-016-1864-9 |
| [19] |
Al ionic radius influence on molecular dynamics simulations of γ-Al2O3[J]. Catal Lett, 1994, 26: 259–267.
DOI:10.1007/BF00810598 |
| [20] |
DNA binding to mica correlates with cationic radius: Assay by atomic force microscopy[J]. Biophys J, 1996, 70(4): 1933–1939.
DOI:10.1016/S0006-3495(96)79757-6 |
| [21] |
Operando identification of a side-on nickel superoxide intermediate and the mechanism of oxygen evolution on nickel oxyhydroxide[J]. Chem Catal, 2023, 3(1): 100475.
DOI:10.1016/j.checat.2022.11.014 |
| [22] |
Ni/NiO nano-sheets for alkaline hydrogen evolution reaction: In situ electrochemical-Raman study[J]. Electrochim Acta, 2020, 361: 137040.
DOI:10.1016/j.electacta.2020.137040 |
| [23] |
Effect of Ni/Al molar ratio on the performance of substoichiometric NiAl2O4 spinel-based catalysts for partial oxidation of methane[J]. Appl Catal B-Environ, 2017, 209: 128–138.
DOI:10.1016/j.apcatb.2017.02.063 |
| [24] |
Characterization of none and yttrium-modified Ni-based catalysts for dry reforming of methane[J]. Appl Catal B-Environ, 2020, 278: 119335.
DOI:10.1016/j.apcatb.2020.119335 |
| [25] |
Synthesis, characterization and catalytic activity during hydrodesulphurization of dibenzothiophene of NiMoW catalysts supported on Al-Ti mixed oxides modified with MgO[J]. Fuel, 2012, 100: 57–65.
DOI:10.1016/j.fuel.2011.12.040 |
| [26] |
In situ controllable assembly of layered-double-hydroxide-based nickel nanocatalysts for carbon dioxide reforming of methane[J]. Catal Sci Technol, 2015, 5(3): 1588–1597.
DOI:10.1039/c4cy01302f |
| [27] |
A study of Ni/Al2O3 and Ni-La/Al2O3 catalysts for the steam reforming of ethanol and phenol[J]. Appl Catal B-Environ, 2015, 174/175: 21–34.
DOI:10.1016/j.apcatb.2015.02.024 |
| [28] |
Hollow NiO nanofibers modified by citric acid and the performances as supercapacitor electrode[J]. Electrochim Acta, 2013, 92: 197–204.
DOI:10.1016/j.electacta.2013.01.009 |
| [29] |
Effect of the nickel precursor on the impregnation and drying of γ-Al2O3 catalyst bodies: A UV-Vis and IR microspectroscopic study[J]. J Phys Chem C, 2008, 112(18): 7201–7209.
DOI:10.1021/jp710676v |
| [30] |
Ni-Al2O3 catalysts prepared by solution combustion method for syngas methanation[J]. Catal Commun, 2012, 17: 34–38.
DOI:10.1016/j.catcom.2011.10.010 |
| [31] |
Probing acid sites in solid catalysts with pyridine UV-Vis spectroscopy[J]. Phys Chem Chem Phys, 2018, 20(33): 21647–21659.
DOI:10.1039/C8CP03991G |
| [32] |
Effect of the impregnation sequence on the catalytic performance of Zn modified Cr/SiO2 catalyst for the oxidative dehydrogenation of ethane to ethylene with CO2(浸渍顺序对Zn改性Cr/SiO2 催化剂在CO2氧化乙烷脱氢制乙烯反应中催化性能的影响)[J]. Chem Res Appl(化学研究与应用), 2018, 30(9): 1493–1500.
DOI:10.3969/j.issn.1004-1656.2018.09.014 |
| [33] |
Effect of NiAl2O4 formation on Ni/Al2O3 stability during dry reforming of methane[J]. ChemCatChem, 2015, 7(16): 2508–2516.
DOI:10.1002/cctc.201500379 |
| [34] |
Effects of doping with CeO2 and calcination temperature on physicochemical properties of the NiO/Al2O3 system[J]. Cent Eur J Chem, 2009, 7(4): 780–786.
DOI:10.2478/s11532-009-0062-7 |
 2025, Vol. 39
2025, Vol. 39


