人类对环境的严重破坏和对能源的过度开采阻碍了社会的发展与进步. 因此, 新能源的开发已经成为当今世界的重大研究课题. 氢气因其绿色环保且可储存的特性而备受关注. 半导体光催化制氢因其制氢方法简单且副产物为经济实用的氧气成为研究热点[1−2]. 常见的光催化剂包括TiO2[3], g-C3N4[4](石墨相氮化碳)和CdS[5]等, 随着越来越多光催化剂的发现, Ga2O3作为一种具有适宜水分解能带结构的金属氧化物开始进入研究者的视野[6]. Ga2O3是一种宽带隙半导体(4.9 eV), 共有α, β, γ, δ, ε五种晶相, 其中β相不仅最为稳定[7−8], 还表现出了更高的催化活性[9]. 然而, 本征β-Ga2O3的带隙较宽, 材料仅在紫外光区有强的光吸收, 紫外光仅占太阳光谱的4%, 这极大限制了对太阳光谱的利用. 为提升宽禁带半导体在可见光区的光吸收能力, 掺杂被认为是一种有效的方法[10−11].
已有研究者通过不同金属元素掺杂β-Ga2O3以提升光催化性能, 取得了较好的效果. Katsuya Shimura等[12]研究了掺杂浓度对光催化性能的影响, 该团队采用均相沉淀法制备了Zn掺杂的 β-Ga2O3样品, 实验表明低掺杂量的Zn2+提高了光催化活性, 高掺杂量的Zn2+降低了光催化活性. Kim, Sunjae等[13]采用水热法合成了不同浓度Al掺杂的β-Ga2O3纳米结构, 通过掺杂少量的Al来增强光催化活性, 这些原子可能在带隙中产生浅层能级陷阱, 这些浅阱通过分离光生电子-空穴对来延缓复合过程. 虽然实验上对金属掺杂改善β-Ga2O3光催化活性进行了一些研究, 但关于掺入的杂质是否稳定, 可见光区光吸收能力如何, 以及光生电子空穴的复合几率如何等尚未系统深入研究.
本文基于密度泛函理论, 从形成能、电子结构、有效质量、带边位置和光学性质五个方面研究了Sr、Ba、V、Nb、Ta等二十种元素掺杂后对β-Ga2O3光催化分解水的影响. 研究结果将为合成高效的β-Ga2O3光催化剂提供有价值的参考.
1 计算模型和方法β-Ga2O3其空间群为 C2/m, 单斜晶体. 晶格常数为a=
|
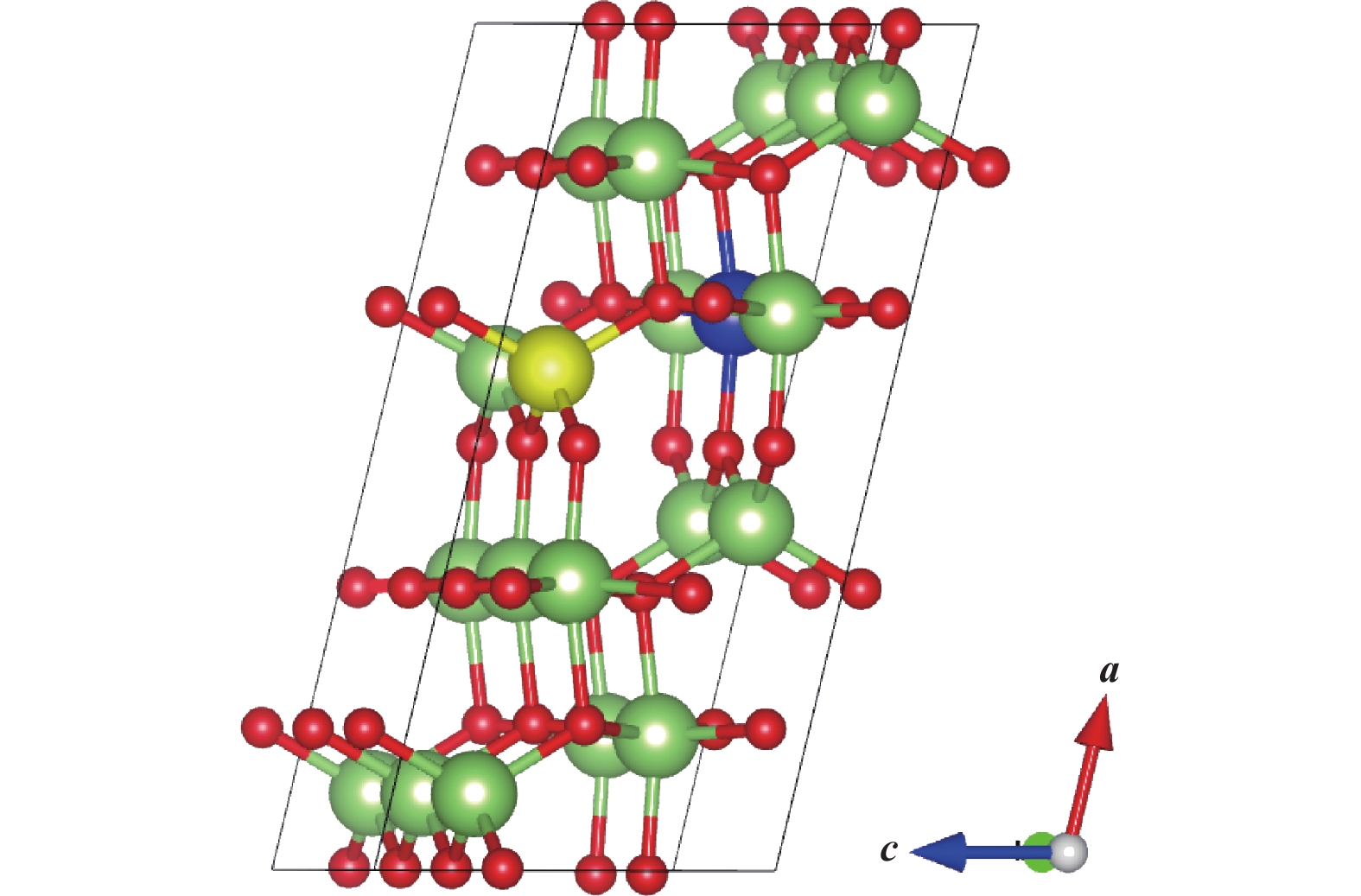
图 1 本征β-Ga2O3晶体结构示意图, 红色球代表O原子, 绿色球代表Ga原子, 黄色球代表Ga1位点, 蓝色球代表Ga2位点 Fig.1 Schematic illustration of the intrinsic β-Ga2O3 crystal structure. Red spheres represent O atoms, green spheres represent Ga atoms, yellow spheres represent Ga1 sites, and blue spheres represent Ga2 sites |
本文基于密度泛函理论[17−18]探究金属掺杂β-Ga2O3的相关性质. 电子和离子之间的相互作用采用投影缀加波方法展开, 交换关联势采用PBE(perdew burke ernzerhof, PBE)[19−20]泛函进行处理. 由于使用PBE泛函计算电子结构得到的带隙一般小于实验值, 为了获得金属掺杂后更加准确的禁带宽度和带边电势位置, 采用了杂化密度泛函(hybrid functional, HSE06)[21]计算材料的能带结构. 在计算过程中, 平面基组的截断能为550 eV, 能量收敛判据为10–6 eV·nm−1, 力收敛判据为0.002 eV·nm−1, 静态计算中布里渊区k点的选取采用Gamma方法, 网格大小为3×6×6, 高斯展开SIGMA设置为0.05.
2 计算结果与讨论 2.1 金属掺杂形成能本文主要研究金属原子替位掺杂对β-Ga2O3光催化性能的影响. 通过计算形成能可以确定金属掺杂后最稳定的掺杂位点, 从而为构建光催化的掺杂模型提供依据.
为研究金属掺杂β-Ga2O3后的掺杂形成能, 在文中引入了掺杂形成能的计算公式[22]:
| $ {E}_{\mathrm{f}}={E}_{x-\mathrm{d}\mathrm{o}\mathrm{p}\mathrm{e}\mathrm{d}}+{\mu }_{\mathrm{G}\mathrm{a}}-{E}_{\mathrm{u}\mathrm{n}\mathrm{d}\mathrm{o}\mathrm{p}\mathrm{e}\mathrm{d}}-{\mu }_{\mathrm{M}} $ | (1) |
Ex-doped代表掺杂体系的总能量, Eundoped代表未掺杂体系的总能量, μGa和μM分别代表Ga原子和掺杂金属原子的化学势. μGa受β-Ga2O3体系合成条件的影响, 根据它们的化学计量比, β-Ga2O3中各组成元素的化学势必须符合公式(2):
| $ 2{\mu }_{\mathrm{G}\mathrm{a}}+3{\mu }_{\mathrm{O}}={\mu }_{\mathrm{G}{\mathrm{a}}_{2}{\mathrm{O}}_{3}} $ | (2) |
根据制备环境不同, μGa计算方法也不同. 富镓条件下, 通过优化体相镓晶体结构求出一个Ga原子的平均能量; 富氧条件下, 先在边长为1.5 nm的立方体晶胞中优化氧气分子, 计算氧气分子能量的一半得到μO, 再根据公式(2)计算出μGa. 金属元素的化学势μM等效于把单个金属原子放入一个10×10×10[23]的立方晶胞中计算得到的总能量. 掺杂金属后体系的掺杂形成能计算结果如图2所示:
|
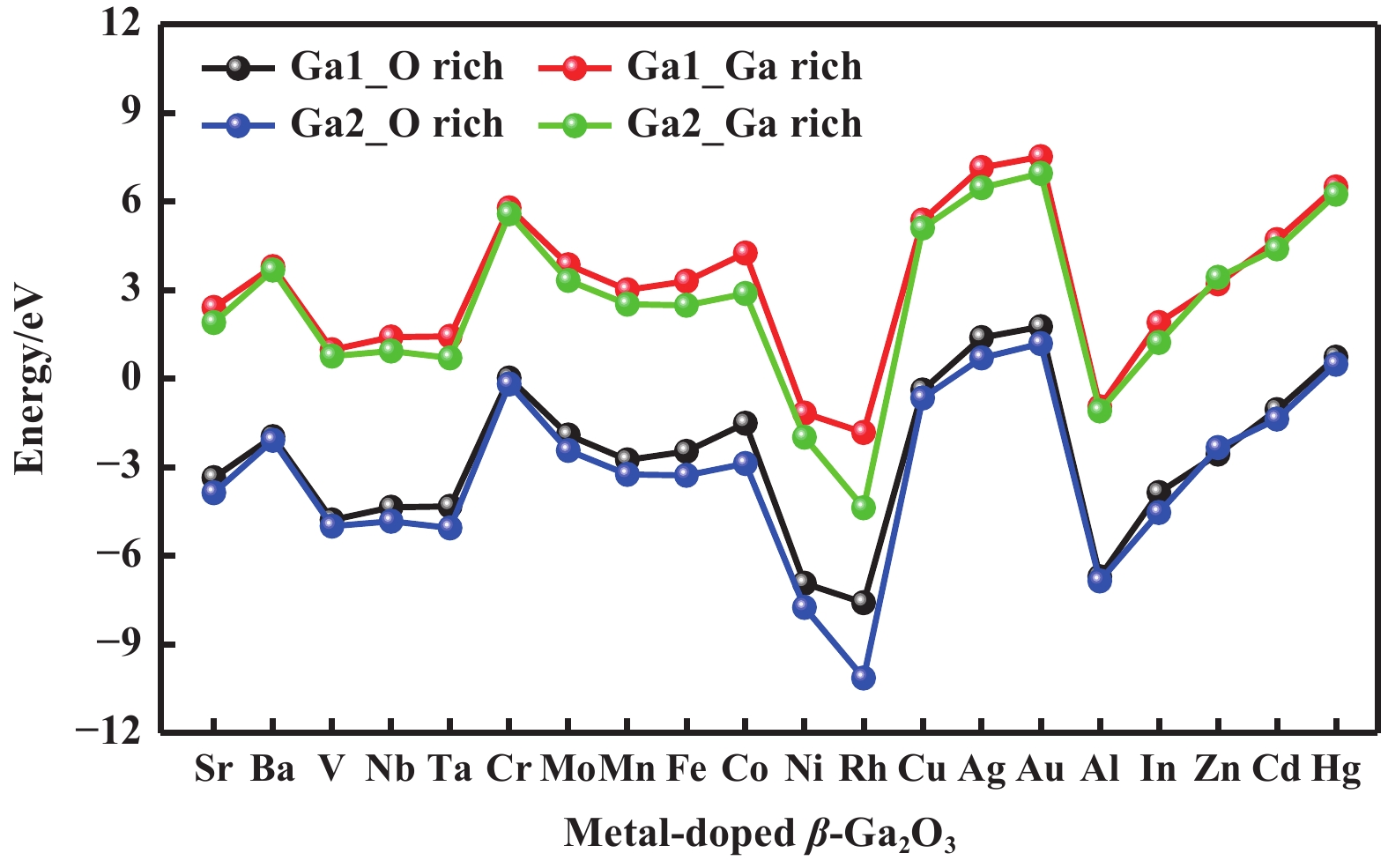
图 2 各金属掺杂β-Ga2O3后的掺杂形成能 Fig.2 Doping formation energies for various metal-doped β-Ga2O3 |
从图2可看出, 与富Ga条件相比, 富O下所有杂质的形成能较低; 其次, 比较掺杂两个Ga位点的形成能, 发现除Zn外, 所有元素掺杂Ga2位点的形成能均低于Ga1位点, 这表明多数金属原子置换高配位数的Ga2位点比置换低配位数的Ga1位点更容易; 此外, 在同一主族中, 掺杂形成能随着原子尺寸的增大而增大, 如V<Nb<Mo, Cu<Ag<Au, 表明随着原子尺寸增大掺杂越困难.
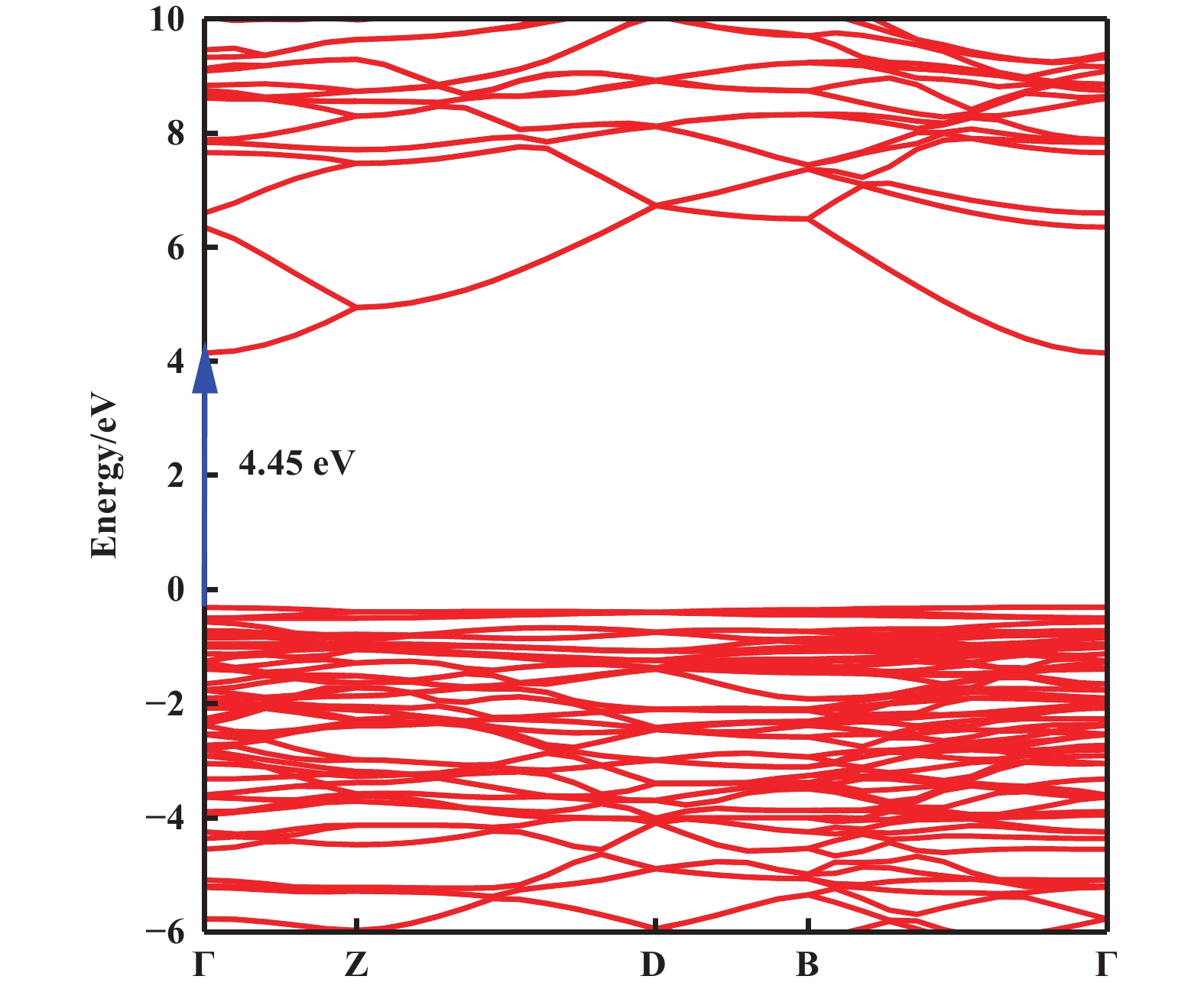
2.2 金属掺杂对能带结构的影响本征β-Ga2O3的能带结构. 从图3可看出本征β-Ga2O3的导带底(CBM)与价带顶(VBM)均位于Γ点, 表明本征β-Ga2O3是直接带隙半导体. 计算后的带隙值为4.45 eV, 这与之前的计算结果类似, 表明了计算结果的可靠性[24−26].
|
图 3 本征β-Ga2O3的能带结构 Fig.3 Band structure of intrinsic β-Ga2O3 |
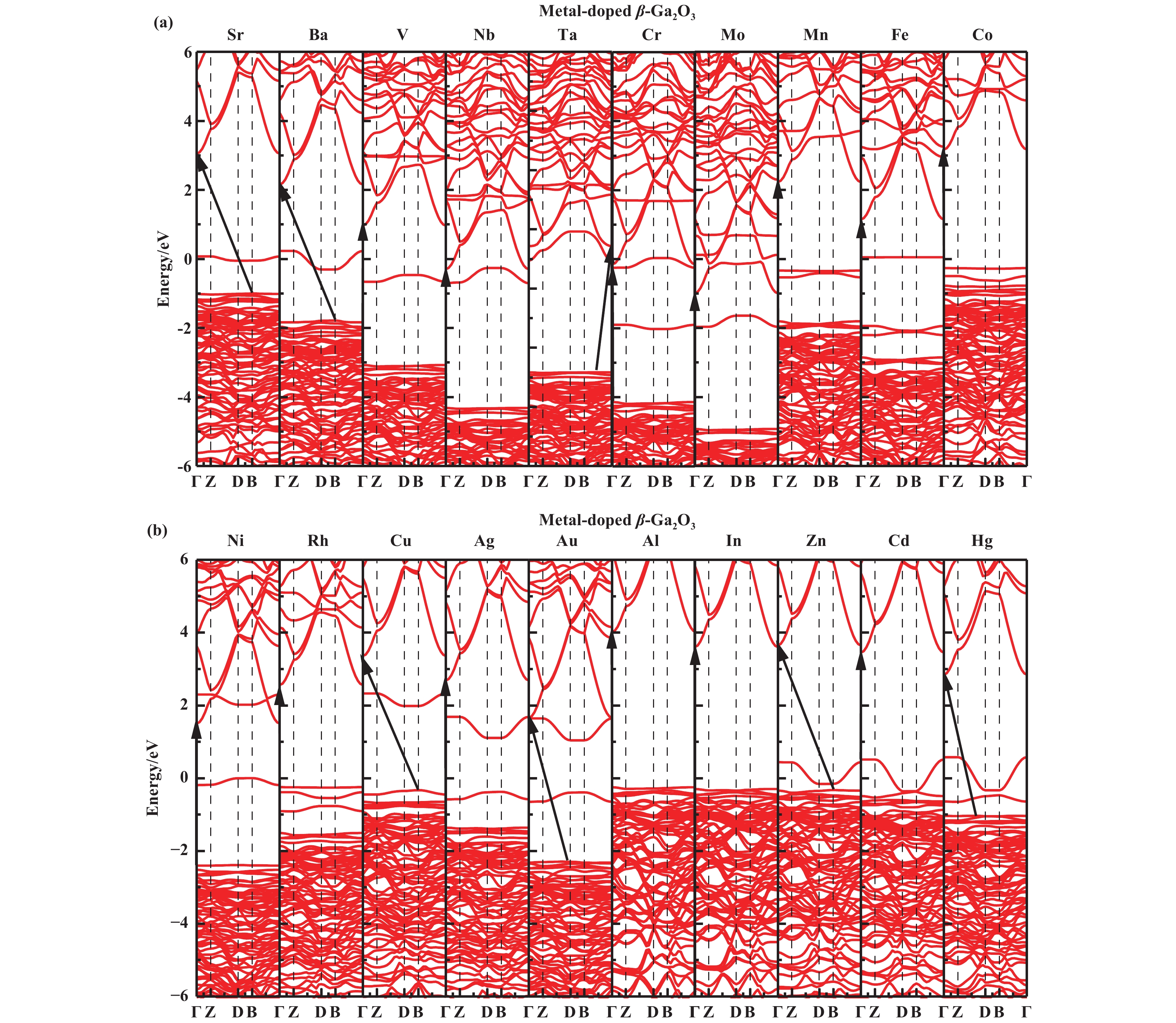
金属掺杂对β-Ga2O3能带结构的影响. 图4是本文研究的二十种金属掺杂β-Ga2O3后的能带结构. 其中图4(a)是Sr、Ba、V、Nb、Ta、Cr、Mo、Mn、Fe、Co分别掺杂β-Ga2O3后的能带结构, 图4(b)是Ni、Rh、Cu、Ag、Au、Al、In、Zn、Cd、Hg分别掺杂β-Ga2O3后的能带结构.
|
图 4 金属掺杂β-Ga2O3后的能带结构 Fig.4 Band structures of metal-doped β-Ga2O3 |
除Al和In外, 其余元素的掺杂都产生了杂质能级, 这主要是由于掺杂元素与Ga有不同的价电子数. 不同位置的杂质能级对光生载流子的分离与复合有不同的影响, 一方面, 杂质能级将禁带分为两个子带隙, 可以使光生载流子吸收小于带隙能量的光子便可跃迁至导带, 增加了可利用的光子数, 有利于光催化效率的提高; 另一方面, 杂质能级可作为陷阱中心促进电子空穴的复合, 不利于提高光催化效率. 通常情况下, VBM附近的浅杂质能级有利于电荷分离, CBM附近的深杂质态容易成为复合中心, 分离与复合取决于VBM与杂质能级和CBM与杂质能级之间的能量差[27−28]. Sr、Co、Rh、Zn、Cd、Hg掺杂后的VBM与杂质能级最小值之间的能量差远小于CBM与杂质能级最大值之间的能量差, 因此VBM中的空穴泵入杂质能级的几率将大于CBM中的电子与杂质能级中空穴复合的几率, 有利于光生载流子的分离, 提高光催化效率. 杂质能级的形态也对光催化效率有不同的影响, 有研究表明[29−31], 平坦的杂质能级会成为电子空穴的复合中心, 弯曲的杂质能级有利于光生载流子的分离, 主要是由于弯曲的杂质能级上的电子和空穴有较小的有效质量, 较高的迁移率. 因此, Zn、Cd、Hg掺杂后弯曲的杂质能级是电子空穴的有效分离中心.
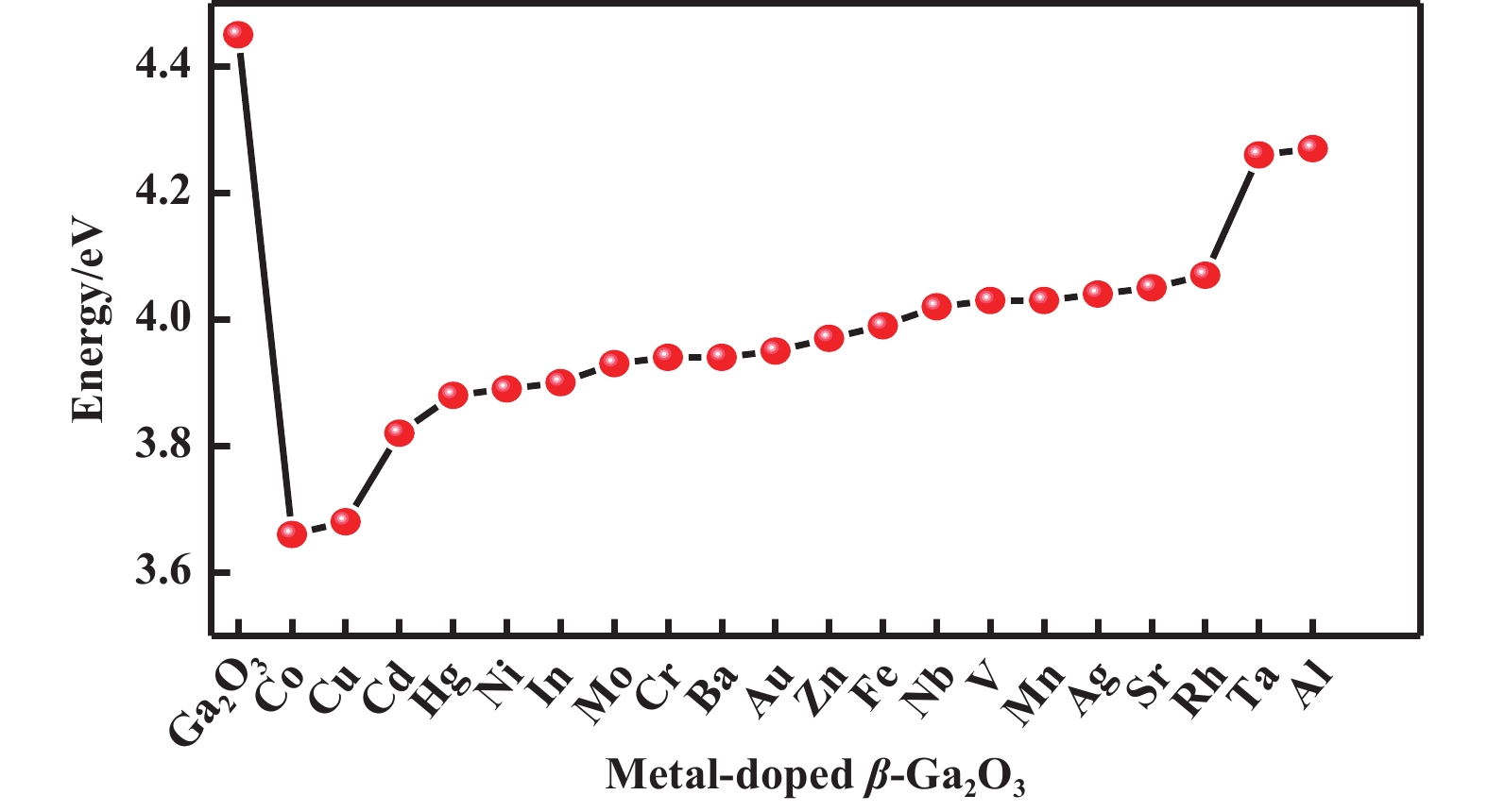
掺杂金属后的带隙值如图5所示, 带隙值按照图中的顺序依次增大, 且相比于本征β-Ga2O3的带隙值均有所减小, 带隙的减小有利于光吸收向可见光方向红移. 从能带类型来看, Sr、Ba、Ta、Cu、Au、Zn、Cd、Hg掺杂后的能带为间接带隙, 对间接带隙材料来说, 光激发的价带电子在吸收能量的同时需要改变动量才能跃迁至导带, 降低了材料中光生电子和空穴的复合概率[32−33], 有利于光催化效率的提高.
|
图 5 金属掺杂β-Ga2O3后的带隙值 Fig.5 The bandgap values of β-Ga2O3 after metal doping |
为研究金属元素掺杂β-Ga2O3材料后哪些元素有利于载流子的分离, 因此对掺杂后材料的光生载流子的相对有效质量(D)进行了研究. 通过研究D值, 可以确定电子-空穴分离效率[34−35]. 根据能带结构对CBM和VBM的抛物线拟合, 可得到金属掺杂β-Ga2O3后的电子和空穴有效质量, 电子和空穴有效质量计算如公式(3)[36]:
| $ \;{m}^{*}\text{=}\pm \frac{{h}^{2}}{{d}^{2}E/d{k}^{2}} $ | (3) |
表1是不同金属掺杂后材料中光生电子和空穴的有效质量, 计算表明, 无论是本征β-Ga2O3还是金属掺杂的β-Ga2O3, 光生电子的有效质量均显著低于空穴的有效质量, 这表明β-Ga2O3是一种轻激发电子、重激发空穴的半导体类型. 与本征β-Ga2O3相比, 除Co、Cd和In元素掺杂外, 其他元素的掺杂使β-Ga2O3中的光生电子有效质量减小, 而空穴有效质量增加. 这种轻电子和重空穴的特性对于光生电子和空穴的分离是有利的, 可显著提高β-Ga2O3的光催化活性.
| 表 1 金属掺杂β-Ga2O3后的电子空穴有效质量和电子-空穴相对有效质量 Table 1 Effective mass of electrons and holes and the relative effective masses of electron-hole pairs for the metal-doped β-Ga2O3 |
进一步计算电子-空穴相对有效质量, 并根据以下公式对本征β-Ga2O3及金属掺杂后的β-Ga2O3进行重组率和光催化活性的评估[37]:
| $ D=\frac{{{m}_{\mathrm{h}}}^*}{{{m}_{\mathrm{e}}}^*} $ | (4) |
D表示相对有效质量,
半导体的能带边缘位置是预测半导体光催化剂性能的重要指标. 为了实现光催化水分解生成氢气(H2)和氧气(O2), 半导体的能带结构需满足以下条件: 导带底(CBM)应低于H+/H2的还原电极电位(0 eV, 相对于标准氢电极, pH=0), 而价带顶(VBM)应高于O2/H2O的氧化电极电位(1.23 eV, 相对于标准氢电极, pH=0)[38−44].
因此, 本文进一步研究了金属掺杂对带边位置的影响. 为描述金属掺杂β-Ga2O3体系的带边与水分解氧化还原电位的关系, 采用公式(5)计算带边位置[45]:
| $ {E}_{\mathrm{C}\mathrm{B}}=X-\frac{1}{2{E}_{\mathrm{g}}}-{E}_{0} $ | (5) |
Eg是金属掺杂后的能带带隙, E0是氢尺度上自由电子的能量(~4.5 eV), EVB根据Eg和ECB的差值确定. X为掺杂金属体系的绝对电负性, 可由公式(6)得出:
| $ X={\left[X\right(A)}^{a}{X\left(B\right)}^{b}{X\left(C\right)}^{c}{]}^{\tfrac{1}{a+b+c}} $ | (6) |
由上述公式可得本征β-Ga2O3的ECB和EVB分别是
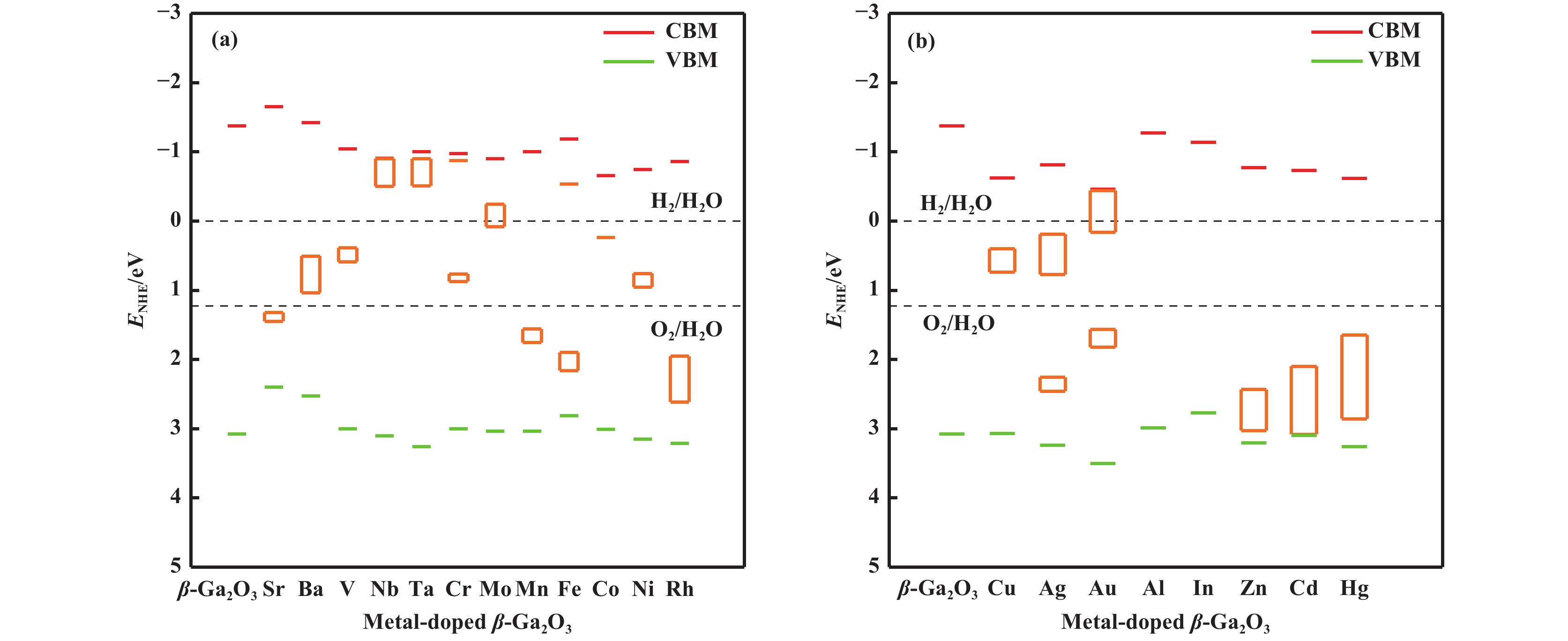
|
图 6 金属元素掺杂β-Ga2O3后的带边位置 (a) Sr、Ba、V、Nb、Ta、Cr、Mo、Mn、Fe、Co、Ni、Rh掺杂后的带边位置图; (b) Cu、Ag、Au、Al、In、Zn、Cd、Hg掺杂后的带边位置图 Fig.6 (a) Band edge positions of β-Ga2O3 doped with metal elements Sr, Ba, V, Nb, Ta, Cr, Mo, Mn, Fe, Co, Ni, and Rh;(b) Band edge positions of β-Ga2O3 doped with metal elements Cu, Ag, Au, Al, In, Zn, Cd, and Hg |
由上述研究可知同时满足低形成能、高电子空穴分离效率、合适带边条件的杂质有: Sr、Nb、Ta、Mn、Fe、Zn、Hg七种元素, 说明这些金属元素可作为良好的光催化掺杂剂. 光催化剂的光吸收能力是决定光催化效率的关键因素之一. 由于太阳光谱中紫外光仅占4%, 而可见光占比高达45%, 因此, 为了尽可能有效地利用太阳光的能量, 一种理想的光催化材料应该在可见光-近红外范围有强的光吸收, 以提高对太阳光的利用率. 通过计算介电函数的实部和虚部可得出未掺杂和以上六种杂质掺杂β-Ga2O3后的光吸收系数, 其计算公式如下[46]:
| $ \alpha (\omega ) = {\sqrt {2\omega }} {\left[{ \sqrt {{\varepsilon _1}^2(\omega ) - {\varepsilon _2}^2(\omega )} - {\varepsilon _1}(\omega )}\right]}^{{1/2}} $ | (7) |
其中ω, α(ω), ε1(ω), ε2(ω)分别为光子频率, 吸收系数, 相对介电函数的实部和虚部.
如图7所示, β-Ga2O3在紫外光区有强的吸收能力而在红外光区没有光吸收能力. 掺杂Sr、Nb和Ta元素后, 材料在红外光区的光吸收系数显著增强, 其中Nb和Ta掺杂后, 在0.5 eV附近的光吸收峰值均超过了1×105 cm−1. 然而, 这两种元素的掺杂也导致紫外光区的光吸收系数显著下降. 从图4(a)可知, Nb和Ta掺杂均使CBM位置显著下移, Nb的CBM位置甚至跨越了费米能级, 这可能是导致光吸收在红外光区出现明显增强的原因. Mn和Fe掺杂显著提升了材料在紫外光区和可见光区的光吸收系数, 特别在3 eV附近可见光区域, 光吸收系数提升至1×105 cm−1; Zn掺杂则主要在红外光区显示出明显的光吸收增强效果. Hg掺杂β-Ga2O3的光吸收系数从红外至深紫外连续光谱带均有较为显著地提升. 这些结果表明, 掺杂元素对β-Ga2O3的光吸收特性有着显著的调节作用, 不同掺杂元素的影响机制和光谱响应特性有所差异.
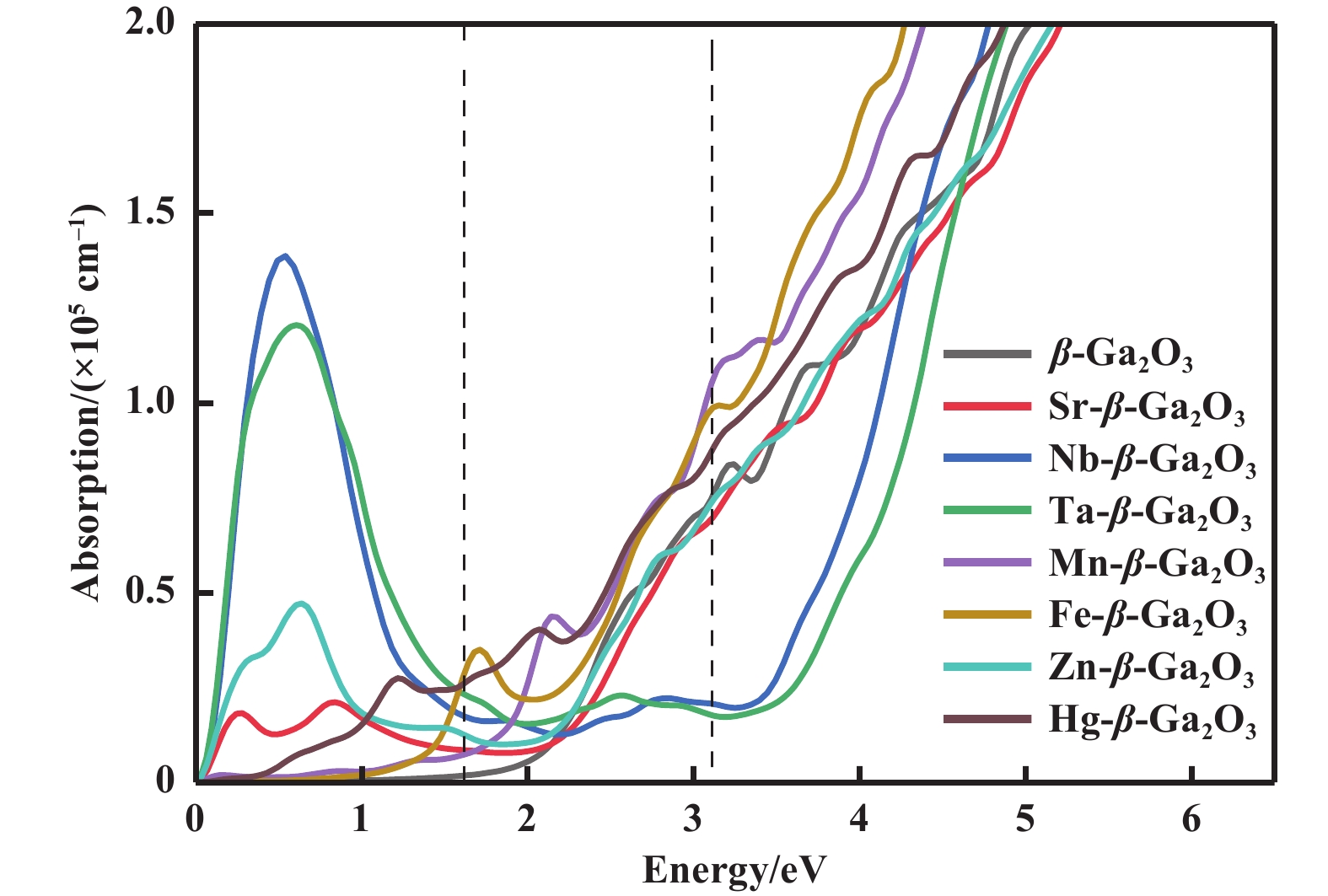
|
图 7 本征β-Ga2O3及掺杂Sr、Nb、Ta、Mn、Fe、Zn、Hg后的光吸收系数 Fig.7 The optical absorption spectra of intrinsic β-Ga2O3 and β-Ga2O3 doped with Sr, Nb, Ta, Mn, Fe, Zn and Hg |
本文从杂质形成能、电子结构、有效质量、带边位置和光学性质五个方面研究了Sr、Ba、V、Nb、Ta等二十种元素掺杂对β-Ga2O3光催化性能的影响. 结果表明, 金属掺杂β-Ga2O3可以有效提高光催化效率并拓宽吸收光谱. 具体如下:
(1) 计算了在富Ga富O条件下替位掺杂不同位点的掺杂形成能, 发现Zn在富O条件下形成能最低的位点是Ga1位点, 其余元素在富O条件下形成能最低的位点为Ga2位点.
(2) 基于最低形成能构型研究了不同金属掺杂β-Ga2O3的电子结构. 结果表明, Sr、Co、Rh、Zn、Cd、Hg掺杂后杂质能级为浅受主能级, 有助于光生电荷分离; Zn、Cd、Hg掺杂后引起杂质能级弯曲, 成为电子-空穴有效分离中心; 所有金属掺杂均使得β-Ga2O3带隙减小, 其中Co掺杂引起的带隙减小最为显著, 相较于本征β-Ga2O3减小了0.79 eV, 这一变化可促进光吸收向可见光区红移.
(3) 进一步计算掺杂后材料的电子-空穴相对有效质量(D). 结果表明, Co、Cd和In掺杂后的D值均小于本征β-Ga2O3 D值(12.23), 光生电子空穴分离效率较低. 相比之下, 掺杂Sr、Hg、Nb和Ta的D值相对于本征β-Ga2O3提高了7~10倍, 而掺杂Zn的D值为664, 远高于本征β-Ga2O3的D值, 表明这些元素的引入将会显著降低光生电子空穴的复合几率.
(4) 对掺杂后相对水分解氧化还原势的带边位置分析表明, Sr、Nb、Ta、Mn、Fe、Rh、Al、In、Zn、Cd、Hg 掺杂后的CBM、VBM和杂质能级位置均符合光催化分解水制氢的条件, 其余金属掺杂后不符合其条件.
综上所述, 同时满足低形成能、高电子空穴分离效率、合适的带边位置条件的元素有: Sr、Nb、Ta、Mn、Fe、Zn、Hg七种元素. 其中, Sr、Nb、Ta掺杂显著增强了材料的红外光吸收能力, Nb在0.5 eV处光吸收系数高达1.38×105 cm−1; Mn和Fe的掺杂显著增强了材料在紫外和可见光区的光吸收能力, 尤其在3 eV处可见光区域光吸收系数提升至1×105 cm−1; Zn掺杂强化了红外吸收; 而Hg掺杂则在红外至深紫外的全光谱范围内均表现出显著的光吸收增强效果, 是实现高效光催化制氢的最佳掺杂剂之一.
| [1] |
The properties of hydrogen as fuel tomorrow in sustainable energy system for a cleaner planet[J]. Int J Hydrogen Energy, 2005, 30(7): 795–802.
DOI:10.1016/j.ijhydene.2004.10.011 |
| [2] |
Photo-electrochemical hydrogen generation from water using solar energy. Materials-related aspects[J]. Int J Hydrogen Energy, 2002, 27(10): 991–1022.
DOI:10.1016/S0360-3199(02)00022-8 |
| [3] |
Metal-organic frameworks derived cake-like anatase/rutile mixed phase TiO2 for highly efficient photocatalysis[J]. J Alloys Compd, 2017, 690: 640–646.
DOI:10.1016/j.jallcom.2016.08.176 |
| [4] |
Enhanced visible-light H2 evolution of g-C3N4 photocatalysts via the synergetic effect of amorphous NiS and cheap metal-free carbon black nanoparticles as co-catalysts[J]. Appl Surf Sci, 2015, 358: 204–212.
DOI:10.1016/j.apsusc.2015.08.244 |
| [5] |
Efficient visible light-driven splitting of alcohols into hydrogen and corresponding carbonyl compounds over a Ni-modified CdS photocatalyst[J]. J Am Chem Soc, 2016, 138(32): 10128–10131.
DOI:10.1021/jacs.6b06860 |
| [6] |
Photocatalytic decomposition of H2O into H2 and O2 over Ga2O3 loaded with NiO[J]. Chem Lett, 2004, 33(6): 726–727.
DOI:10.1246/cl.2004.726 |
| [7] |
Thermodynamic assessment of the gallium-oxygen system[J]. J Am Ceram Soc, 2004, 87(4): 683–691.
DOI:10.1111/j.1551-2916.2004.00683.x |
| [8] |
Synthesis, characterization and photocatalytic activity of β-Ga2O3 nanostructures[J]. Powder Technol, 2010, 203(3): 440–446.
DOI:10.1016/j.powtec.2010.06.004 |
| [9] |
Efficient decomposition of benzene over a β-Ga2O3 photocatalyst under ambient conditions[J]. Environ Sci Technol, 2006, 40(18): 5799–5803.
DOI:10.1021/es061004s |
| [10] |
Effects of Zn2+ and Pb2+ dopants on the activity of Ga2O3-based photocatalysts for water splitting[J]. Phys Chem Chem Phys, 2013, 15(44): 19380–19386.
DOI:10.1039/c3cp53333f |
| [11] |
Development of Rh-doped Ga2O3 photocatalysts for reduction of CO2 by H2O as an electron donor at a more than 300 nm wavelength[J]. J Phys Chem C, 2018, 122(37): 21132–21139.
DOI:10.1021/acs.jpcc.8b04956 |
| [12] |
Effect of doped zinc species on the photocatalytic activity of gallium oxide for hydrogen production[J]. Phys Chem Chem Phys, 2012, 14(8): 2678–2684.
DOI:10.1039/c2cp23220k |
| [13] |
Impact of Al doping on a hydrothermally synthesized β-Ga2O3 nanostructure for photocatalysis applications[J]. RSC Adv, 2021, 11(13): 7338–7346.
DOI:10.1039/D1RA00021G |
| [14] |
A review of Ga2O3 materials, processing, and devices[J]. Appl Phys Rev, 2018, 5(1): 011301.
DOI:10.1063/1.5006941 |
| [15] |
Tailoring the electronic structure of β-Ga2O3 by non-metal doping from hybrid density functional theory calculations[J]. Phys Chem Chem Phys, 2015, 17(8): 5817–5825.
DOI:10.1039/C4CP05637J |
| [16] |
Theoretical study of metal-doped β-Ga2O3 photocatalysts for overall water splitting[J]. Theor Chem Acc, 2017, 136(7): 79.
DOI:10.1007/s00214-017-2112-0 |
| [17] |
Density functional theory[J]. Photosynth Res, 2009, 102(2/3): 443–453.
DOI:10.1007/s11120-009-9404-8 |
| [18] |
Self-consistent equations including exchange and correlation effects[J]. Phys Rev, 1965, 140(4A): A1133.
DOI:10.1103/PhysRev.140.A1133 |
| [19] |
Towards extending the applicability of density functional theory to weakly bound systems[J]. J Chem Phys, 2001, 115(19): 8748–8757.
DOI:10.1063/1.1412004 |
| [20] |
Simulation and calculation of conducting property of Zn1−xTMxO(TM = Al, Ga, In)(Zn1−xTMxO (TM=Al, Ga, In)导电性能的模拟计算)[J]. Acta Phys Sin(物理学报), 2013, 62(15): 157102.
DOI:10.7498/aps.62.157102 |
| [21] |
Hybrid functionals based on a screened Coulomb potential[J]. J Chem Phys, 2003, 118(18): 8207–8215.
DOI:10.1063/1.1564060 |
| [22] |
New insight into the enhanced visible-light photocatalytic activities of B-, C-and B/C-doped anatase TiO2 by first-principles[J]. Phys Chem Chem Phys, 2013, 15(29): 12040–12047.
DOI:10.1039/c3cp44651d |
| [23] |
严崇勇. p型掺杂宽禁带半导体β‐Ga2O3的第一性原理研究[D]. 西安: 西安电子科技大学, 2021. [Yan C Y. First-principles study on p-type doping wide band gap semiconductor β-Ga2O3[D]. Xi'an: Xidian University, 2021.]
Yan C Y. First-principles study on p-type doping wide band gap semiconductor β-Ga2O3[D]. Xi'an: Xidian University, 2021.
|
| [24] |
Crystal structure of β-Ga2O3[J]. J Chem Phys, 1960, 33(3): 676–684.
DOI:10.1063/1.1731237 |
| [25] |
Relaxation of crystals with the quasi-Newton method[J]. J Comput Phys, 1997, 131(1): 233–240.
DOI:10.1006/jcph.1996.5612 |
| [26] |
Band-to-band transitions, selection rules, effective mass, and excitonic contributions in monoclinic β-Ga2O3[J]. Phys Rev B, 2017, 96(24): 245205.
DOI:10.1103/PhysRevB.96.245205 |
| [27] |
High-throughput HSE study on the doping effect in anatase TiO2[J]. Phys Chem Chem Phys, 2020, 22(1): 39–53.
DOI:10.1039/C9CP04591K |
| [28] |
Insight into the enhanced photocatalytic activity of Mo and P codoped SrTiO3 from first-principles prediction[J]. RSC Adv, 2020, 10(66): 40117–40126.
DOI:10.1039/D0RA07026B |
| [29] |
Formation of an intermediate band in the energy gap of TiO2 by Cu-N-codoping: First principles study and experimental evidence[J]. Solar Energy Mater Solar Cells, 2014, 125: 120–126.
DOI:10.1016/j.solmat.2014.02.032 |
| [30] |
The new understanding on photocatalytic mechanism of visible-light response N-S codoped anatase TiO2 by first-principles[J]. Appl Catal B-Environ, 2013, 142: 45–53.
DOI:10.1016/j.apcatb.2013.04.063 |
| [31] |
Enhancing photocatalytic activity in monolayer MoS2 by charge compensated co-doping with P and Cl: First principles study[J]. Mol Catal, 2019, 468: 94–99.
DOI:10.1016/j.mcat.2019.02.002 |
| [32] |
Study of the electronic structure and photocatalytic activity of the BiOCl photocatalyst[J]. Appl Catal B-Environ, 2006, 68(3/4): 125–129.
DOI:10.1016/j.apcatb.2006.08.002 |
| [33] |
The characteristics and photocatalytic activities of BiOCl as highly efficient photocatalyst[J]. J Mol Struct, 2012, 1007: 196–202.
DOI:10.1016/j.molstruc.2011.10.046 |
| [34] |
Effects of triaxial strain on carrier activity, carrier lifetime, and absorption spectrum of (S, Se, Te) and 2 N Co-doped ZnO[J]. Vacuum, 2020, 182: 109684.
DOI:10.1016/j.vacuum.2020.109684 |
| [35] |
Tuning photocatalytic performance of the near-infrared-driven photocatalyst Cu2(OH)PO4 based on effective mass and dipole moment[J]. Phys Chem Chem Phys, 2014, 16(7): 3267–3273.
DOI:10.1039/c3cp53381f |
| [36] |
First-principle study of the effects of biaxial strain on the photocatalytic and magnetic mechanisms of ZnO with Sm doping and point defects (VZn, Hi)[J]. Vacuum, 2021, 189: 110225.
DOI:10.1016/j.vacuum.2021.110225 |
| [37] |
Towards better photocatalysts: First-principles studies of the alloying effects on the photocatalytic activities of bismuth oxyhalides under visible light[J]. Phys Chem Chem Phys, 2012, 14(3): 1286–1292.
DOI:10.1039/C1CP23516H |
| [38] |
Iron-doped C3N4/BiVO4 as a Z-scheme photocatalyst system for water splitting(铁掺杂氮化碳/ BiVO4构建Z型光催化全解水)[J]. J Mol Catal (China)(分子催化), 2024, 38(2): 112–120.
DOI:10.16084/j.issn1001-3555.2024.02.003 |
| [39] |
Sulfur-oxygen bonded BiVO4 photoanodes and FeNi catalysts toward efficient oxygen evolution(硫氧键合BiVO4光阳极与FeNi催化剂实现高效水氧化)[J]. J Mol Catal (China)(分子催化), 2023, 37(6): 535–544.
DOI:10.16084/j.issn1001-3555.2023.06.003 |
| [40] |
Photocatalytic hydrogen production performance of oxygen-containing vacancy-deficient bismuth tungstate(含氧空位缺陷钨酸铋光催化产氢性能研究)[J]. J Mol Catal (China)(分子催化), 2024, 38(2): 154–159.
DOI:10.16084/j.issn1001-3555.2024.02.008 |
| [41] |
Electronic structure and photocatalytic properties of copper-doped CaTiO3[J]. Int J Hydrogen Energy, 2010, 35(7): 2713–2716.
DOI:10.1016/j.ijhydene.2009.04.050 |
| [42] |
Photoelectrocatalysis hydrogen production using silicon based photoelectrodes(硅基光电极光电催化制氢)[J]. J Mol Catal (China)(分子催化), 2024, 38(1): 94–98.
DOI:10.16084/j.issn1001-3555.2024.01.011 |
| [43] |
Sulfur-deficient In2S3 photocatalyst for high-efficiency hydrogen evolution via water splitting(硫缺陷型In2S3光催化剂高效分解水制氢研究)[J]. J Mol Catal (China)(分子催化), 2024, 38(3): 215–223.
DOI:10.16084/j.issn1001-3555.2024.03.003 |
| [44] |
Research progress in photocatalytic decomposition of water using organic semiconductors containing perylene rings(含苝环有机半导体的光催化分解水研究进展)[J]. J Mol Catal (China)(分子催化), 2024, 38(1): 81–92.
DOI:10.16084/j.issn1001-3555.2024.01.010 |
| [45] |
Hybrid density functional theory description of non-metal doping in perovskite BaTiO3 for visible-light photocatalysis[J]. J Solid State Chem, 2019, 280: 121018.
DOI:10.1016/j.jssc.2019.121018 |
| [46] |
Linear optical properties in the projector-augmented wave methodology[J]. Phys Rev B, 2006, 73(4): 045112.
DOI:10.1103/PhysRevB.73.045112 |
 2025, Vol. 39
2025, Vol. 39


