2. 恩泽生物质精细化工北京市重点实验室, 北京 102617
2. Beijing Key Laboratory of Enze Biomass Fine Chemicals, Beijing, China, 102617
在当今时代, 环境保护已成为全球性的重要课题. 其中, 以水为介质来制取氢气已逐渐被醇氧化耦合制氢技术所取代. 醇氧化反应中, 阳极利用具有更低理论电压的醇氧化反应替代动力学迟缓的析氧反应, 可以在实现节约能源的同时获得高附加值的产物. 该综述全面且深入地探讨了电催化醇氧化耦合制氢领域的研究进展, 涵盖反应机理、贵金属催化剂、非贵金属催化剂以及贵金属与非贵金属复合催化剂等多方面内容. 着重论述了针对催化剂材料在纳米结构优化、电子结构调控、多组分协同效应强化等方面的改性策略, 例如运用表面化学工程、非晶态修饰及协同效应等手段提升催化剂的本征活性. 通过表面化学工程能够有效改变催化剂的电子结构, 进而调控中间体的吸附特性与吸附能, 文中详细综述了包括杂原子掺杂、空位工程、合金化、核-壳结构等一系列表面化学工程技术手段. 深入剖析了d电子轨道、空轨道、晶格参数等因素对催化剂催化性能的重大影响, 从多个维度深度阐释了催化剂微观结构的可调控方式, 为未来催化剂领域的突破指明了前进方向. 最后, 该综述还针对催化剂微观结构调控提出了前瞻性的思考方向, 如精准控制醇分子氧化的目标产物选择性、合理调控复合催化剂的导电性以及有效降低催化剂活性位点的吸附能等. 若能实现这些高效且精准的控制目标, 该技术有望突破当前醇氧化耦合制氢催化剂材料的局限, 获取高附加值的醇氧化产物, 为实现“碳达峰碳中和”时代的节能环保目标提供强有力的技术支撑与保障.
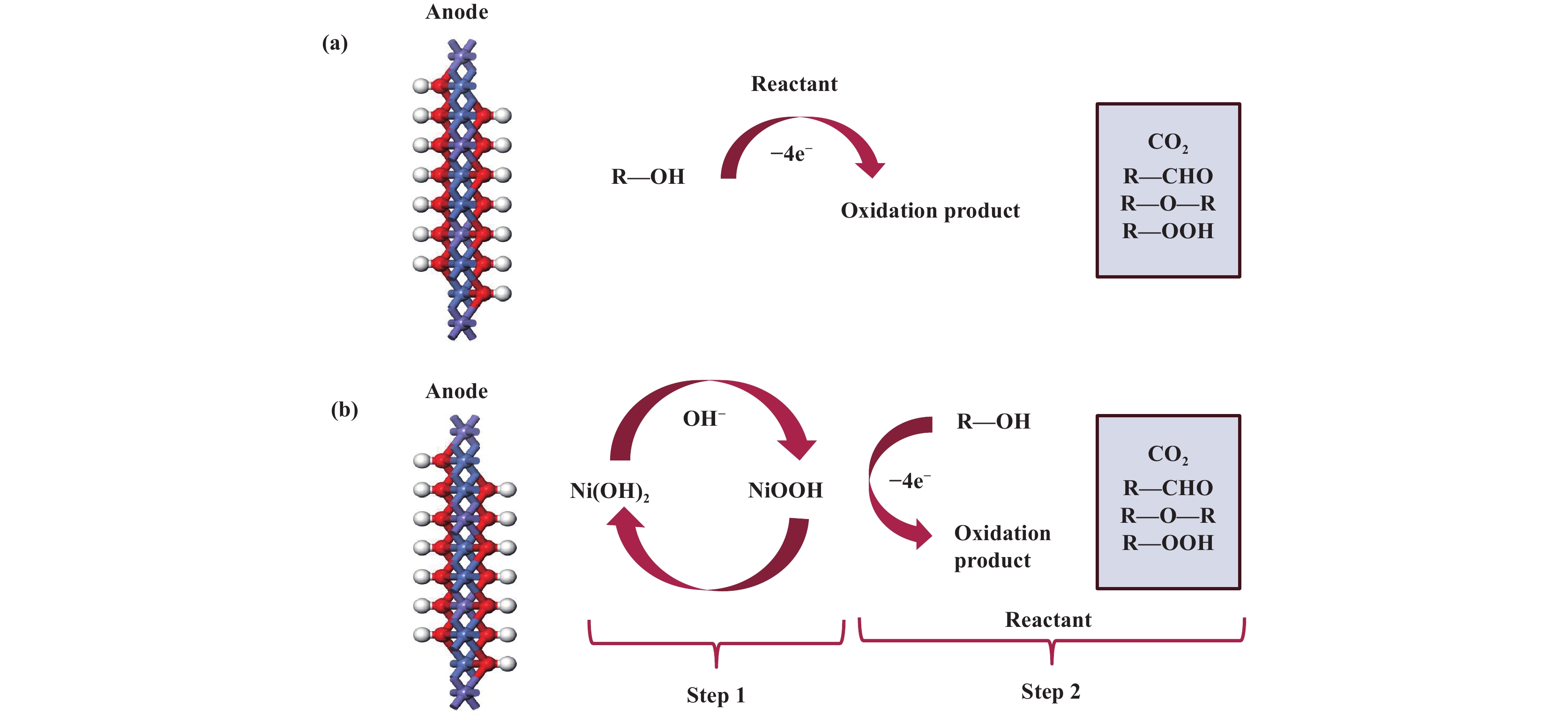
1 反应机理 1.1 直接机理醇氧化反应, 从反应途径方面分为直接氧化和间接氧化两种机理[1]; 在氧化产物方面, 当醇被完全氧化时生成CO2和H2O, 被部分氧化时生成衍生物. 在直接机理中, 醇分子直接在电极表面发生氧化反应, 电极提供的电位直接驱动醇分子失去电子并转化为氧化产物, 不涉及其他中间氧化还原介质[2−4], 见图1(a). 醇分子首先吸附到电极表面, 与电极表面的活性位点相互作用. 然后, 在电极提供的电位作用下, 醇分子中的羟基(―OH)上的氢原子被夺取, 或者醇分子中的碳氢键(C—H)被活化, 使醇分子失去氢原子和电子形成阳离子自由基中间体. 随后, 阳离子自由基中间体进一步发生反应, 经过一系列的结构重排和电子转移过程, 最终转化为相应的氧化产物. Cheng等[5]以MoO3/Ni(OH)2为催化剂进行甲醇的氧化反应[6], 反应过程中无NiOOH生成, 以Ni2+为主要的吸附离子吸附在甲醇上, Mo6+与Ni2+形成Mo-Ni复合物, 有效降低了CH2O* → CHO* + H*的反应能垒. Lu等[7]利用Co3O4催化剂将HMF(5-hydroxymethylfurfural)进行直接氧化, 验证了催化剂Co3O4对HMF的氧化反应具有高效催化的作用, 同时将Ni掺杂进尖晶石钴氧化物四面体催化剂中心, 进而提高羟基活性, 将OH−与HMF通过吸附结合进行研究得出高浓度OH−更有利于HMF的氧化.
|
图 1 电化学醇氧化(a)直接机理和(b)间接机理示意图 Fig.1 Schematic diagram of electrochemical alcohol oxidation (a) direct mechanism and (b) indirect mechanism |
间接机理是指醇的氧化反应并非由电极材料直接作用于醇分子来实现, 而是借由一种中间介质的氧化还原过程完成醇分子的氧化[8], 见图1(b). 首先, 在电极表面会发生氧化反应, 在此过程中, 电解液里的特定物质(金属离子或配合物[9])或电极材料中的过渡金属会被氧化, 进而转变为高价态的氧化还原介质. 随后, 高价态的氧化还原介质与醇分子产生化学反应, 使得醇被氧化形成对应的产物, 而此氧化还原介质自身则被还原为低价态[10]. 需要注意的是, 电化学间接醇氧化本质上是羟基氧化物或高价态离子与醇之间相互作用并生成羰基氧化物的化学反应过程, 这一过程在整个电化学体系的物质转化与能量传递中具有关键意义[11−12]. Fleischmann等[13]通过NiOOH上的电化学醇氧化的机理, 将Ni(OH)2电化学氧化成NiOOH, 用NiOOH作为电催化剂氧化醇, 该步骤将NiOOH还原为Ni(OH)2. 该反应将Ni(OH)2/NiOOH用作催化媒介, 起着运载催化底物醇的作用, 整体看本身并未参与反应. DiMeglio等[14]通过电极反应使
直接机理和间接机理的主要区别在于氧化反应的驱动力来源不同. 直接机理中, 电极材料直接驱动醇的氧化; 而间接机理中, 需要通过中间氧化还原介质来传递氧化能力, 实现醇的氧化. 这两种机理在不同的电化学醇氧化反应体系中可能会同时存在或相互竞争, 具体的反应机理取决于醇的种类、电极材料、电解液组成以及反应条件等因素.
2 电极材料 2.1 贵金属铂(Pt)电极材料在醇氧化反应中表现出优异的催化性能, 能够有效促进醇分子在其表面的吸附与脱氢过程, 降低反应活化能. Liu等[17]通过研究发现, Pt催化氧化甲醇和乙醇的氧化电流密度分别是商业用Pt/C的41.15和25.19倍. 这一显著的性能提升归因于晶格工程的改造, 通过调整Pt的晶格, 使得(100)和(111)晶面与Pd纳米颗粒相围绕, 从而增强了OH的吸附能力. 这种结构优化不仅提高了催化剂的活性, 还增强了其在反应中的稳定性.
钯(Pd)催化剂具有良好的延展性, 可通过拉长其表面粘结长度, 以此来控制d带中心的位置, 并且对OH有着强吸附作用, 减弱了CO的吸附[18]. 将Pd与其他贵金属元素结合使用可大幅度提升特定醇氧化性能. Zhou等[19]利用湿化学外延法提前制备出具有规则的fcc-2H-fcc异相Au@Pd核壳纳米棒, 该材料在碱性条件下的电催化醇氧化表现出优异的电催化性能. 这种双金属结构不仅提高了催化剂的活性, 还增强了其在复杂反应条件下的稳定性.
金(Au)催化剂凭借着其独特的阶梯状结构, 通常被用于伯醇和仲醇的氧化反应. 对于伯醇, Au催化剂可以将其氧化为相应的醛或羧酸; 对于仲醇, 能够使其氧化为酮. Wei等[20]通过比例调配合成了Au1.0/Pt0.2, 以2.3 nm的Au纳米线为模板, 形成球形的纳米颗粒, 最高可达到75%的双金属活性位点. 这种结构不仅促进了C―C分裂, 还减弱了CO的吸附, 进而提高了氢氧自由基的吸附能力, 从而提高了反应的选择性和效率.
尽管Pt、Au和Pd基催化剂在醇氧化反应中表现出卓越的性能, 但它们的高成本和资源稀缺性限制了其大规模工业化应用. 当前, 科研人员致力于通过纳米技术等手段调控贵金属的粒径、形貌与负载量, 以提高其原子利用率与催化效率. 例如, 通过原子层沉积(ALD)技术, 可以在多孔碳载体上均匀沉积Pt纳米颗粒, 从而显著提高催化剂的电化学活性表面积(ECSA)和稳定性.
2.2 非贵过渡金属贵金属电极材料在电催化醇氧化反应中成本过大, 而非贵过渡金属成本明显偏低, 是替代贵金属催化剂的经济性材料, 被广泛用作醇氧化反应的电极材料. 过渡金属常见的有铁(Fe)、镍(Ni)、钴(Co)、锰(Mn)、钼(Mo)等元素, 通过金属元素间的不同比例调配[21−22]可起到较好的催化活性作用.
钴基催化剂也在电催化醇氧化领域中研究广泛, 将钴与其他金属调配可具有表面疏松、增大颗粒间隙的作用, 也可具有协同效应作用, 催化作用显著[23]. 例如, CoMn基、CoNi基等电催化剂. Liu等[24]利用电沉积法合成CoMn二元催化剂, 该催化剂以其较小于氧化钴、氧化锰一元催化剂的粒径, 最小粒径可达到3~4 nm, 这就增大了醇分子与催化剂的接触机会, 最终为醇氧化提供了更多的接触比表面积. Medany等[25]以镍钴氧化物修饰壳聚糖电催化剂用于乙二醇氧化, 以尖晶石氧化物和壳聚糖之间的协同效应为反应机理, 其氧化电流可达到36 mA·cm−2.
近年来, 电化学领域中对镍基催化剂的使用较为广泛, 如NiFe基、NiMo基、MOF/NF基等电催化剂[26]. 这些催化剂在醇氧化反应(如甲醇、甘油等)中表现出优异的性能, 主要归因于它们独特的电子结构和表面化学性质[27]. 以下是对这些催化剂的深入分析: NiFe基电催化剂不仅具有分散性和稳定性增强作用, 还可扩大催化剂的活化面积和OH吸附位点. 镍基催化剂近两年运用最为广泛, 如Tsuji等[28]利用电沉积法合成了NiFeOx电催化剂, 该催化剂在电解过程中, Fe的氧化态从Fe(II)略微转变成Fe(III), 研究表明可能为Fe3O4和Fe2O3, 而NiO/Ni2O3部分转变为Ni(OH)2, 最终可达到过电位约0.3 V. NiMo基催化剂的协同效应可有效减小反应能垒, 提高醇氧化反应速率[29]. 在甲醇氧化反应中, Mo催化剂可弥补NiOOH在反应中的速率受限影响, 甚至有可能更好. 例如, NiMo基催化剂在电催化氢气生成反应中表现出优异的性能, 通过合理的设计和功能导向, 解决了关键的科学和技术问题.
目前在电催化醇氧化反应领域中, 已有对三元过渡金属催化剂的大量研究, 相关研究使用一定比例的三元过渡金属催化剂(如NiCoFe、NiCoMo催化剂)进行醇氧化耦合制氢反应, 其催化效果比二元过渡金属催化剂明显要好, 催化活性更高, 能有效提高醇氧化反应速率[30]. 镍基和钴基催化剂在醇氧化反应中表现出优异的催化性能, 这主要归因于它们独特的电子结构和表面化学性质. 通过晶格工程和纳米技术的优化, 这些催化剂的性能得到了进一步提升. 然而, 高昂的成本和资源稀缺性仍然是其大规模应用的主要障碍. 未来的研究将集中在进一步提高催化剂的原子利用率和催化效率, 以实现其在工业应用中的可行性.
2.3 贵/非贵过渡金属结合尽管贵金属催化剂在催化性能上表现出色, 但其高昂的成本限制了其大规模应用. 将贵金属与非贵金属结合, 不仅能够降低反应能耗, 还能提高电流密度, 有效促进活性位点的暴露. 这种结合方式通常包括掺杂和异质结构等方法[31], 见图2(a)和(b). 以下将分别对这两种方法进行深入分析.

|
图 2 (a) Pt@ZnO的异质结构合成路线[31]; (b) Pt@ZnO对氨吸附机理[31]; (c) PdCu纳米片(NSs)的合成路线[33]; (d) PdAgSn/PtBi 高熵合金(HEA)纳米颗粒(NPs)的合成路线[34] Fig.2 (a) Synthesis routes of heterostructures of Pt@ZnO[31]; (b) Mechanism of Pt-decorated ZnO sensor toward NH3[31]; (c) Synthesis routes of PdCu nanosheets (NSs)[33]; (d) Synthesis routes of PdAgSn/PtBi HEA nanoparticls (NPs)[34] |
以掺杂方式结合的贵/非贵过渡金属催化剂, 通过在贵金属中引入非贵金属元素, 调整催化剂的电子结构, 从而提高其催化性能. 例如, Yang等[32]合成了PdBi纳米链(NCs)催化剂, 在乙醇氧化反应(EOR)中, Pd的电子结构中加入Bi后, 减弱了Pd和CO的结合, 为反应提供了丰富的活性位点. 该研究表明, 纳米链结构有助于活性位点的完整暴露, 并提高了催化剂的稳定性. 以异质结构方式结合的贵/非贵过渡金属催化剂, 是近五年被应用逐渐增多的一种催化剂, 其通过不同的晶格结构或不同物质组成形成, 具有高电氧化活性和良好的耐久性, 且在双金属间表现出显著的协同作用. 例如, PdCu基催化剂通过Pd改变Cu相界面的晶体结构, 显著降低了能耗, 其催化性能优于单一贵金属. Jiang等[33]利用Pd改变了Cu相界面的晶体结构(见图2(c)), 以乙二醇为底物时, PdCu纳米片(NSs)和Pd的起始电位分别为0.54 V和0.62 V, 证明了PdCu NSs催化剂在催化能耗上的优势. 此外, Pd与Bi等过渡金属元素的结合可拓宽催化剂的活性位点, 如在甲醇和乙醇氧化反应中, 甲醇氧化电流密度可达4.94 A·mg−1, 乙醇氧化电流密度可达8.67 A·mg−1, 分别是商业用Pd/C的10.5和7.4倍[34], 见图2(d).
贵金属与非贵金属的结合在醇氧化耦合制氢反应中具有重要的应用前景. 通过异质结构和掺杂方法, 可以有效降低反应能耗, 提高电流密度, 促进活性位点的暴露[35−39]. 这些方法不仅优化了催化剂的性能, 还为贵金属催化剂低成本化提供了可能. 未来的研究将进一步探索这些结合方式的机制, 以实现更高效、更经济的催化剂设计, 推动醇氧化耦合制氢技术的工业化应用. 贵金属、非贵过渡金属、贵/非贵过渡金属三种类型催化剂的特点见表1.
| 表 1 贵金属、非贵过渡金属、贵/非贵过渡金属三种类型催化剂的特点一览表 Table 1 List of characteristics of three types of catalysts: Precious metal, non-precious transition metal, and precious/non-precious transition metal |
原位表征在反应机理研究中具有重要意义[40]. 它能实时监测反应进程, 精确捕捉反应中间体、过渡态等关键信息. 电催化醇氧化反应里, 通过原位拉曼、红外、X射线吸收精细结构谱等技术, 直观呈现分子结构变化与物种演变, 从而精准推断反应路径, 为深入理解反应本质提供有力依据.
3.1 原位拉曼拉曼光谱是一种散射光谱, 一种无损的分析技术, 它是基于光和材料内化学键的相互作用而产生的, 可以提供样品化学结构、相和形态、结晶度以及分子相互作用的详细信息. 原位拉曼光谱在电催化醇氧化研究中具有独特优势. 它能够实时监测电极材料表面分子水平的变化, 通过检测拉曼峰位移与强度变化, 揭示电极表面吸附物种、反应中间体及产物的动态演变. Sun等[41]通过原位拉曼光谱(见图3(a, b))对制备的Mn-α-Ni(OH)2/NF电极的表面Mn—O、O—O、NiIII—O三种键的位移和强度变化进行了检测, 揭示出Mn-α-Ni(OH)2/NF上阳极氧化产生的活性氧化中间体有可能成为氧化苯甲醇的关键物种. 同时, 通过分析不同电极材料在相同条件下的拉曼光谱差异, 能深入理解材料结构对反应路径及活性的影响[42]. 原位拉曼光谱在电催化醇氧化研究中提供了一种强大的工具, 能够实时监测电极材料表面的分子水平变化, 揭示反应中间体的动态演变. 然而, 该方法也面临一些挑战, 如信号强度和灵敏度、背景干扰、时间分辨率以及样品制备和稳定性等问题. 未来的研究将致力于解决这些挑战, 进一步提高原位拉曼光谱在电催化研究中的应用效果.

|
图 3 (a) Mn—O原位拉曼图谱[41]; (b) NiIII—O原位拉曼图谱[41]; (c) 乙醇酸、甘油酸、甲酸盐等分子的原位红外图谱[43]; (d)原位红外图谱分析后得出的分子结构[43] Fig.3 (a) In-situ Raman mapping of Mn—O[41]; (b) In-situ Raman mapping of NiIII—O[41]; (c) In-situ IR mapping of molecules such as glycolic acid, glyceric acid, and formate[43]; And (d) molecular structures derived from in-situ IR mapping analyses[43] |
原位红外在定性和定量鉴别分子的组成和结构中扮演着重要角色. 当以连续波长的红外光为光源照射样品, 引起分子振动能级之间跃迁, 所生的分子振动光谱, 称红外吸收光谱. 该方法在醇氧化反应中得到了广泛的运用, 可用来识别反应过程中不同峰值的产物. Du等[43]在丙三醇氧化反应中的研究中, 通过原位红外光谱(见图3(c, d))详细监测了反应过程中的产物变化. 具体步骤为: 第一步: 检测到
X射线吸收精细结构谱是一种用于研究电子的激发、跃迁与电离; 散射和干涉的一种原位表征方法. 将X射线能量调整至与所研究的元素中内电子层一致, 再用于探测样品, 然后监测吸收的X射线数量与其能量的函数关系. Zhao等[44]在研究富空穴CoSi合金的无溶剂无碱醇氧化反应中, 利用X射线吸收精细结构谱(见图4)对AM-CoSi合金的能级进行了检测. 研究发现, AM-CoSi合金中的Co元素以零价金属态形式存在. 这表明XAFS能够精确地检测到合金中元素的氧化态和电子结构, 从而为理解催化剂的活性和反应机制提供了重要信息. X射线吸收精细结构谱在醇氧化反应中提供了一种强大的工具, 能够精确检测催化剂中元素的氧化态和电子结构, 从而揭示反应机制. 然而, 该方法也面临一些挑战, 如结构和热无序的影响、活性位点的鉴别、样品要求和数据处理的复杂性. 未来的研究方向将着重于克服这些挑战, 以提升XAFS技术在材料科学研究中的应用成效. 原位拉曼、原位红外、X射线吸收精细结构谱三种表征方法的特点见表2.

|
图 4 通过XAFS光谱进行结构表征(a) AM-CoSi合金和参考样品(Co箔、Co3O4和S-CoSi)的实验Co K边缘XANES光谱和(b) 实验Co K边缘EXAFS信号的傅里叶变换幅度; (c) AM-CoSi合金的k3加权EXAFS信号的小波变换(WT); (d) AM-CoSi合金对应的EXAFS R空间拟合曲线[43] Fig.4 Structural characterization by XAFS spectroscopy: (a) Experimental Co K-edge XANES spectra and (b) Fourier-transformed magnitude of the experimental Co K-edge EXAFS signal of AM-CoSi alloy and reference samples (Co foil, Co3O4, and S-CoSi); (c) Wavelet transform (WT) for the k3-weighted EXAFS signals of AM-CoSi alloy; (d) Corresponding EXAFS R-space fitting curve of AM-CoSi alloy[43] |
| 表 2 原位拉曼、原位红外、X射线吸收精细结构谱三种表征方法特点一览表 Table 2 List of characteristics of three characterization methods: In-situ Raman, In-situ Infrared, and X-ray absorption fine structure spectroscopy |
在醇氧化反应的电催化研究中, 贵金属催化剂(如Pt、Au、Pd等)展现出优异的催化性能, 通过促进醇分子的吸附与脱氢反应显著降低反应活化能. 然而, 贵金属面临着高成本与资源稀缺限制的问题. 为克服这些问题, 研究者们正在通过纳米技术优化贵金属催化剂的粒径与形貌, 提升其原子利用率并与非贵金属催化剂复合, 力图在降低成本的同时维持甚至增强催化性能. 另一方面, 非贵金属(如镍、钴、锰等)以其低廉的成本和良好的催化特性逐渐成为贵金属催化剂的替代选择. 尤其是镍基催化剂和钴基催化剂, 在微观上对金属元素进行电子调节和几何结构改良, 可以实现较高的催化活性.
5 展望由当前的电催化醇氧化耦合制氢的研究现状来看, 该领域的电催化剂在微观上的调控还有比较大的提升潜力, 可重点从微观上进行合理调控, 如: (1) d带中心和氧空位的控制. d带中心的控制可围绕三个方面: 位置控制, 偏移角度控制, 以及偏移速度的控制. d带中心控制的同时, 也可采取氧空位的控制, 需对产生后所受到外来干扰因素的干扰程度进行控制. (2)通过晶面结构调控, 以实现表面化学工程改性. 在这一方面, 利用XRD、原位拉曼光谱、红外光谱等技术从微观结构上进行活性位点数的控制, 检测活性中心数目的多少, 以此促进比表面积扩大和醇氧化反应催化性能增大的功能. (3)贵金属和非贵过渡金属的微观调控. 以过渡金属元素为主, 贵金属元素为辅, 设计出新型贵金属与非贵金属相结合的电催化剂, 从新的领域上去探索醇氧化耦合制氢反应的催化剂性能.
最后, 电催化醇氧化耦合制氢是燃料电池的重要技术, 可实现氢能的产出和高附加值化学品的合成, 有着比电解水制氢更低能耗的优势, 可实现节能, 且该技术反应条件较温和, 对环境友好. 未来该技术有望进一步扩大应用, 更大限度地推进燃料电池的可持续发展.
| [1] |
Direct electrochemical oxidation of alcohols with hydrogen evolution in continuous-flow reactor[J]. Nat Commun, 2019, 10: 2796.
DOI:10.1038/s41467-019-10928-0 |
| [2] |
Oxidation of alcohol[J]. Nature, 1957, 179(4551): 142–143.
DOI:10.1038/179142a0 |
| [3] |
Highly efficient, organocatalytic aerobic alcohol oxidation[J]. J Am Chem Soc, 2011, 133(17): 6497–6500.
DOI:10.1021/ja110940c |
| [4] |
Mechanism of alcohol oxidation mediated by copper(II) and nitroxyl radicals[J]. J Am Chem Soc, 2014, 136(34): 12166–12173.
DOI:10.1021/ja5070137 |
| [5] |
Direct electrocatalytic methanol oxidation on MoO3/Ni(OH)2: Exploiting synergetic effect of adjacent Mo and Ni[J]. J Am Chem Soc, 2023, 145(49): 26858–26862.
DOI:10.1021/jacs.3c09399 |
| [6] |
Understanding the oxidative properties of nickel oxyhydroxide in alcohol oxidation reactions[J]. ACS Catal, 2023, 13(13): 8467–8476.
DOI:10.1021/acscatal.3c01120 |
| [7] |
Integrated catalytic sites for highly efficient electrochemical oxidation of the aldehyde and hydroxyl groups in 5-hydroxymethylfurfural[J]. ACS Catal, 2022, 12(7): 4242–4251.
DOI:10.1021/acscatal.2c00174 |
| [8] |
Predictive control of selective secondary alcohol oxidation of glycerol on NiOOH[J]. Nat Commun, 2022, 13(1): 5848.
DOI:10.1038/s41467-022-33637-7 |
| [9] |
Metal/oxide inter-facial effects on the selective oxidation of primary alcohols[J]. Nat Commun, 2017, 8: 14039.
DOI:10.1038/ncomms14039 |
| [10] |
Alcohols electrooxidation coupled with H2 production at high current densities promoted by a cooperative catalyst[J]. Nat Commun, 2022, 13(1): 147.
DOI:10.1038/s41467-021-27806-3 |
| [11] |
Performance evolution of ethanol carbonylation on Ni/Activated carbon catalyst(Ni/活性炭催化剂上乙醇羰基化性能演变研究)[J]. J Mol Catal (China)(分子催化), 2024, 38(6): 530–540.
DOI:10.16084/j.issn1001-3555.2024.06.004 |
| [12] |
Water oxidation intermediates applied to catalysis: Benzyl alcohol oxidation[J]. J Am Chem Soc, 2012, 134(9): 3972–3975.
DOI:10.1021/ja210718u |
| [13] |
The oxidation of organic compounds at a nickel anode in alkaline solution[J]. J Electroanal Chem Interfacial Electrochem, 1971, 31(1): 39–49.
DOI:10.1016/S0022-0728(71)80040-2 |
| [14] |
Base-assisted nitrate mediation as the mechanism of electrochemical benzyl alcohol oxidation[J]. J Phys Chem C, 2021, 125(15): 8148–8154.
DOI:10.1021/acs.jpcc.0c10476 |
| [15] |
Selective chloride-mediated neat ethanol oxidation to 1,1-diethoxyethane via an electrochemically generated ethyl hypochlorite intermediate[J]. J Am Chem Soc, 2021, 143(39): 15907–15911.
DOI:10.1021/jacs.1c05976 |
| [16] |
Insights into active sites and mechanisms of benzyl alcohol oxidation on nickel-iron oxyhydroxide electrodes[J]. ACS Catal, 2023, 13(7): 4272–4282.
DOI:10.1021/acscatal.2c05656 |
| [17] |
Hydrogen-intercalation-induced lattice expansion of Pd@Pt core-shell nanoparticles for highly efficient electrocatalytic alcohol oxidation[J]. J Am Chem Soc, 2021, 143(29): 11262–11270.
DOI:10.1021/jacs.1c05856 |
| [18] |
Atomically reconstructed palladium metallene by intercalation-induced lattice expansion and amorphization for highly efficient electrocatalysis[J]. ACS Nano, 2022, 16(9): 13715–13727.
DOI:10.1021/acsnano.2c05190 |
| [19] |
Preparation of Au@Pd core-shell nanorods with fcc-2H-fcc heterophase for highly efficient electrocatalytic alcohol oxidation[J]. J Am Chem Soc, 2022, 144(1): 547–555.
DOI:10.1021/jacs.1c11313 |
| [20] |
Au/Pt bimetallic nanowires with stepped Pt sites for enhanced C–C cleavage in C2+ alcohol electro-oxidation reactions[J]. J Am Chem Soc, 2023, 145(34): 19076–19085.
DOI:10.1021/jacs.3c07027 |
| [21] |
Electrocatalytic oxidation of primary alcohols at the triple-phase boundary in an anion-exchange membrane reactor with nickel, cobalt, and iron catalysts[J]. ACS Catal, 2024, 14(11): 8922–8929.
DOI:10.1021/acscatal.4c01097 |
| [22] |
Coprecipitation preparation of copper-cobalt based catalysts for higher alcohol production[J]. Cambridge Sci Adv, 2024, 2: 32–35.
DOI:10.62852/csa/2024/13 |
| [23] |
Biomass carbon anchored Co-N4 single-atom catalyst for efficient hydrogen evolution, oxygen evolution and alcohol oxidation reaction[J]. ChemistrySelect, 2024, 9(9): e202303637.
DOI:10.1002/slct.202303637 |
| [24] |
Electrodeposition preparation and NO catalytic capacity of Co/Mn-based monolithic catalysts(钴锰整体式催化剂的电沉积法制备及NO催化氧化性能)[J]. Chem Ind Eng Prog(化工进展), 2019, 38(10): 4588–4594.
DOI:10.16085/j.issn.1000-6613.2019-0090 |
| [25] |
Nickel-cobalt oxides decorated Chitosan electrocatalyst for ethylene glycol oxidation[J]. Surf Interfaces, 2023, 40: 103077.
DOI:10.1016/j.surfin.2023.103077 |
| [26] |
Open active sites in Ni-based MOF with high oxidation states for electrooxidation of benzyl alcohol[J]. Inorg Chem, 2024, 63(27): 12572–12581.
DOI:10.1021/acs.inorgchem.4c01507 |
| [27] |
Porous cobalt-nickel binary oxide nanosheets for electrochemical glycerol oxidation[J]. ACS Appl Energy Mater, 2024, 7(24): 11787–11798.
DOI:10.1021/acsaem.4c01995 |
| [28] |
Effect of the substrate materials in the fabrication of an electrode based on mixed nickel-iron oxide electrocatalyst[J]. Adv Sustainable Syst, 2024, 8(7): 2300475.
DOI:10.1002/adsu.202300475 |
| [29] |
Catalytic activity enhancement on alcohol dehydrogenation via directing reaction pathways from single- to double-atom catalysis[J]. J Am Chem Soc, 2022, 144(11): 4913–4924.
DOI:10.1021/jacs.1c12705 |
| [30] |
Ternary Ni-Co-Se nanostructure for electrocatalytic oxidative value addition of biomass platform chemicals[J]. ACS Appl Energy Mater, 2023, 6(10): 5331–5341.
DOI:10.1021/acsaem.3c00313 |
| [31] |
Advances in noble metal-decorated metal oxide nanomaterials for chemiresistive gas sensors: Overview[J]. Nano-Micro Lett, 2023, 15(1): 89.
DOI:10.1007/s40820-023-01047-z |
| [32] |
Rational design of PdBi nanochains with grain boundaries for enhanced ethanol oxidation reaction[J]. Int J Hydrogen Energy, 2022, 47(33): 14859–14868.
DOI:10.1016/j.ijhydene.2022.02.235 |
| [33] |
Cu2+-regulated one-pot wet-chemical synthesis of uniform PdCu nanostars for electrocatalytic oxidation of ethylene glycol and glycerol[J]. J Colloid Interface Sci, 2023, 649: 118–124.
DOI:10.1016/j.jcis.2023.06.044 |
| [34] |
Pd-enriched-core/Pt-enriched-shell high-entropy alloys with face-centred cubic structure for C1 and C2 alcohol oxidation[J]. Angew Chem Int Edit, 2023, 62(31): e202304510.
DOI:10.1002/anie.202304510 |
| [35] |
Covalent organic frameworks supported noble-metal Pt for electrocatalytic hydrogen evolution(共价有机框架负载贵金属铂用于电催化析氢)[J]. J Mol Catal (China)(分子催化), 2024, 38(1): 42–50.
DOI:10.16084/j.issn1001-3555.2024.01.006 |
| [36] |
Photoelectrocatalysis hydrogen production using silicon based photoelectrodes(硅基光电极光电催化制氢)[J]. J Mol Catal (China)(分子催化), 2024, 38(1): 94–98.
DOI:10.16084/j.issn1001-3555.2024.01.011 |
| [37] |
Silver-doped γ-MnO2 for oxygen evolution reaction in acidic media(Ag掺杂γ-MnO2酸性电催化析氧反应研究)[J]. J Mol Catal (China)(分子催化), 2024, 38(3): 224–233.
DOI:10.16084/j.issn1001-3555.2024.03.004 |
| [38] |
N-doped FeNi cocatalysts for enhancing the OER activity in Fe2O3 photoanodes(N掺杂FeNi催化剂提升Fe2O3光阳极析氧活性)[J]. J Mol Catal (China)(分子催化), 2024, 38(6): 521–529.
DOI:10.16084/j.issn1001-3555.2024.06.003 |
| [39] |
NiFeOOH nanosheets self-supported on the NiFe alloy foam for oxygen evolution reaction(泡沫镍铁合金自支撑NiFeOOH纳米片的制备及析氧性能研究)[J]. J Mol Catal (China)(分子催化), 2023, 37(6): 528–534.
DOI:10.16084/j.issn1001-3555.2023.06.002 |
| [40] |
Spectroscopic study of surface dynamics of Al2O3 supported Pt-catalysts(Al2O3负载 Pt基催化剂表面动态变化的谱学研究)[J]. J Mol Catal (China)(分子催化), 2024, 38(1): 7–16.
DOI:10.16084/j.issn1001-3555.2024.01.002 |
| [41] |
Highly selective electrocatalytic oxidation of amines to nitriles assisted by water oxidation on metal-doped α-Ni(OH)2[J]. J Am Chem Soc, 2022, 144(33): 15185–15192.
DOI:10.1021/jacs.2c05403 |
| [42] |
Mechanistic investigation of enhanced catalytic selectivity toward alcohol oxidation with Ce oxysulfate clusters[J]. J Am Chem Soc, 2022, 144(27): 12092–12101.
DOI:10.1021/jacs.2c02625 |
| [43] |
Copper nanoparticles dotted on copper sulfide nanosheets for selective electrocatalytic oxidation of glycerol to formate[J]. ACS Appl Nano Mater, 2022, 5(8): 10174–10182.
DOI:10.1021/acsanm.2c00323 |
| [44] |
Facile synthesis of CoSi alloy catalysts with rich vacancies for base- and solvent-free aerobic oxidation of aromatic alcohols[J]. Chin J Catal, 2023, 48: 175–184.
DOI:10.1016/S1872-2067(23)64418-3 |
 2025, Vol. 39
2025, Vol. 39


