传统化石能源短缺, 开发可再生生物质能源对构建可持续能源体系具有重要意义[1]. 生物质基能源中呋喃家族燃料, 例如: 2-甲基呋喃(2-MF)和2,5-二甲基呋喃(DMF)来源广泛、成本低, 被视为有前景的第二代生物燃料[2]. 近年来, 2-甲基四氢呋喃(2-MTHF)凭借其卓越的燃烧性能(高热值、强稳定性及高能量密度)成为新型生物质燃料, 受到广泛的关注. 2-MTHF能提升汽油的辛烷值和燃烧效率, 且与发动机系统适配性良好、不损伤发动机, 是极具潜力的燃料添加剂[3]. 此外, 2-MTHF溶解性好、毒性低、沸点高, 是环境友好型溶剂, 在醚化、氢化、酯化等反应中广泛应用[4]. 目前, 2-MTHF的工业化生产有以贵金属钯和铂为代表的催化剂, 虽然活性和选择性较高, 但其成本高且易失活, 导致2-MTHF价格居高不下. 研发价廉易得的非贵金属催化剂用于生物质催化转化为2-MTHF, 极具吸引力.
2-甲基-1,4丁二醇、内酯、乙酰丙酸等都可以作为生产2-MTHF的原料, 但它们存在原料成本高、反应条件苛刻或者催化成本高等问题, 难以实现大规模工业生产[5−8]. 生物基糠醛及其下游产物2-MF, 来源广泛、成本低, 以其为原料合成2-MTHF是符合绿色化学概念的理想工艺路线, 成为当前化工领域的研究热点[9]. Chang X等[10]以Cu-Pd双金属为催化剂, 以2-丙醇作为氢供体, 催化糠醛选择性加氢获得了2-MTHF. Fang等[11]设计了双床层催化系统(Cu/SiO2-Pd/SiO2), 实现糠醛一步转化为2-MTHF, 在常压下2-MTHF收率突破97%. Liu 等[12]采用两步装填法, 以Co/Al2O3和Ni/Al2O3为催化剂, 实现糠醛一锅转化为2-MTHF, 糠醛在Co基催化剂上转化为2-MF, 然后2-MF在Ni基催化剂的作用下进一步转化为2-MTHF, 其收率达到87%. 糠醛衍生的2-MF, 呋喃环中C=C进行选择性加氢就可以获得产物2-MTHF. 林涛等[13]以Pd/C、Pt/C和Ru/C等贵金属为催化剂, 在气相条件下, 将2-MF转化为2-MTHF, 收率达99.9%, 但催化成本高, 工业化存在很大挑战. 研究表明, Ni基催化剂对C=C加氢反应存在优异的选择性, 非贵金属Ni储量丰富、成本低, 开发Ni基催化剂能降低生产成本[14]. Ni基催化剂的空间结构与催化性能可以通过制备方法进行有效调控, 常用的有溶胶-凝胶、蒸氨、浸渍及共沉淀法. Xia等[15]发现溶胶凝胶法制备的Ni/SiO2, 相较于浸渍法制备的Ni基催化剂, Ni粒径小且分布也较为均匀. 丁茯等[16]采用凝胶-溶胶法制备了不同Ni负载量的Ni/SiO2催化剂, 研究其对2-MF加氢性能的影响, 结果表明, 在合适的反应条件下25%的Ni负载量可以使2-MF的转化率达到98%, 2-MTHF的选择性可以达到86%, 但催化剂稳定性较差, 10 h就发生了失活. 王英文等[8]通过蒸氨法制备了Ni/SiO2催化剂, 2-MTHF的收率达到了93.5%. 李增杰等[17]通过浸渍法制备了Ni/Al2O3催化剂, 用于2-MF液相加氢, 在3 MPa、150 ℃的温和条件下实现了2-MF的高效转化, 2-MTHF的收率达到了96.5%. 方姿予等[18]以浸渍法制备了Ni/Al2O3催化剂, 应用于2-MF气相反加氢反应, 在更加温和的条件下得到了更高的2-MTHF收率, 2-MTHF的收率达到了97%, 但是催化剂的稳定性仍有欠缺, 在运行40 h之后, 催化剂因Ni聚集和碳沉积发生了失活. 蒸氨法和溶胶-凝胶法制备的Ni催化剂活性高, 但对2-MTHF的选择低, 浸渍法制备的催化剂稳定性较差. 有研究表明, 共沉淀法可以通过改变沉淀剂种类、溶液pH以及沉淀温度等制备参数改变催化剂的空间结构和催化性能, 调控催化剂活性组分分散性以及金属载体间的相互作用, 从而提高催化剂的稳定性[19]. Wang等[20]通过共沉淀法制备了Ni/Al2O3催化剂, 用于乙醇重整制氢反应, 相比于浸渍法制备的催化剂, 游离Ni颗粒较少、金属-载体相互作用更强, 表现出了更高的活性和稳定性. Wang等[21]以碳黑为模板, 通过共沉淀法制备了高比表面积的Ni/MgAl2O4催化剂, 其在CO甲烷化反应中表现出较高的活性和稳定性、显著的抗烧结性和抗积碳能力.
本文采用共沉淀法制备Ni/Al2O3催化剂, 研究了Ni含量对催化剂结构及2-MF气相加氢性能的影响, 考察了反应温度和压力对催化性能的影响规律. 结果表明, 10%Ni/Al2O3催化剂在90 ℃、2 MPa、n(H2/2-MF)=6.4、WHSV=2.7 h−1的反应条件下, 2-MF转化率接近100%, 2-MTHF选择性达到了98.6%, 催化剂稳定运行140 h性能保持不变, 具有良好的工业应用前景.
1 实验部分 1.1 实验试剂及催化剂的制备硝酸镍(Ni(NO3)2·6H2O, 99%, AR), 硝酸铝(Al(NO3)3·9H2O, 99%, AR), 碳酸钠(Na2CO3, 99%, AR), 均购自国药控股化学试剂有限公司. Ni/Al2O3催化剂制备方法(以15%Ni/Al2O3为例): 称取5.84 g Ni(NO3)2·6H2O, 31.27 g Al(NO3)3·9H2O加入100 mL去离子水中搅拌、溶解后记为溶液S1. 称取29.15 g Na2CO3加入500 mL去离子水中, 搅拌配置成溶液, 记为溶液S2. 沉淀剂Na2CO3 对金属离子的摩尔比保持在1.1∶1. 在烧杯中加入少量的去离子水, 放入40 ℃水浴锅中, 将溶液S1、S2并流加入到烧杯中搅拌, 控制沉淀溶液pH值始终保持在7左右. 待完全沉淀后, 在40 ℃下搅拌, 老化4 h, 过滤、洗涤至滤液电导率<100 μs·cm−1, 120 ℃干燥12 h, 450 ℃焙烧4 h制得Ni/Al2O3催化剂. 催化剂记作x%Ni/Al2O3(x%代表不同的Ni含量).
1.2 催化剂的表征通过Autosorb-i Q-C型全自动物理化学吸附仪(美国康塔公司)测试样品的比表面积及孔结构, 测试前样品在真空条件下进行预处理(80、120 ℃处理 30 min, 300 ℃ 处理 3 h), 在液氮条件下进行等温吸附脱附; D8 Advance型X射线多晶衍射分析仪测试催化剂的物相结构, 测试条件: Cu Kα射线 (λ=
在固定床连续反应器中, 进行催化剂活性评价. 反应管长度为380 mm, 内径8 mm. 焙烧后的催化剂经破碎、筛分得到0.425~0.850 mm颗粒, 取1 g催化剂置于反应管中心的催化剂托盘中, 并在催化剂上方覆盖4 g石英砂. 在反应前, 通入25% H2/N2(体积比)混合气, 在600 ℃下还原4 h. 还原后, 反应器温度调至所需反应温度, 并通入氢气(流量为80 mL·min−1); 2-MF经高压泵连续注入反应器. 反应后的气相产物依次通过冷凝器、分离器, 最终在分离器出口收集液态产物, 采用气相色谱分析产物组成. 取样间隔为1 h. 反应产物通过气相色谱仪(GC9790Ⅱ, 浙江福立分析仪器有限公司)进行定性和定量分析. 色谱柱为二甲基聚硅氧烷色谱柱(KB-1, 30 m×0.32 mm×0.50 μm), 进样口温度设定为180 ℃, 检测器温度为250 ℃, 色谱柱初始温度为50 ℃, 保持6 min, 然后以10 ℃·min−1的升温速率升至250 ℃. 2-MF的转化率及产物2-MTHF的选择性通过以下公式进行计算:
| $ {X}_{2\text-\mathrm{M}\mathrm{F}}=\frac{{n}_{2\text-\mathrm{M}\mathrm{F},\mathrm{ }\mathrm{i}\mathrm{n}}-{n}_{2\text-\mathrm{M}\mathrm{F},\mathrm{ }\mathrm{o}\mathrm{u}\mathrm{t}}}{{n}_{2\text-\mathrm{M}\mathrm{F},\mathrm{ }\mathrm{i}\mathrm{n}}}\times 100\text{%} $ | (1) |
| $ {S}_{2\text-\mathrm{M}\mathrm{T}\mathrm{H}\mathrm{F}}=\frac{{n}_{2\text-\mathrm{M}\mathrm{T}\mathrm{H}\mathrm{F}}}{{n}_{2\text-\mathrm{M}\mathrm{F},\mathrm{ }\mathrm{i}\mathrm{n}}-{n}_{2\text-\mathrm{M}\mathrm{F},\mathrm{ }\mathrm{o}\mathrm{u}\mathrm{t}}}\times 100\text{%} $ | (2) |
式中: n2-MF,in为反应前2-MF的摩尔数, n2-MF,out为反应后2-MF的摩尔数, n2-MTHF为产物中2-MTHF的摩尔数.
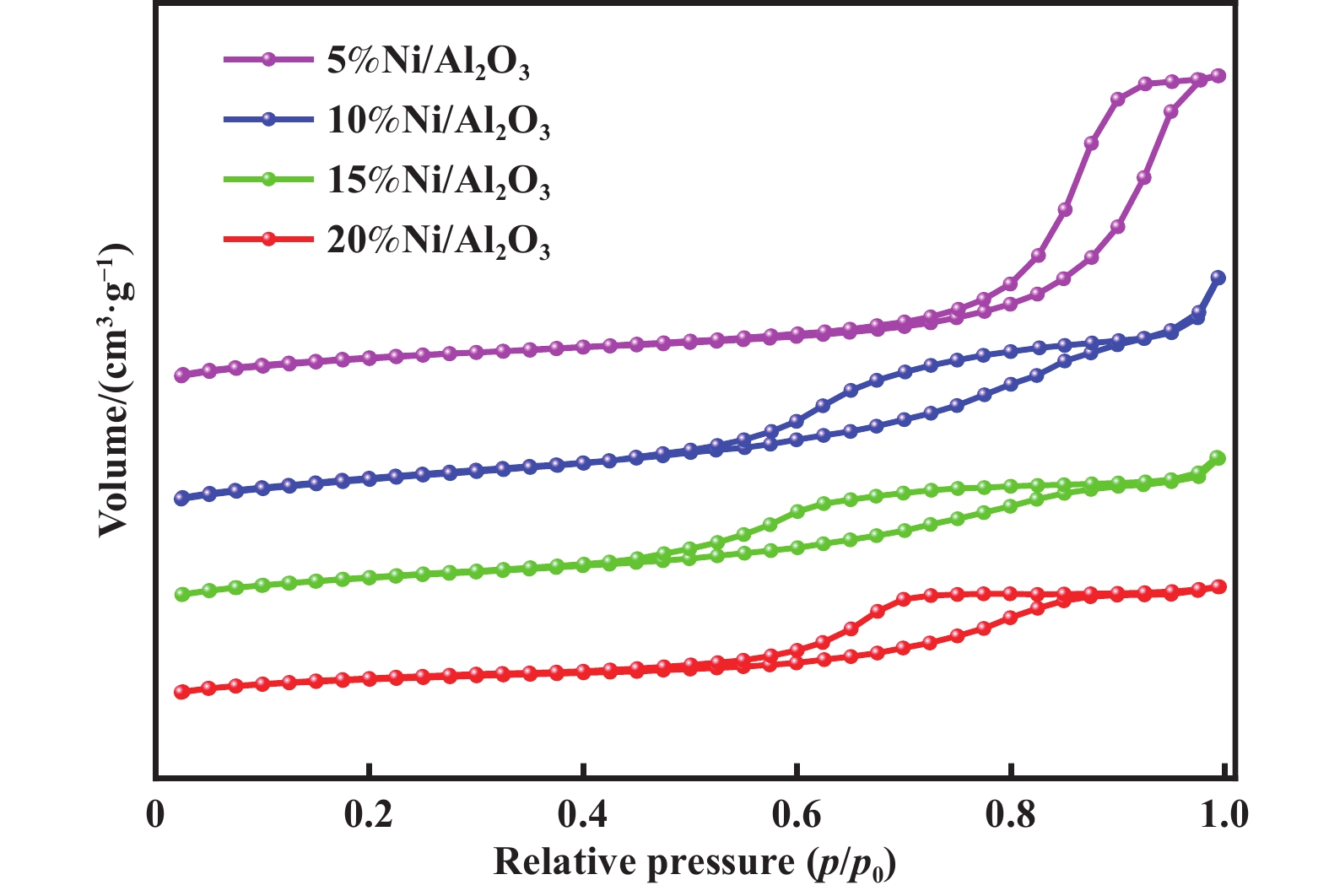
2 结果与讨论 2.1 催化剂的比表面积及孔结构图1为Ni/Al2O3催化剂的N2吸附-脱附等温线. 依据等温线数据, 采用BET模型计算比表面积, 采用BJH法计算孔结构参数, 结果见表1. 根据IUPAC分类, 一系列Ni/Al2O3催化剂的等温线均表现出Ⅳ型等温线特征, 带有H1型迟滞环, 表明催化剂具有介孔结构, 孔形状为均匀的圆柱形孔[22]. 随着催化剂中Ni含量的变化, 等温线上迟滞环的位置发生了变化. 5%Ni/Al2O3催化剂的迟滞环相对压力p/p0在0.9~1.0, 表明其介孔孔径比较大. 当Ni含量增大(10%, 15%, 20%)时, 迟滞环出现在相对压力p/p0较低的位置(0.6~0.8), 表明介孔的孔径变小. 另外, 随着Ni含量的增加, 催化剂的比表面积显著下降, 20%Ni/Al2O3催化剂比表面积相比于5%Ni/Al2O3催化剂下降了21.7%. 催化剂的孔容减少了约50%, 这可能是由于活性组分在催化剂孔道中的聚集所导致, 负载量越大, 聚集得越多, 所以孔径降低. 较大的比表面积能够促进活性组分Ni在载体上分散, 提高催化剂的活性. 介孔孔道尺寸和均匀的圆柱形孔有利于反应物和产物分子有效扩散, 减少副产物的生成, 从而提升2-MTHF的催化选择性[23].
|
图 1 催化剂N2吸附-脱附等温线 Fig.1 N2 adsorption-desorption isotherms of catalysts |
| 表 1 催化剂的比表面积、孔容和平均孔径 Table 1 The specific surface area, pore volume, and average pore size of the catalysts |
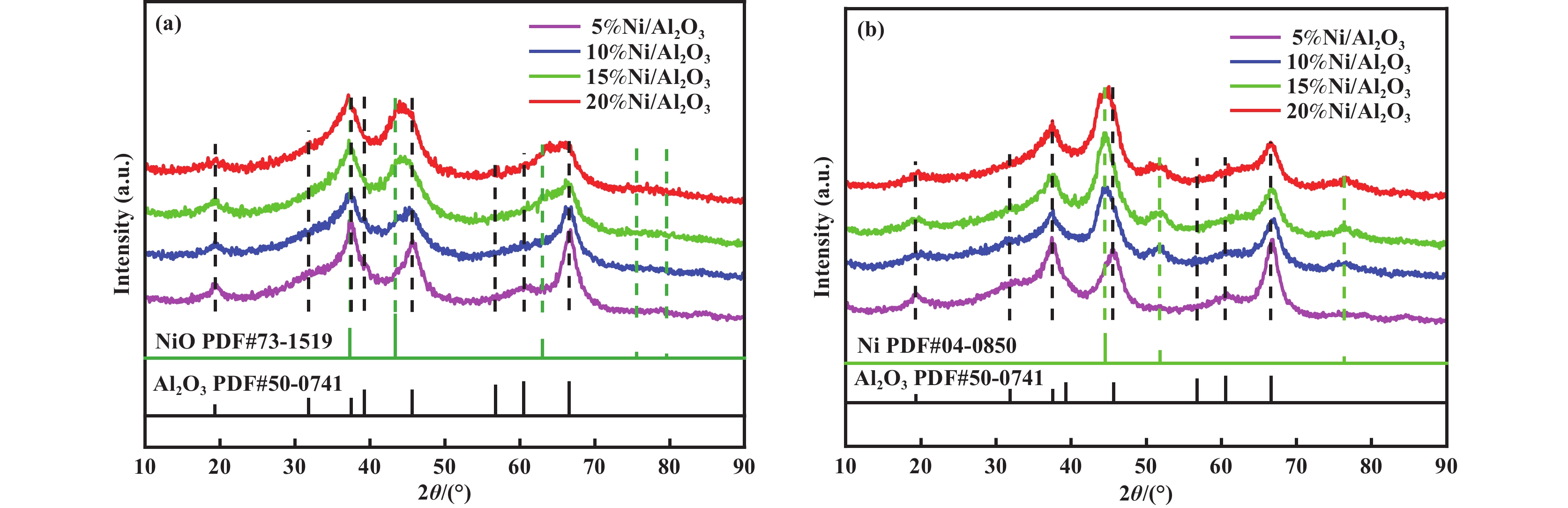
焙烧和还原后催化剂的XRD图谱见图2. 焙烧后催化剂均为γ-Al2O3负载的NiO, 物相包括Al2O3和NiO. 在图2(a) 中, 衍射角2θ=19.3°、31.9°、37.5°、39.3°、45.7°、56.7°、60.5°、66.6°处, 观察到与γ-Al2O3 (PDF#50-0741)不同晶面对应的衍射峰相匹配. 在2θ=37.3°、43.4°、63.2°、75.6°、79.6°处出现的衍射峰则归属于NiO (PDF#73-1519). 随着催化剂中Ni含量的增加, NiO的衍射峰强度逐渐由宽泛变得尖锐, 说明NiO结晶度增强. 在图2(b)中, 2θ=44.5°、51.8°、76.4°处观察到的衍射峰分别对应于Ni (PDF#04-0850)的(111)、(200)、(220)晶面, 表明催化剂经过600 ℃高温氢氮混合气还原处理后, 催化剂中的NiO组分被还原为金属Ni. 值得注意的是, 经过还原处理后催化剂的XRD谱图中仍然存在NiO的衍射峰, 表明催化剂中的NiO并未完全还原为金属Ni[24]. 对于还原后的5%Ni/Al2O3催化剂, 在2θ=44.5°、51.8°处并未明显观察到Ni的衍射峰, 可能是金属Ni数量少且高度分散于载体表面. Li 等[25]发现在450 ℃下焙烧Ni/γ-Al2O3会产生NiAl2O4相. NiAl2O4相的衍射峰位置几乎和γ-Al2O3相同, 很难从XRD衍射峰位置判断是否存在NiAl2O4相, 但主要衍射峰的相对强度可以用来区别这两个相[26]. γ-Al2O3 (PDF#50-0741)和NiAl2O4 (PDF#73-0239)在37.5°和44.5°的衍射峰强度比分别为0.65和1.94, 催化剂中这两个衍射峰强度在1.12~1.20之间, 比γ-Al2O3的比值高, 表明存在NiAl2O4相[27].
|
图 2 催化剂(a)焙烧后和(b)还原后XRD谱图 Fig.2 XRD spectra of the catalysts after (a) calcination and (b) reduction |
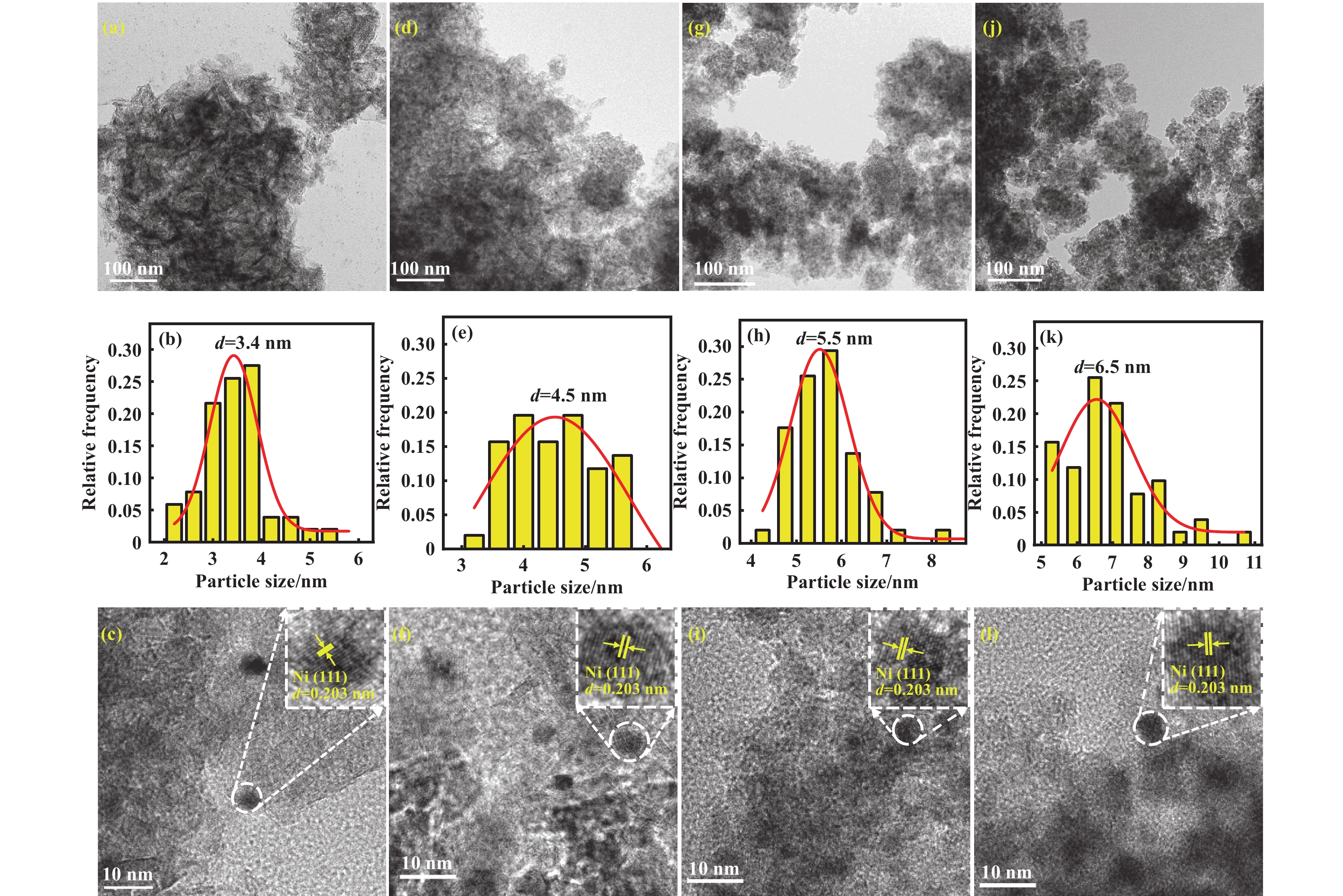
还原后催化剂的透射电镜(TEM)图像、Ni粒径尺寸分布如图3所示. 结果表明, 催化剂在600 ℃以25%的H2/N2混合气还原处理4 h后, 不同Ni含量的Ni/Al2O3催化剂上金属Ni颗粒分布均匀, 未见显著聚集现象. 颗粒尺寸分布图显示(图3(b, e, h, k)), Ni颗粒会随着Ni含量的升高而逐渐增大, 催化剂5%Ni/Al2O3、10%Ni/Al2O3、15%Ni/Al2O3和20%Ni/Al2O3的Ni颗粒平均粒径分别为3.4、4.5、5.5和6.5 nm. Bukhari等[28]发现Ni/F-SBA-15中, 随着Ni负载量的增大, 催化剂中Ni颗粒会形成较大团簇, 导致Ni粒径增大. Ni颗粒的粒径在很大程度上决定了催化剂的活性, 是影响催化剂性能的关键因素之一. 催化剂的比表面积与金属粒径的分布密切相关, 高比表面积的载体能够为活性金属组分提供更大的负载空间, 从而提高活性组分的分散度, 分散度越好, Ni的粒径也会越小[29]. 此外, 当Ni含量为5%时, 可以观察到较多层状结构的氧化铝, 见图3(a). 当Ni负载量达到10%, 氧化铝的形貌发生变化, 层状结构开始变少, 见图3(d). 当Ni负载量达到15%、20%时, 几乎已经观察不到层状结构的氧化铝(如图3(g, j)). 层状氧化铝载体结构能与Ni组分之间形成较强的金属-载体相互作用, 这种相互作用能够显著提升催化剂的活性和稳定性[30]. HRTEM图像中(图3(c, f, i, l))观察到的晶格条纹间距为0.203 nm, 与Ni (111)晶面间距一致(fcc, PDF#04-0850), 证实了NiO已经被还原为Ni.
|
图 3 还原后催化剂的TEM图像和粒径分布统计图 Fig.3 TEM images of catalysts after reduction and size distribution (a, b, c) 5%Ni/Al2O3; (d, e, f) 10%Ni/Al2O3; (g, h, i) 15%Ni/Al2O3; (j, k, l) 20%Ni/Al2O3 |
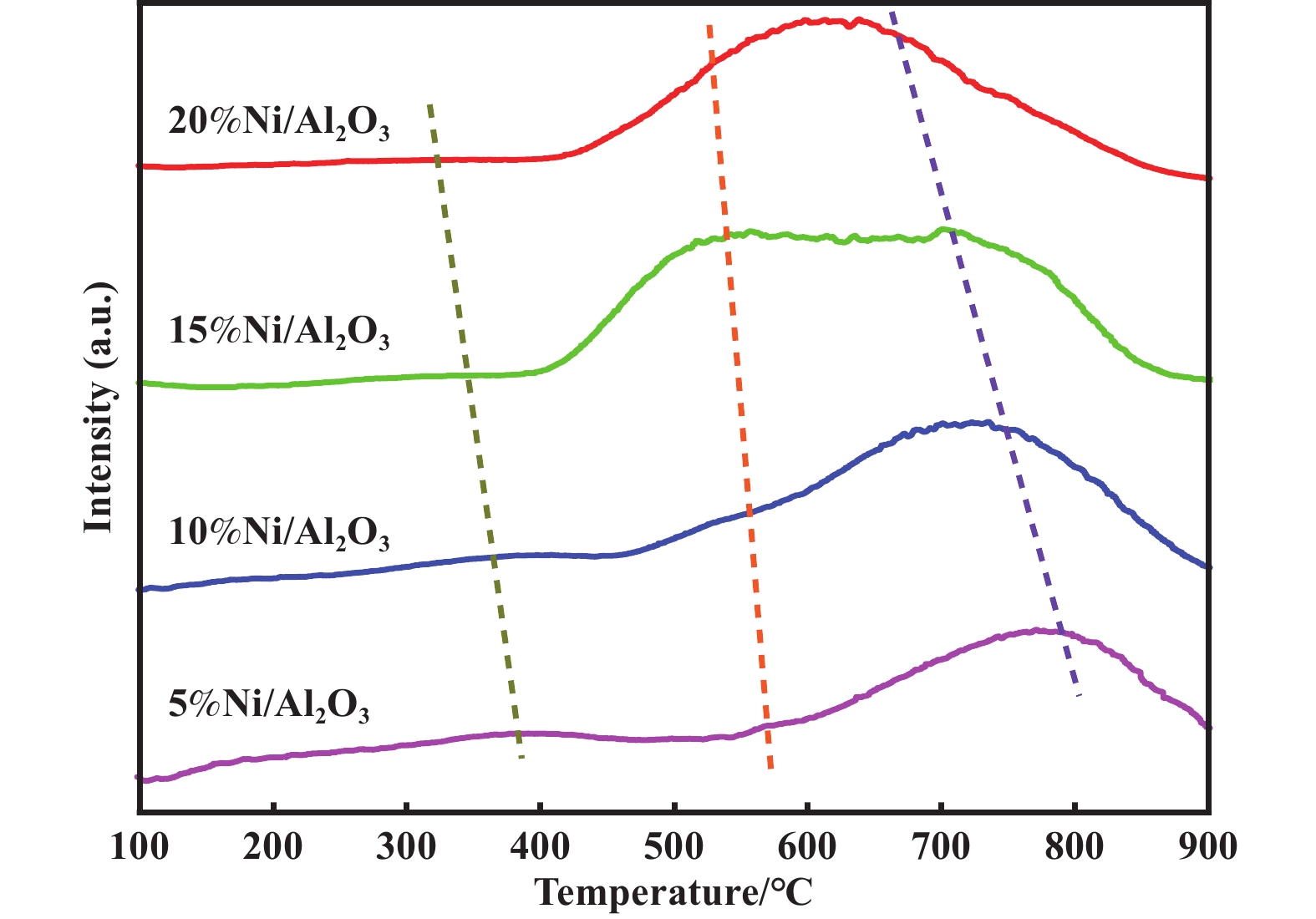
Ni/Al2O3催化剂的H2-TPR结果如图4所示. H2-TPR结果反映了催化剂在氢气气氛下的还原温度和氢气消耗情况, 还原温度高低反映了催化剂金属-载体相互作用强度的差异. H2-TPR曲线上出现了三个不同的还原峰, 对应着三种Ni物种的还原. 400 ℃以下的还原峰归属于Al2O3表面游离态NiO的还原, 因其与氧化铝载体之间的金属-载体相互作用较弱, 最易还原; 500~600 ℃范围内的还原峰则对应于与Al2O3载体具有较强相互作用的NiO组分的还原; 而700 ℃以上出现的还原峰可能和Ni与Al2O3形成的部分NiAl2O4的还原过程有关. 随着NiO含量的增加, 还原温度逐渐向低温方向移动. 5%Ni/Al2O3、10%Ni/Al2O3催化剂在600~800 ℃之间的高温还原峰较为明显, 表明NiO颗粒与Al2O3载体之间的金属-载体相互作用比较强, 还原需要克服较高的能垒. 随着NiO的负载量进一步增大到15%Ni/Al2O3, 主还原峰温度开始向低温移动, 并逐渐宽化. 当负载量达到20%时, 催化剂的主还原峰温度在650 ℃左右. 可能是因为催化剂中NiO粒径增大, 体积效应促进了金属-载体相互作用相对较弱的NiO形成, 降低了还原能垒和所需的还原温度[31]. 一般来说, 随着催化剂负载量的增大, 需要更高的还原温度来处理更多的活性金属用于反应. 本研究中呈现出了低Ni含量高还原温度的反常规律, 可能是因为低Ni含量下Al2O3呈现出的层状载体结构以及较小的体积效应使载体与金属Ni之间的相互作用变强导致的. 这也说明了在选择性加氢的反应中提高催化活性, 不能仅追求高的活性金属Ni含量, 更需要充分考虑活性组分的体积效应和金属-载体相互作用之间的竞争关系, 两者的动态平衡机制直接影响了催化剂的反应活性.
|
图 4 催化剂H2-TPR图 Fig.4 H2-TPR profiles of catalysts |
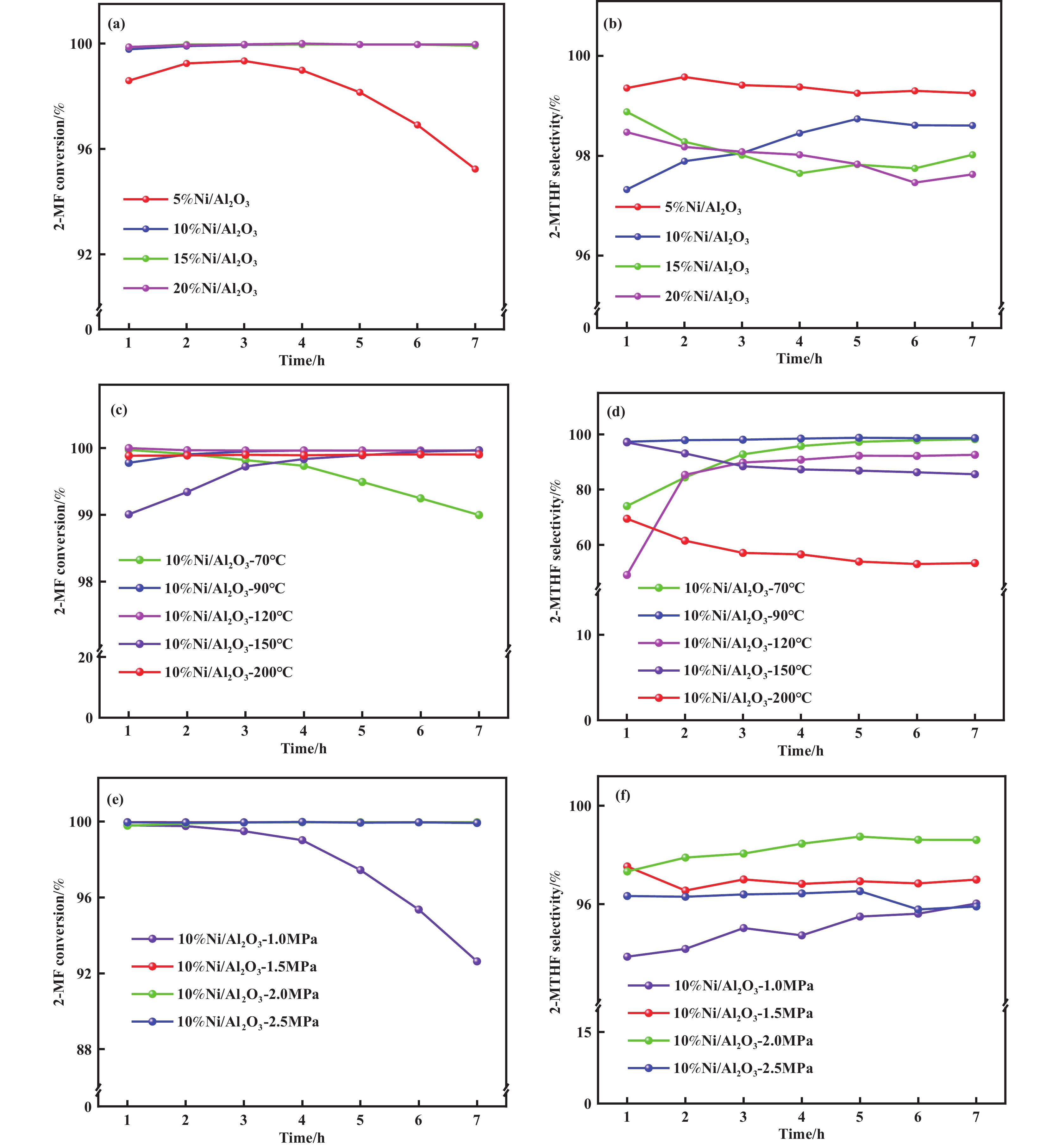
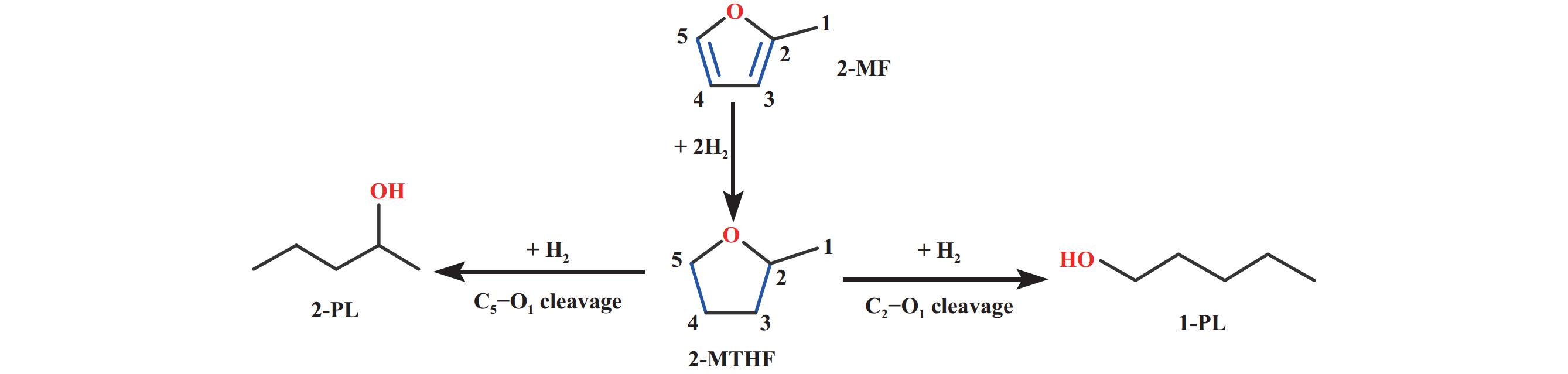
不同Ni/Al2O3催化剂对于2-MF气相加氢合成2-MTHF反应催化性能结果见图5, 具体数值总结于表2中. 在2 MPa, 90 ℃的反应条件下, 5%Ni/Al2O3催化剂活性较低且失活较快, 仅仅反应7 h, 2-MF的转化率就由99.3%下降到了95.2%. 随着Ni含量增加, 催化剂的活性和稳定性均提高, 这是因为提高Ni含量增加了反应活性位的数量[32]. 2-MTHF选择性随着Ni负载量的增加而减小, 5%Ni/Al2O3催化剂上2-MTHF选择性为99.3%, 而20%Ni/Al2O3催化剂2-MTHF选择性为97.7%, 见图5(b). 较高Ni含量的催化剂活性高, 但2-MTHF的选择性较低, 这是因为过高Ni负载量会使2-MF发生除C=C加氢外的反应: C—C键或者C—O键的断裂等, 从而引发聚合或者过度加氢反应, 生成副产物2-戊醇(2-PL)、2-戊酮(2-PN)、戊醇(1-PL) 等, 同时不同分子之间还可能发生缩合或者聚合反应, 也会降低主产物2-MTHF的选择性[12,33]. 在一定的反应条件下(2 MPa, 90 ℃), 10%Ni/Al2O3催化剂上2-MTHF的收率最高, 达到了98.5%. 反应温度对Ni/Al2O3催化剂上2-MF加氢性能影响较大: 70 ℃时, 2-MF转化率会随着反应时间的增长发生明显的下降, 如图5(c) 所示, 随着反应温度的升高, 催化剂的催化活性明显增强并保持稳定. 过高的反应温度使得2-MTHF的选择性出现了不同程度的降低, 当反应温度达到90 ℃的时候, 2-MF的转化率以及2-MTHF的选择性均比较高并保持稳定. 反应温度为200 ℃时, 2-MTHF的选择性仅有54.3%, 而副产物2-PL的选择性增加到31.9%. 2-PL是2-MTHF分子呋喃环上中C5−O1断裂、加氢生成的副产物, 而1-PL是2-MTHF分子中C2−O1断裂、加氢生成的副产物[34], 见图6. 在反应温度为70~200 ℃范围内, 2-PL的选择性随着反应温度增加迅速上升, 而1-PL的选择性变化不大, 说明升高温度会促进C5−O1断裂. 方姿予[18]在关于Ni/γ-Al2O3催化剂的研究也提到了反应温度会使C5−O1加速断裂进而生成2-PL. 此外, 在相同温度、空速下考察了不同反应压力下10%Ni/Al2O3催化剂对2-MF加氢性能的影响, 结果见图5(e、f). 当压力低于1.5 MPa时, 10%Ni/Al2O3催化剂很快出现了失活现象, 反应3 h之后转化率急剧下降. 随着反应压力的升高, 2-MF的转化率和2-MTHF的选择性均发生了明显的提升, 2.0 MPa反应时, 2-MTHF的选择性随着反应时间的增加, 由97.3%持续升高至98.6%以上并保持稳定. 过高的反应压力却使得2-MTHF的选择性下降, 如图5(f)所示, 当压力达到2.5 MPa时, 2-MTHF的选择性始终在97.1%左右, 压力升高副产物2-PL的选择性也逐渐上升. 该反应是放热反应, 压力的升高提高了催化加氢反应速率, 反应放热后床层温度迅速升高, 温度的增高使得C5−O1键断裂加速, 从而降低了2-MTHF的选择性[35].
|
图 5 催化剂的反应性能 Fig.5 Performance of the catalysts Reaction conditions: n(H2/2-MF)=6.4, WHSV=2.7 h−1, 1 g catalyst; (a, b) 90 ℃, 2 MPa; (c, d) 2 MPa; (e, f) 90 ℃ |
| 表 2 2-MF加氢产物分布 Table 2 Distribution of 2-MF hydrogenation products over catalysts |
|
图 6 2-MF加氢生成2-MTHF的反应路径示意图 Fig.6 Schematic diagram of the reaction pathway of 2-MF hydrogenation to 2-MTHF |
综上所述, 对催化加氢反应[36−39], 过高或过低的反应温度和压力对10%Ni/Al2O3催化剂在催化2-MF加氢反应中的表现均存在不利的影响. 当反应条件为2 MPa和90 ℃时, 2-MF的转化率以及2-MTHF的选择性均达到最佳水平, 2-MF转化率达到99.9%以上, 2-MTHF选择性达到了98.6%.
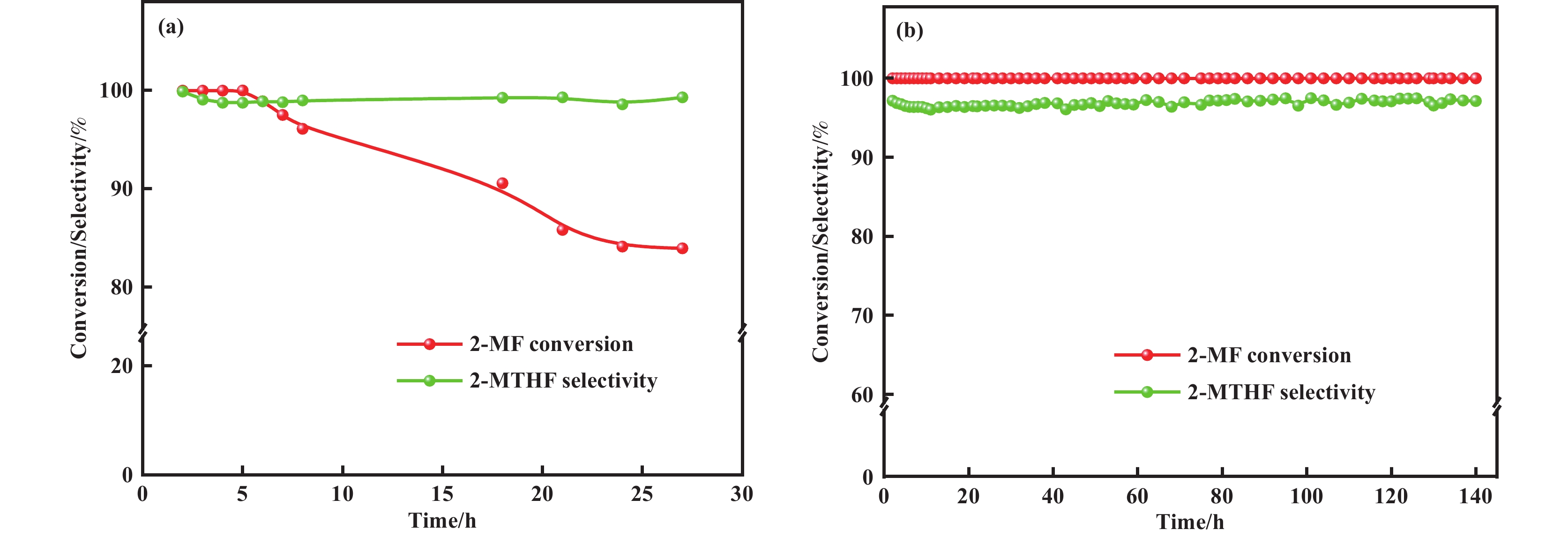
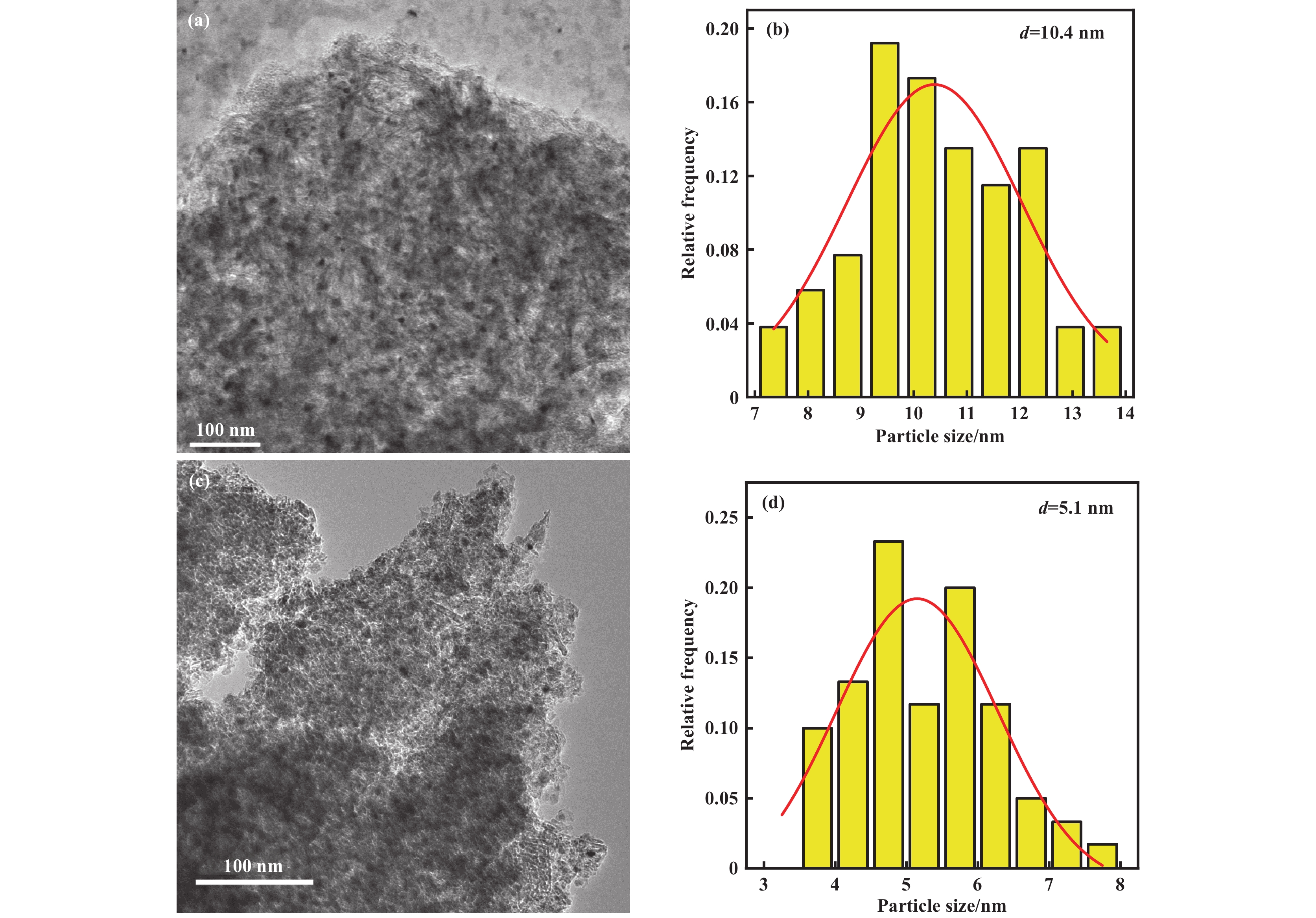
2.6 催化剂稳定性图7为5%和10%镍负载量的Ni/Al2O3催化剂在相同反应条件下的稳定性测试结果. 5%Ni/ Al2O3在27 h内出现了明显的失活现象, 2-MF转化率由初始99.9%逐渐下降至84.9%. 相比之下, 10%Ni/Al2O3展现出良好的稳定性, 连续反应140 h, 2-MF转化率始终维持99.9%以上, 稳定性能良好. 采用TEM表征了5%Ni/Al2O3、10%Ni/Al2O3催化剂反应后的形貌结构并进行了粒径分析, 见图8. 5%Ni/Al2O3催化剂经27 h反应后, Ni颗粒平均粒径由初始3.4 nm增长至10.4 nm, 增幅超过两倍, 呈现出典型的金属Ni聚集现象. 10%Ni/Al2O3催化剂经过140 h连续运行, 催化剂中金属Ni粒径未发生明显增大. 这说明当催化剂中Ni金属活性位点密度不足时, 催化性能会出现明显的下降趋势. 金属Ni颗粒的迁移-团聚过程, 也致使镍颗粒平均尺寸变大, 进一步降低催化剂的活性.
|
图 7 催化剂稳定性测试 Fig.7 Results of catalyst stability (a) 5%Ni/Al2O3, (b) 10%Ni/Al2O3 ; WHSV=2.7 h−1, n(H2/2-MF)=6.4, 90 ℃, 2 MPa |
|
图 8 使用后催化剂的TEM图像以及粒径统计 Fig.8 TEM images and Ni particles size distribution of used catalysts (a, b) 5%Ni/Al2O3; (c, d) 10%Ni/Al2O3 |
采用共沉淀法制备了不同Ni含量的Ni/Al2O3催化剂, 用于2-MF气相催化加氢反应制备2-MTHF. 随着Ni含量的增加, 催化剂的Ni晶粒尺寸逐渐增加, 金属-载体相互作用逐渐变弱. 10%Ni/Al2O3催化剂因均匀分散的Ni颗粒、较小的Ni粒径、较强的金属-载体相互作用表现出优异的反应活性和稳定性, 催化剂连续稳定运行140 h保持性能不变. 较低的Ni含量(5%)因活性位不足导致催化剂活性低, 会快速失活, 使用后催化剂中Ni颗粒会发生明显的聚集. 过高的Ni含量(20%)活性位点过多, 则会导致反应时副反应增加, 降低主产物2-MTHF选择性. 反应温度或压力过高会加速2-MTHF中C5−O1键断裂, 副产物2-PL选择性上升. 本研究为开发高效稳定的2-MF加氢非贵金属Ni基催化剂提供了良好的基础.
| [1] |
Molecular interactions between 2-methyltetrahydrofuran and alcohols: A combination of thermodynamic, spectroscopic and quantum chemistry studies[J]. J Mol Liq, 2024, 394: 123755.
DOI:10.1016/j.molliq.2023.123755 |
| [2] |
Combustion chemistry and flame structure of furan group biofuels using molecular-beam mass spectrometry and gas chromatography-Part I: Furan[J]. Combust Flame, 2014, 161(3): 748–765.
DOI:10.1016/j.combustflame.2013.05.028 |
| [3] |
Laminar burning characteristics of 2-MTHF compared with ethanol and isooctane[J]. Fuel, 2017, 190: 10–20.
DOI:10.1016/j.fuel.2016.11.036 |
| [4] |
Recent advancements on the use of 2-methyltetrahydrofuran in organometallic chemistry[J]. Monatsh Chem, 2017, 148(1): 37–48.
DOI:10.1007/s00706-016-1879-3 |
| [5] |
Selective and flexible transformation of biomass-derived platform chemicals by a multifunctional catalytic system[J]. Angew Chem Int Edit, 2010, 49(32): 5510–5514.
DOI:10.1002/anie.201002060 |
| [6] |
One-pot conversion of biomass-derived levulinic acid to furanic biofuel 2-methyltetrahydrofuran over bimetallic NiCo/γ-Al2O3 catalysts[J]. Mol Catal, 2022, 524: 112317.
DOI:10.1016/j.mcat.2022.112317 |
| [7] |
Cyclodehydration of 1,4-butanediols by pentaethoxyphosphorane[J]. J Org Chem, 1984, 49(15): 2831–2832.
DOI:10.1021/jo00189a044 |
| [8] |
Preparation of Ni/SiO2 by ammonia evaporation method for synthesis of 2-MTHF from 2-MF hydrogenation(蒸氨法制备Ni/SiO2催化剂及其在2-MF加氢制2-MTHF反应中的应用)[J]. J Fuel Chem Technol(燃料化学学报), 2021, 49(1): 97–103.
DOI:10.1016/S1872-5813(21)60007-5 |
| [9] |
Recent catalytic innovations in furfural transformation[J]. Green Chem, 2024, 26(19): 9957–9992.
DOI:10.1039/D4GC01983K |
| [10] |
Catalytic transfer hydrogenation of furfural to 2-methylfuran and 2-methyltetrahydrofuran over bimetallic copper-palladium catalysts[J]. ChemSusChem, 2016, 9(23): 3330–3337.
DOI:10.1002/cssc.201601122 |
| [11] |
One-step conversion of furfural into 2-methyltetrahydrofuran under mild conditions[J]. ChemSusChem, 2015, 8(9): 1534–1537.
DOI:10.1002/cssc.201500178 |
| [12] |
Efficient one-pot conversion of furfural into 2-methyltetrahydrofuran using non-precious metal catalysts[J]. Mol Catal, 2020, 490: 110951.
DOI:10.1016/j.mcat.2020.110951 |
| [13] |
Study on 2-Methylfuran hydrogenation catalyst(2-甲基呋喃加氢催化剂的研究)[J]. Shandong Chem Ind(山东化工), 2018, 47(6): 26–27.
DOI:10.19319/j.cnki.issn.1008-021x.2018.06.010 |
| [14] |
Highly selective hydrogenation of C=C double bond in unsaturated carbonyl compounds over NiC catalyst[J]. Chem Eng J, 2012, 188: 155–159.
DOI:10.1016/j.cej.2012.01.127 |
| [15] |
Partial oxidation of methane into syngas (H2+CO) over effective high-dispersed Ni/SiO2 catalysts synthesized by a sol-gel method[J]. Int J Hydrogen Energy, 2012, 37(10): 8343–8353.
DOI:10.1016/j.ijhydene.2012.02.141 |
| [16] |
Synthesis and catalytic performance of Ni/SiO2 for hydrogenation of 2-methylfuran to 2-methyltetrahydrofuran[J]. J Nanomater, 2015, 2015: 791529.
DOI:10.1155/2015/791529 |
| [17] |
Catalytic performance of Ni/Al2O3 catalyst for hydrogenation of 2-methylfuran to 2-methylte trahydrofuran(Ni/Al2O3 催化 2-甲基呋喃加氢制 2-甲基四氢呋喃性能的研究)[J]. J Fuel Chem Technol(燃料化学学报), 2018, 46(1): 54–58.
DOI:10.3969/j.issn.0253-2409.2018.01.007 |
| [18] |
Preparation of Ni/γ-Al2O3 and their catalytic performance for 2-MF gas phase hydrogenation(Ni/γ-Al2O3催化剂的2-MF气相加氢合成2-MTHF性能研究)[J]. J Mol Catal (China)(分子催化), 2023, 37(5): 461–472.
DOI:10.16084/j.issn1001-3555.2023.05.005 |
| [19] |
Research progress on the coupling of iron based bimetallic catalysts with peroxymonosulfate for pollutants removal(铁基双金属催化剂耦合过一硫酸盐去除污染物的研究进展)[J]. Environ Chem(环境化学), 2024, 43(11): 3909–3920.
DOI:10.7524/j.issn.0254-6108.2023052202 |
| [20] |
Highly loaded Ni-based catalysts for low temperature ethanol steam reforming[J]. Nanoscale, 2016, 8(19): 10177–10187.
DOI:10.1039/C6NR02586B |
| [21] |
Facile preparation of a Ni/MgAl2O4 catalyst with high surface area: Enhancement in activity and stability for CO methanation[J]. Main Group Met Chem, 2018, 41(3/4): 73–89.
DOI:10.1515/mgmc-2018-0003 |
| [22] |
The steam reforming of guaiacol for hydrogen via Ni/Al2O3: The influence of dispersion[J]. Int J Energy Res, 2020, 44(4): 2754–2767.
DOI:10.1002/er.5090 |
| [23] |
The impact of catalyst structure and morphology on the catalytic performance in NH3-SCR reaction: A review[J]. Fuel, 2024, 361: 130541.
DOI:10.1016/j.fuel.2023.130541 |
| [24] |
Reductive paths and the catalytic performance over Ni/AC catalyst(Ni/活性炭催化剂上还原途径及其催化性能)[J]. Chem React Eng Technol(化学反应工程与工艺), 2007, 3: 244–247.
DOI:10.3969/j.issn.1001-7631.2007.03.010 |
| [25] |
Temperature-programmed-reduction studies of nickel oxide/alumina catalysts: Effects of the preparation method[J]. Thermochim Acta, 1995, 256(2): 457–465.
DOI:10.1016/0040-6031(94)02177-P |
| [26] |
Comparison of reducibility and stability of alumina-supported Ni catalysts prepared by impregnation and co-precipitation[J]. Appl Catal A-Gen, 2006, 301(1): 16–24.
DOI:10.1016/j.apcata.2005.11.013 |
| [27] |
Rare earth oxides doped NiO/γ-Al2O3 catalyst for oxidative dehydrogenation of cyclohexane[J]. J Rare Earths, 2015, 33(6): 611–618.
DOI:10.1016/S1002-0721(14)60461-0 |
| [28] |
Optimal Ni loading towards efficient CH4 production from H2 and CO2 over Ni supported onto fibrous SBA-15[J]. Int J Hydrogen Energy, 2019, 44(14): 7228–7240.
DOI:10.1016/j.ijhydene.2019.01.259 |
| [29] |
Effect of Ni-based catalyst Ni particle size on dry reforming of methane reaction and its application prospect(Ni 基催化剂中Ni 颗粒粒径对甲烷干气重整反应的影响及其应用展望)[J]. Nat Gas Chem Ind(天然气化工—C1化学与化工), 2022, 47(2): 1–10.
DOI:10.3969/j.issn.1001-9219.2022.02.001 |
| [30] |
Design refinement of catalytic system for scale-up mild nitrogen photo-fixation[J]. Nano-Micro Lett, 2025, 17(1): 182.
DOI:10.1007/s40820-025-01695-3 |
| [31] |
Enhancing alkyne semi-hydrogenation through engineering metal-support interactions of Pd on oxides[J]. Nano Res, 2023, 17(5): 3707–3713.
DOI:10.1007/s12274-023-6280-z |
| [32] |
Bioethanol steam reforming for hydrogen production over Ni-Cr/SBA 15: Influence of metal loading and Ni/Cr ratio[J]. Molecules, 2025, 30(6): 1206.
DOI:10.3390/molecules30061206 |
| [33] |
High yield production of 2-methyltetrahydrofuran biofuel with reusable Ni-Co catalysts[J]. Fuel, 2023, 332: 126118.
DOI:10.1016/j.fuel.2022.126118 |
| [34] |
2-methylfuran vapor-phase hydrogenation on nickel-based catalysts: The effect of support(镍基催化剂上2-甲基呋喃气相加氢: 载体的影响)[J]. J Mol Catal (China)(分子催化(中英文)), 2024, 38(4): 331–341.
DOI:10.16084/j.issn1001-3555.2024.04.004 |
| [35] |
Synthesis of novel NaNi/C catalyst and selective hydrogenation study of furfural(新型NaNi/C催化剂合成及对糠醛选择性加氢的研究)[J]. J Beijing For Univ(北京林业大学学报), 2023, 45(1): 140–147.
DOI:10.12171/j.1000−1522.20220358 |
| [36] |
Nitrogen-doped ordered mesoporous carbon supported Co nanoparticles catalyzed hydrogenation of aliphatic amides(氮掺杂的有序介孔碳负载钴纳米颗粒用于脂肪酰胺的催化加氢)[J]. J Mol Catal (China)(分子催化(中英文)), 2024, 38(3): 208–214.
DOI:10.16084/j.issn1001-3555.2024.03.002 |
| [37] |
N-ligand regulated heterogenous copper catalyst for selective hydrogenation of cinnamaldehyde(1,10-菲啰啉修饰Cu/Al2O3催化肉桂醛羰基高效选择性加氢)[J]. J Mol Catal (China)(分子催化), 2023, 37(3): 213–224].
DOI:10.16084/j.issn1001-3555.2023.03.001 |
| [38] |
Confined Pd/TiO2 catalyst constructed by ALD for the hydrogenation of 1,4-butynediol(原子层沉积构筑Pd/TiO2限域催化剂及其在1,4-丁炔二醇加氢的应用)[J]. J Mol Catal (China)(分子催化), 2023, 37(4): 348–355.
DOI:10.16084/j.issn1001-3555.2023.04.004 |
| [39] |
Hydrocracking performance of kaolinite-based ZSM-5 zeolite for Jimsar shale oil(高岭土基ZSM-5沸石用于吉木萨尔页岩油加氢裂化反应性能研究)[J]. J Mol Catal (China)(分子催化(中英文)), 2024, 38(5): 448–456.
DOI:10.16084/j.issn1001-3555.2024.05.006 |
 2025, Vol. 39
2025, Vol. 39


